Часть первая. Оптимальное питание для веганов
Когда в публикациях, например, Немецкого общества питания (DGE), сообщается о так называемых жизненно важных питательных веществах в веганской диете, это не обязательно означает только то, что они необходимы каждому вегану. Это следует понимать и так, что многие веганы могут потенциально недополучить некоторые питательные вещества при обычном выборе продуктов питания. Тем не менее каждое из этих питательных веществ содержится в целом ряде продуктов растительного происхождения, которые могут полностью удовлетворить потребности организма в соответствующем питательном веществе.
В стандартах Немецкого общества питания (DGE) прописан ряд потенциально важных питательных веществ в рационе вегана. Однако не все из перечисленных питательных веществ одинаково важны. На рис. 3 показано, насколько сложно удовлетворить потребности в каждом из этих критически важных питательных веществ исключительно растительной пищей.
РИС. 3: ЖИЗНЕННО ВАЖНЫЕ ПИТАТЕЛЬНЫЕ ВЕЩЕСТВА В РАЦИОНЕ ВЕГАНА В ЗАВИСИМОСТИ ОТ ИХ ЗНАЧЕНИЯ ДЛЯ ОРГАНИЗМА [1]
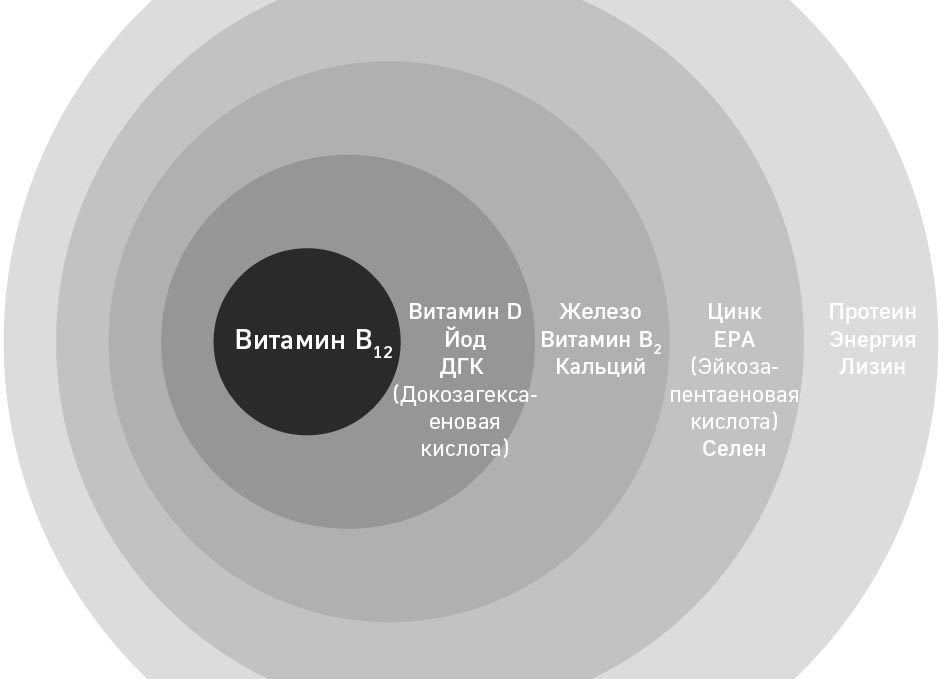
В центре рисунка находится витамин В12, который является наиболее редким питательным веществом в растительном рационе. Чем дальше от центра расположено питательное вещество, тем легче удовлетворить потребности в нем с помощью веганской диеты. Немецкое общество питания (DGE) или другие профессиональные сообщества, занимающиеся вопросами питания, не относят все остальные питательные вещества, не представленные на рисунке, к критически важным для веганского рациона. Такие питательные вещества априори представлены в необходимом количестве в рамках сбалансированного питания веганов с подсчетом калорий. Как будет показано в следующих разделах, теоретически потребность во всех этих важных питательных веществах можно полностью удовлетворить за счет потребляемой пищи. Однако на практике наиболее важные из них, такие как витамин B12, поступают в организм в виде пищевых добавок, поскольку растительные источники либо еще недостаточно изучены, либо не всем доступны.
Все питательные вещества, показанные на рис. 3, подробно представлены и объяснены в следующих разделах. Авторы уточняют, почему они признаны критически важными, какие продукты растительного происхождения лучше всего использовать для удовлетворения потребности в определенных питательных веществах и какие еще особенности необходимо принять во внимание. Несмотря на важность грамотно спланированного рациона веганов, наслаждение едой никогда не должно отходить на второй план. Таким образом, необходимо подобрать такую диету, которая подходит для повседневного следования ей, осуществима и доставляет удовольствие, обогащает жизнь и не усложняет ее без необходимости.
Глава 1. Белок
Несмотря на то что десятки мировых спортсменов-веганов добились высочайших результатов в самых разных видах спорта, некоторые публикации до сих пор ошибочно связывают растительно ориентированный рацион с недостатком силы, выносливости и работоспособности, а также с нехваткой белка. Однако успешные спортсмены показывают, что даже несколько лет исключительно растительной диеты не приводят к снижению физической силы. Так, спортсмен-силач и веган Патрик Бабумян в 2013 году установил мировой рекорд в ходьбе на 10 м с весом 555 кг на спине [1].
Ультрамарафонец Скотт Юрек, придерживающийся веганской диеты с 1999 года, побил множество рекордов, в том числе семь раз подряд победил в сверхмарафоне «Вестерн Стейтс», в забеге на 160 км [2].
Конечно, такие частные случаи не являются научно обоснованными доказательствами преимуществ растительной диеты, однако это важные примеры для научных публикаций о потребностях веганов в белке. Эти и сотни других спортсменов показывают, что такой режим питания работает не только в теории, но и на практике. Однако, поскольку Немецкое общество питания (DGE) называет белок одним из важнейших питательных веществ для веганов [3], в настоящей главе подробно объясняется, каким образом веганская диета может обеспечить достаточное количество высококачественного белка и в каких случаях в чисто растительной пище может наблюдаться его дефицит.
Основные сведения о белках
Слово «белок» (протеин) восходит к греческому рroteios, что в переводе означает «первый». Уже само название свидетельствует о взгляде диетологов на белок с момента его открытия. Наиболее важной функцией белков является его участие в построении тканей организма. Однако они также выполняют и ряд других задач. Большинство пищевых белков содержат двадцать необходимых человеку аминокислот, однако только восемь из них не могут быть синтезированы в организме взрослого человека. Поэтому такие белки считаются незаменимыми (необходимыми для поддержания жизнедеятельности) и должны поступать с пищей [4]. Некоторые другие аминокислоты незаменимы только при определенных обстоятельствах и поэтому называются условно незаменимыми или полузаменимыми. Например, аминокислота гистидин в одних случаях указывается как девятая незаменимая аминокислота, а в других – только как полузаменимая. Для взрослого человека эта аминокислота не играет такой роли, как для маленьких детей. Все остальные аминокислоты не являются незаменимыми, поскольку могут вырабатываться самим организмом при определенных условиях.
В конечном счете, для организма важен не сам белок, а только определенные аминокислоты [5].
Однако, поскольку они обычно поступают с пищевым белком, а не в изолированной форме, ниже мы рассмотрим вопрос потребности организма в белке.
Восемь незаменимых аминокислот включают фенилаланин, изолейцин, лизин, валин, метионин, лейцин, треонин и триптофан. Чтобы обеспечить потребность во всех этих аминокислотах, нужно потреблять их в объемах, определенных рекомендуемыми дозировками. Однако если следовать приведенным в настоящей главе советам по выбору продуктов питания для удовлетворения потребностей в белке, то можно не пользоваться отдельными рекомендациями по дозировке, поскольку при выборе правильных растительных продуктов учитывается общее потребление белка.
Расчет необходимого количества белка
По данным Немецкого общества питания (DGE), официально рекомендованное суточное потребление белка составляет 0,8 г белка на 1 кг массы тела для людей с нормальным весом [6]. Это соответствует рекомендациям многих других соответствующих организаций, например, рекомендациям Всемирной организации здравоохранения (ВОЗ), которая рекомендует потреблять 0,83 г легкоусвояемого белка в сутки на 1 кг массы тела [7]. Людям с избыточной массой тела при расчете суточной потребности в белке следует ориентироваться не на фактическую массу тела, а на теоретически нормальный или идеальный вес. В противном случае существует опасность передозировки. Идеальную массу тела можно рассчитать с помощью различных методов, таких как индекс Брока или формула Хамви, или определить по стандартным таблицам, составленным с учетом пола [8]. Официально суточная норма потребления белка (0,8 г на 1 кг массы тела) рассчитана с запасом индивидуальных особенностей организма. Таким образом, суточные нормы не являются абсолютным минимумом, а скорее оптимальным количеством. По данным Европейского агентства по безопасности продуктов питания (EFSA), при условии потребления легкоусвояемых и высококачественных белков в сутки организму реально требуется всего 0,66 г белка на 1 кг массы тела [9].
Если предположить, что женщина с нормальной массой тела весит 60 кг, то ее суточная потребность в белке составит 48 г в соответствии с рекомендованными Немецким обществом питания 0,8 г белка на 1 кг массы тела. При средней энергетической ценности 4,1 ккал на каждый грамм белка это соответствует суточному потреблению чуть менее 197 ккал из белка. При суточной норме калорий для женщин в 1 800-2 100 ккал [10] в зависимости от уровня активности это составляет около 10 % общей энергетической ценности суточного рациона. Как будет подробно описано ниже, некоторые источники рекомендуют для чисто веганской диеты несколько большее потребление белка – 0,9 г на 1 кг массы тела, поэтому в дальнейшем мы будем ориентироваться именно на это значение.
Хотя у спортсменов общая норма белка выше, потребность в калориях у них также увеличена.
Таким образом, повышенное потребление калорий существенно увеличивает суточную норму белка при достаточно высоком так называемом «белково-энергетическом балансе», т. е. проценте калорийности при потреблении белка по отношению к общей энергетической ценности.
Если это соотношение составляет 10 % и более, то этого достаточно, даже если белок усваивается несколько хуже [11].
Получают ли веганы достаточно белка?
На вопрос о том, способна ли исключительно растительная диета покрыть потребности человека в белке, еще в 1946 году [12] ответил американский диетолог д-р К. Дэвид Марк Хегстед в одной из своих публикаций.
Он подчеркивал, что чисто растительная диета, основанная на зерновых культурах, может удовлетворить потребность человека в белке при достаточном потреблении калорий.
Он основывался на результатах своего исследования с участием 26 респондентов, которые смогли достичь положительного азотистого баланса с помощью чисто растительной диеты с содержанием белка всего 0,5 г на 1 кг массы тела. Положительный азотистый баланс является важным параметром, показывающим, что взрослый человек потребляет достаточное количества белка.
Кроме того, возможность удовлетворения потребности в белке исключительно за счет пищи растительного происхождения подтвердили ученые д-р Вернон Янг и д-р Питер Пеллетт в работе 1994 года о важности белков растительного происхождения в питании человека. Эта публикация также показала, что в рамках сбалансированной, чисто растительной диеты не стоит беспокоиться о дефиците белка при достаточном потреблении калорий [13]. При этом авторы указали на опасность того, что роль растительных белков в рационе человека может быть недооценена на основе результатов стандартных экспериментов по оценке качества белка. Первые такие исследования проводились в основном на грызунах, которых кормили различными видами белка для построения выводов о его качестве на основе роста животных. Однако, поскольку растительные белки часто содержат меньше аминокислот, в которых крысы нуждаются больше, чем люди, опыты по кормлению крыс могут умалить ценность растительных источников белка для человека [14]. В конце своей работы ученые наглядно отобразили в таблице все распространенные мифы о белках и объяснили, что в них правда, а что ложь. Этот подход вдохновил нас на включение подобных таблиц с мифами и реальным положением вещей в конце каждой главы настоящей книги.
Результаты нескольких исследований, проведенных в Великобритании [15], Швеции [16], Германии [17], Швейцарии [18] и США [19], также подтвердили, что веганы в среднем получают более 10 % калорий из белка, что соответствует официальным рекомендациям по его суточному потреблению при достаточном количестве калорий. С момента публикации в 2003 году новаторского документа Американской академии питания и диетологии (AND, ранее известной как Американская диетическая ассоциация, ADA) было также официально подтверждено, что оптимально сбалансированный рацион веганов может обеспечить достаточное количество белка в любом возрасте [20]. Этот документ был обновлен в 2009 [21] и в 2016 годах [22], и с момента его первой публикации в нем неизменно рекомендуется веганская диета для каждого человека в любом возрасте, занимающегося любым видом спорта. Другие сообщества диетологов, такие как Британская ассоциация диетологов (BDA), также не видят никаких трудностей с потреблением белка в любом возрасте при правильно сбалансированной веганской диете [23]. В заявлении о веганском питании Ассоциация диетологов Австралии (DAA) даже не поднимает проблему дефицита белка, а указывает на важность достаточного потребления железа, кальция, витамина B12 и жирных кислот омега-3 [24].
Американская кардиологическая ассоциация (AHA) также подчеркивает, что для получения достаточного количества белка не обязательно потреблять продукты животного происхождения, а растительные белки содержат достаточное количество незаменимых аминокислот при условии разнообразности питания и соблюдения норм по калориям [25].
Растительные источники белка
Будучи веганом, можно легко рассчитать достаточность суточной нормы потребляемого белка, используя любой набор бобовых, цельнозерновых, орехов и семян, в бесплатных калькуляторах питания, таких как Cronometer (www.cronometer.com). Вы обнаружите, что уже потребляете достаточно белка в сутки, а в то же время вы еще не набрали минимальное необходимое количество калорий за день. Таким образом, вы сможете включить достаточное количество низкобелковых, но очень полезных фруктов и овощей для получения оставшегося количества калорий. Однако содержание белка в переработанных пищевых продуктах, таких как тофу, в значительной степени зависит от производителя, поэтому всегда следует проверять информацию о пищевой ценности на упаковке для фактического расчета белка. Следует также отметить, что сухие продукты, такие как чечевица и макароны, значительно увеличивают свою массу при варке, и поэтому при расчете белка всегда следует различать сухой вес (до варки) и вес приготовленного продукта. В прошлом эта путаница неоднократно приводила к появлению в Интернете графиков, сравнивающих содержание белка в бобовых и мясе, в соответствии с которыми черная фасоль почему-то содержала почти вдвое больше белка, чем говядина. Однако на них сушеную фасоль сравнивали с сырой говядиной, что давало неверную информацию о бобовых, поскольку при варке фасоль увеличивается больше, чем мясо. Поэтому важно сравнивать вареные бобы с вареным мясом. После варки бобовые по-прежнему содержат достаточно белка и других питательных веществ, поэтому не стоит пренебрегать ими. На рис. 5 показано увеличение массы сухих продуктов, таких как бобовые, макаронные изделия, крупы и другие продукты, в процессе приготовления.
Для расчета содержания белка в готовых продуктах с использованием коэффициентов, приведенных ниже, необходимо сначала взять количество белка в сухом продукте из таблиц пищевой ценности, а затем по правилу пропорциональной зависимости рассчитать количество белка, содержащегося в готовом продукте по сравнению с сухим.
Если, например, используется красная чечевица с содержанием белка 24 г на 100 г сухого веса, то для получения среднего веса в вареном виде это количество умножают на коэффициент 2,25 в соответствии с формулой на странице 34. Таким образом, 100 г сухой чечевицы дают в среднем 225 г в вареном виде, которые по-прежнему содержат 24 г белка. Однако эти 24 г распределены уже не в 100 г, а в 225 г, поскольку чечевица в процессе приготовления впитала воду и, соответственно, увеличилась в объеме. Таким образом, в вареной чечевице содержится всего около 10 г белка на 100 г. Однако точное количество набранного веса зависит от сорта, а также от точного времени замачивания и варки, количества используемой воды и может использоваться только в качестве приблизительного ориентира. Приведенные значения являются средними, и, например, одно и то же киноа может увеличиться в весе в 2,75, или в 3 раза, или даже в 3,25 раза в зависимости от перечисленных условий. Подобные колебания наблюдаются и у других сухих продуктов. Поэтому, если вы хотите знать, сколько именно весит итоговый продукт, стоит готовить его самостоятельно.
Ориентиры для расчета увеличения массы сухих продуктов в процессе варки
Изменения в весе сушеных зерновых и бобовых в результате приготовления:
– Неповрежденные цельнозерновые крупы (полба, овес и т. д.) ×2.
– Бобовые ×2,25.
– Бобовые, крупяные и макаронные изделия ×2,25.
– Амарант ×2,5.
– Киноа/гречка/пшено ×2,75.
– Кускус ×3.
– Подсолнечный фарш и соевые кусочки (TVP) ×3,25.
Сухой вес × коэффициент = вес в приготовленном виде
Вес в приготовленном виде ÷ коэффициент = сухой вес
Точный вес зависит от сорта, времени замачивания и приготовления
На рис. 4 представлена информация о содержании белка в ряде богатых им растительных источников, при этом содержание белка в обычных сухих продуктах, таких как бобовые и зерновые, уже пересчитано на содержание в вареном виде. Это дает первоначальное представление о том, какие растительные продукты особенно подходят для удовлетворения суточной потребности в белке.
РИС. 4: СОДЕРЖАНИЕ БЕЛКА В НЕКОТОРЫХ ПРОДУКТАХ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ [27, 28, 29]

Как видно из рис. 4, в некоторых растительных продуктах значительное количество белка. Например, в тыквенных семечках, семенах конопли, арахисе и т. д. Однако они также содержат большое количество жира, а значит, и калорий, поэтому такие продукты лучше рассматривать как прекрасное дополнение рациона, но в качестве основных источников растительного белка больше подходят бобовые, цельнозерновые культуры. Хотя в этих продуктах немного меньше белка на 100 г, они содержат гораздо меньше калорий за счет меньшего содержания жира, что увеличивает их ценность в качестве источников белка.
Следующий пример показывает, насколько легко получить рекомендуемую норму белка в веганской диете за счет бобовых и цельнозерновых продуктов с добавлением орехов и семян. Например, если испытуемая весом 60 кг выбирает на завтрак омлет, состоящий из 120 г тофу (15 г белка), 100 г грибов (3 г белка), 10 г тыквенных семечек (3,5 г белка) и двух ломтиков ржаного хлеба сорта «пумперникель» (5 г белка), а на обед готовит 180 г отварной чечевичной пасты (сухой вес 80 г, 22 г белка) с 200 г томатного соуса (3 г белка) и 20 г кешью (4 г белка), то согласно простому расчету она уже потребляет более 55 г белка, чем за первую половину дня покрывает больше его суточной нормы. Вместо этого на завтрак можно было бы съесть цельнозерновой хлеб с хумусом (с тахини) и перцем или овсяные хлопья с соевым молоком, орехами, молотыми семенами льна и фруктами, которые также весьма богаты белком. На обед, например, можно было бы приготовить быстрый салат из киноа с листьями шпината и горошком с арахисовой заправкой или чечевичный суп с коричневым рисом и кусочками поджаренного миндаля. На ужин лучше выбрать сливочный овощной карри из нута с небольшим количеством миндального масла и пшеном на гарнир или овощное рагу с темпе, киноа и жареными семечками подсолнечника. На что бы не пал выбор, присутствие в ежедневном рационе цельнозерновых и бобовых продуктов с добавлением орехов или семян вполне удовлетворит потребность в белке. Однако при всем оправданном внимании к белку не следует пренебрегать потреблением овощей и фруктов. Хотя ни одна из этих групп продуктов не дает большого количества белка, они богаты целым рядом витаминов и фитохимических веществ и поэтому также должны занимать особое место в питании веганов.
Растительный белок или животный белок?
В ходе часто односторонних дискуссий на тему того, какая пища – животная или растительная – богаче белком, нередко забывают о том, что продукты потребляются не только из-за содержания в них этого макронутриента. Когда вы едите грецкие орехи, вам важен не только белок, но и высокая доля жирных кислот омега-3 и витамина Е. В случае с темпе, помимо белка, ценят и содержащиеся в нем клетчатку, фитохимические вещества и целый ряд жирных кислот.
Пища всегда представляет собой набор питательных веществ, и к ней следует относиться именно так. Поэтому рассуждения о том, в какой пище больше белка, не имеют особого смысла.
Тем не менее необходимо отметить два различных метода оценки продуктов с высоким содержанием белка. Один из них основан на абсолютном содержании белка, информацию о котором всегда можно найти на упаковке продукта. Если вы покупаете товар на развес или по каким-либо другим причинам содержание белка не указано на упаковке, достаточно обратиться к таблице пищевой ценности любого автора. Другой, не менее актуальный метод – определение содержания белка по отношению к общей калорийности продукта. Поскольку продукты животного происхождения не содержат клетчатки, их калорийность обычно выше, чем у растительной пищи. Так как суточная потребность в питании в подавляющем большинстве случаев измеряется в калориях, эта оценка безусловно важна. Поэтому особое значение приобретает фактическое соотношение калорийности жиров, белков и углеводов. Так, в 1 г жира калорий более чем в два раза больше, чем в 1 г белка или 1 г углеводов. Разберем разницу в содержании белка в зависимости от массы и калорийности на примере вареной чечевицы и вареных яиц.
Вареные яйца (пригодная для употребления часть без скорлупы) содержат около 12,6 г белка, 10,6 г жира и чуть менее 1,1 г углеводов на 100 г массы [30]. В пересчете граммов на проценты количество белка, жира и углеводов в яйцах составляет 51,9 %, 43,6 %, 4,5 % соответственно, причем содержание клетчатки – 0 %. Отсюда можно сделать вывод, что яйца состоят из белка чуть более чем наполовину, и с точки зрения массы макроэлемента это так и есть. Однако, поскольку жир, содержащий 9,3 ккал, обеспечивает в среднем более чем в два раза больше калорий, чем белки и углеводы вместе взятые (около 4,1 ккал/г у каждого), соотношение калорий иное, и в яйцах содержание белка составляет лишь около трети калорийности. В пересчете на калории яйца состоят примерно из 33,4 % белков (51,7 ккал), 63,7 % жиров (98,6 ккал), 2,9 % углеводов (4,5 ккал) и 0 % клетчатки (0 ккал). С этой точки зрения видно, что хотя яйцо действительно содержит много белка, на самом деле его калорийность обеспечивается больше за счет жира, чем за счет белка.
В вареной красной чечевице на 100 г продукта содержится около 10,4 г белка, 0,7 г жира, 18,0 г углеводов и 7,6 г клетчатки [31]. Таким образом, соотношение макронутриентов в чечевице составляет 28,3 % белка, 1,9 % жира, 49,1 % углеводов и 20,7 % клетчатки. Клетчатка также является углеводом, но поскольку организм может использовать ее для производства энергии лишь в очень ограниченном объеме, в обычных таблицах пищевой ценности она учитывается только как 2 ккал/г вместо 4,1 ккал/г. Если сравнить процентное соотношение калорий в макронутриентах, то чечевица содержит 30,9 % белка (42,6 ккал), 4,7 % жира (6,5 ккал), 53,4 % углеводов (73,8 ккал) и 11,0 % клетчатки (15,2 ккал). Процентное содержание белка в яйце существенно различается в обоих случаях (51,9 % против 33,4 %). Это объясняется более высокой долей богатого калориями жира в яичном желтке по сравнению с низким содержанием жира в чечевице.
В процентном соотношении чечевица имеет почти такое же содержание белка, как и яйца, – чуть меньше трети. Эти значения станут еще больше равными, если далее рассчитать, сколько еще чечевицы можно съесть благодаря ее несколько меньшей калорийности, чтобы получить то же количество калорий, что и в яйце.
Вареные яйца в среднем содержат 155 ккал на 100 г пригодного для употребления продукта (без скорлупы) [32]. Свежеприготовленная красная чечевица содержит около 138 ккал на 100 г продукта [33]. Таким образом, можно съесть около 112 г чечевицы, чтобы получить то же количество калорий, что и в яйцах (155 ккал), и получить 11,6 г белка, что всего на 1 г меньше, чем в яйце.
Дефицит белка означает дефицит калорий
В большинстве случаев дефицит белка связан с дефицитом калорий, которого не возникает при сбалансированном веганском питании. Например, «Исследование веганов в Германии» (DVS) показывает, что, хотя участвовавшие в нем веганы потребляли в среднем более 10 % калорий в виде белка, около 25 % испытуемых не потребляли рекомендуемого общего суточного количества белка [34], так как в целом количество калорий в их рационе было недостаточным.
Проще говоря: недостаток белка в веганской диете обычно также означает недостаток калорий. Можно избежать и того и другого, потребляя достаточное количество калорий в виде разнообразной, полезной растительной пищи.
Единственными возможными исключениями из этого общего утверждения являются несколько очень строгих форм веганства. К ним относятся, среди прочего, жестко ограниченное сыроедение, в котором практически или полностью отсутствуют цельнозерновые и бобовые продукты. Как показывают данные Гиссеновского исследования сыроедения, у некоторых людей, питающихся исключительно сырой пищей, действительно наблюдается недостаток белка и калорий [35]. Так, чистые фрукторианцы, придерживающиеся весьма жестких рекомендаций, например, следуя диете 80/10/10 (углеводы/жиры/белки) по доктору Дугласу Грэму, рискуют получать слишком мало белка и других необходимых питательных веществ. Хотя эта диета нацелена на 10 % белка, некоторые ее приверженцы не потребляют норму из-за высокой доли фруктов и ограниченного количества листовых овощей, орехов и семян, а также полного отсутствия цельнозерновых и бобовых продуктов. Такие идеи, как «фрукты содержат все питательные вещества, необходимые нашему организму, именно в тех пропорциях, которые нам нужны» [36], ошибочны и создают неверное представление о растительной диете, которая должна отвечать нашим потребностям. Даже в сочетании с обилием овощей с темно-зелеными листьями в некоторых случаях диета 80/10/10 не обеспечит необходимой нормы белка и некоторых других питательных веществ. Только потребление большого количества орехов и семян могло бы дать рекомендуемую норму белка, однако, этот объем намного превышает требования диеты 80/10/10 с учетом 10 % жира. В этом можно легко убедиться, введя любое сочетание фруктов, (листовых) овощей и небольшого количества орехов в соответствии с вашими потребностями в калориях на сайте www.cronometer.com и рассчитав потребление белка, аминокислот и общего количества питательных веществ. Кроме того, негативное отношение к бобовым и цельнозерновым в рамках таких диет не отражает современной научной точки зрения, как показано в главах, посвященных этим культурам, и поэтому нет никаких оснований исключать эти две полезные и важные для здоровья группы продуктов из питания веганов. Таким образом, когда в рамках настоящей работы мы говорим о веганской диете, мы имеем в виду не какие-то особые и строгие формы растительного рациона, а скорее сбалансированную, здоровую, полезную диету на основе растительных источников с большим количеством цельнозерновых и бобовых продуктов, овощей, фруктов, орехов и семян.
Оптимальное обеспечение белками
Хотя с чисто математической точки зрения вряд ли возможно снизить уровень белка ниже минимального в рамках полноценной веганской диеты с необходимым количеством калорий, все же следует стремиться к оптимизации потребления белка, а не к обеспечению его достаточного количества. Этого можно легко достичь в случае питания исключительно растительными продуктами. Необходимо учесть лишь несколько моментов. Помимо соблюдения норм калорийности рациона, есть одно серьезное препятствие, которое стоит между некоторыми веганами и оптимальным потреблением белка: недостаточное количество бобовых. Бобовые полезны во многих отношениях, но в нашем случае особенно важно относительно высокое содержание в них незаменимой аминокислоты лизина [37].
Многие веганы едят бобовые слишком редко и поэтому упускают из своего растительного рациона лучшие источники белка и лизина.
Это особенно верно, если учитывать количество белка в соотношении с калорийностью. Орехи и семена также богатые источники белка, а иногда и лизина, однако при этом они содержат значительно больше калорий на 100 г из-за более высокого содержания жира.
Лизин участвует в синтезе мышечного белка, некоторых гормонов [38], а также важен для заживления ран [39] и оптимального обмена кальция [40] и железа [41] в организме. Кроме того, он предположительно может защищать от выпадения волос [42]. По данным ВОЗ, человеку требуется около 37 мг лизина на 1 кг массы тела (с учетом индивидуальных особенностей) [43]. Для женщины весом 60 кг суточная норма составляет 1800 мг. Если бы такая женщина попыталась получить норму лизина с помощью не бобовых, а, например, цельнозерновых продуктов, ей бы это удалось, хотя это было бы непросто. В случае с бобовыми ей потребовалось бы всего около 190 г вареного гороха или 200 г вареного маша, чтобы получить суточную норму лизина (1800 мг). Конечно, не обязательно есть столько бобовых, поскольку лизин можно получить и из других продуктов питания, но этот пример показывает, каким хорошим источником лизина они являются. Чтобы получить норму лизина с помощью цельнозерновых продуктов, необходимо съесть около 600 г цельнозернового хлеба или 400 г овсянки. Что касается орехов, то необходимые для потребления лизина 240 г кешью или 310 г миндаля покрыли бы почти всю суточную норму калорий из-за высокого их содержания в орехах [44]. Количество белка и лизина во фруктах и овощах очень низкое, причем лизин присутствует в минимальной дозе. Для наглядного сравнения на рис. 5 представлены данные о содержании лизина в отдельных продуктах питания.
РИС. 5: СОДЕРЖАНИЕ ЛИЗИНА В ОТДЕЛЬНЫХ ВИДАХ РАСТИТЕЛЬНОЙ ПИЩИ [45]

Растительные продукты с низким содержанием лизина сами по себе не являются бесполезными, поскольку некоторые из них богаты многими другими важными питательными веществами. Однако они не вносят существенного вклада в обеспечение организма лизином, поэтому их следует ежедневно сочетать с богатыми этой аминокислотой продуктами. Если кто-то не ест бобовые, то потребность в лизине можно восполнить с помощью некоторых псевдозерновых культур, например киноа и амаранта, в сочетании с орехами, такими как кешью и миндаль, или обезжиренной ореховой мукой. Однако благодаря огромной пользе бобовых их лучше есть, по возможности, каждый день или как минимум несколько раз в неделю.
Определение качества белка
Раньше считалось, что растительный белок уступает животному. Однако это мнение основано на результатах экспериментов по оценке белка, каждый из которых имеет серьезные ограничения и, следовательно, не может адекватно отражать реальные требования, предъявляемые к растительным белкам.
За последние десятилетия для вычисления качества белков были разработаны, по сути, три системы оценки: коэффициент эффективности белка (PEV), биологическая ценность (BW) и аминокислотный коэффициент усвояемости белков (PDCAAS).
В рамках PEV качество белка определяется в зависимости от его влияния на рост крыс по результатам экспериментов. Однако у крыс и других грызунов потребность в некоторых серосодержащих аминокислотах значительно выше, чем у человека, поэтому оценка с помощью PEV дает более высокую норму белка для человека и занижает потребность в растительных белках из-за относительно низкого содержания в них серосодержащих аминокислот [46]. Это наглядный пример того, что эксперименты на животных имеют серьезные ограничения и часто не могут быть перенесены на человека, поэтому опыты на животных не только неприемлемы с этической точки зрения, но и часто могут давать ложные результаты.
Вероятно, наиболее популярным методом является определение качества белка с помощью биологической ценности. Этот способ оценивает эффективность использования организмом пищевого белка. Организм применяет пищевой белок оптимально, если он содержит большое количество незаменимых аминокислот, наиболее полно отвечающих потребностям человека [47]. Эта система также имеет определенные особенности, поскольку некоторые этапы подготовки, например, проращивание [48], повышают концентрацию незаменимых аминокислот в бобовых и зерновых культурах. Как и в случае с методом PDCAAS, описанном ниже, при интерпретации биологической ценности всегда следует оценивать весь спектр аминокислот для суточного рациона, а не их содержание в отдельном продукте или за конкретный прием пищи. Это важно, поскольку наборы аминокислот различных продуктов питания могут дополнять и, таким образом, усиливать друг друга в течение дня.
В настоящее время аминокислотный коэффициент усвояемости белков (PDCAAS) является популярным способом оценки пищевых белков, в частности, их аминокислотного состава в соответствии с реальными потребностями человека в аминокислотах [49]. Однако большинство результатов оценки белка на основе PDCAAS не учитывают взаимодействие различных пищевых белков и их взаимное усиление, а также различия и изменения в усвояемости, вызванные приготовлением. При варке источников растительного белка, например, бобовых, высокие температуры могут значительно снизить содержание некоторых веществ, влияющих на процесс пищеварения, таких как ингибиторы ферментов, тем самым повышая усвояемость [50]. По сравнению с сырым состоянием растительный белок вареных бобов в среднем усваивается примерно на 15 % лучше, а если бобовые перед приготовлением замачиваются на 12 часов, то после замачивания и варки их усвояемость увеличивается в целом на 25 % [51]. В другом исследовании значения PDCAAS для фасоли практически удвоились за счет термообработки [52].
Независимо от того, потребляете ли вы отдельные продукты с высоким или низким PDCAAS, в конечном итоге эти значения не так важны для повседневной жизни веганов, придерживающихся сбалансированной по калориям диеты, как для практических экспериментов по исследованию белков. В прошлом результаты таких опытов уже подвергались критике за возможное завышение потребности в аминокислотах (особенно в лизине) и, следовательно, за переоценку рекомендованных норм [53]. Кроме того, они недостаточно учитывают способность организма адаптироваться к различным уровням потребления белка и многие другие факторы, на которые влияет пищевая обработка и комбинации продуктов.
Небольшое увеличение суточной нормы белка, как это предлагается и объясняется далее в качестве меры предосторожности для веганов, может легко компенсировать любые пониженные показатели белка, поэтому не составит большого труда обеспечить необходимое количество этого макронутриента, если следовать простым рекомендациям, приведенным в настоящей главе.
Сочетания белков
Теоретически, если белки поступают преимущественно из одного источника, не содержащего незаменимых аминокислот в достаточном для потребностей человека соотношении, это может привести к дефициту. Так, если человек питается в основном лишь одним видом зерна, это не удовлетворит его потребности в целом ряде питательных веществ, в том числе и аминокислот [54]. Однако если не просто есть зерновые или бобовые культуры, а ежедневно сочетать два основных продукта с орехами и семенами, то эти источники растительного белка будут дополнять друг друга и уравновешивать лимитирующие аминокислоты, повышая тем самым биологическую ценность питания.
Необходимость комбинирования белков объясняется довольно просто: хотя в принципе все растительные белки обычно содержат весь спектр незаменимых аминокислот, некоторые из них часто присутствуют в слишком малых количествах, поэтому их называют «неполноценными». Аминокислота, которая есть в белке в наименьшем количестве по сравнению с физиологической потребностью, называется «лимитирующей» и является причиной низкой биологической ценности некоторых растительных белков [55]. Например, если бы мы питались только пшеницей, то получали бы слишком мало незаменимой аминокислоты лизина. Треонин, метионин и триптофан также не содержатся в пшенице в оптимальных количествах, поэтому после восполнения дефицита лизина они станут следующими лимитирующими аминокислотами. Для наглядности эта ситуация представлена на рис. 6.
РИС. 6: БИОЛОГИЧЕСКАЯ ЦЕННОСТЬ НА ПРИМЕРЕ БЕЛКА ПШЕНИЦЫ [56]

Биологическая ценность на 100% соответствует эталонной (содержанию белка в яйце). Низкое количество лизина ограничивает усвоение остальных белков.
Если к зерну добавить очень богатый лизином продукт, который полностью компенсирует его нехватку, то это приведет к увеличению ценности белка до тех пор, пока мы не столкнемся со следующей лимитирующей аминокислотой, которой в нашем примере является треонин. Если дополнительный, так называемый «комплементарный белок» обеспечивает достаточное количество не только лизина, но и треонина, то ценность снова увеличится, пока мы не столкнемся с дефицитом следующей лимитирующей аминокислоты, которой в данном примере является метионин, а затем триптофан. Если комплементарный белок также может обеспечить достаточное количество этих аминокислот, то два белка дополняют друг друга и достигается оптимальная биологическая ценность. Теоретически она может быть даже выше 100 %.
Анализ традиционных национальных кухонь показывает, что сочетание зерновых с низким содержанием лизина с бобовыми, богатыми лизином, всегда входило в состав множества блюд.
Будь то рис с бобовыми в Азии, пшеница с бобовыми на Ближнем Востоке или кукуруза с бобовыми в Южной Америке [57]. Такие вкусные и богатые белком блюда, как жареный рис с тофу, хумус из нута с лепешками, фасоль с кукурузой и многие другие, уже сочетают в себе обе группы продуктов.
Эта идея о взаимодействии белков была также представлена в 1971 году в популярной книге Фрэнсис Мур Лаппе «Диета для маленькой планеты». Однако в то время была выдвинута гипотеза, которая впоследствии оказалась ложной, но до сих пор публикуется в некоторых книгах, блогах и журналах и имеет сторонников. Это миф о том, что для получения полноценных белков необходимо сочетать в одном приеме пищи различные неполноценные источники растительного белка [58]. Уже при переиздании книги в 1981 году, автор сама признала это утверждение ложным, заявив, что своей теорией сочетания белков она создала настоящий миф. Она подчеркивает, что получить достаточное количество высококачественного растительного белка гораздо проще, чем ей казалось вначале [59]. В своей публикации 1994 года д-р Вернон Янг и д-р Питер Пеллетт также четко указали, что количество аминокислот важно учитывать не за один прием пищи, а за весь день суммарно [60]. Ученые отмечают тот важный факт, что организм имеет значительный запас свободных аминокислот в мышцах, где определенные аминокислоты, поступившие с пищей, могут храниться в течение определенного периода времени. Если через несколько часов после еды человек употребит продукты, в которых не хватает одной или нескольких незаменимых аминокислот, организм может просто восполнить недостающие своими собственными из запасов в мышцах. Это означает, что, например, аминокислоты, полученные утром из цельнозернового хлеба, могут дополнить аминокислоты, полученные вечером из тофу в овощном жарком.
Таким образом, несмотря на важность ежедневного достаточного потребления всех восьми незаменимых аминокислот, не обязательно сочетать их в одном блюде. Если следовать рекомендациям Американского института исследования раковых заболеваний (AICR) и Всемирного фонда исследований рака (WCRF) и дополнять цельнозерновыми и/или бобовыми культурами каждый прием пищи [61], а также хотя бы раз в день съедать горсть орехов, то при достаточной калорийности рациона можно автоматически получить суточную норму белка, включая все незаменимые аминокислоты.
Рекомендованные нормы белка для веганов
Несмотря на то, что в процессе приготовления пищи усваивается большее количество растительного белка, а комплементарные белки оказывают взаимодополняющее воздействие, некоторые авторы советуют увеличить рекомендуемую норму белка для веганов с 0,8 г до 1 г на 1 кг массы тела, чтобы обеспечить получение нужных аминокислот при любых условиях [62]. Другие исследователи рекомендуют увеличить норму лишь на 5-10 % для рациона, основанного исключительно на растительных продуктах, что примерно составляет 0,9 г на 1 кг массы тела [63]. С другой стороны, данные метаанализа показали, что даже в рамках исключительно растительного питания сочетание различных комплементарных белков (например, из зерновых и бобовых культур) устраняет необходимость более высокой дозировки белка [64]. Например, для женщины с массой тела 60 кг увеличение нормы потребления белка до 0,9 г на 1 кг массы тела означает повышение общей суточной нормы с 48 до 54 г, а увеличение до 1 г белка на 1 кг массы тела приведет к повышению общего объема потребления до 60 г белка в сутки. Все три рекомендации справедливы для рациона, включающего исключительно растительные продукты.
Чтобы немного увеличить суточное потребление белка всем взрослым людям, не страдающим аллергией на сою, рекомендуется включать в рацион соевые продукты с минимальной обработкой.
Однако все остальные бобовые продукты могут также способствовать повышению объема потребляемого белка. К таким относятся, например, соевые бобы, эдамаме, тофу и темпе. Несмотря на более высокую степень обработки соевое молоко и соевый йогурт без сахара и масла также являются хорошей альтернативой. Просто замените в мюсли рисовое молоко (0,1 г белка на 100 мл) соевым (3,5 г на 100 мл), и разница составит более чем в 10 г белка на тот же объем жидкости при использовании 300 мл растительного молока. Несколько хрустящих жареных горошин нута в салате, темпе в овощном жарком, тофу в овощном карри или бобовая паста вместо цельнозерновых макарон – это лишь несколько идей того, как можно превратить практически любое блюдо в хороший источник белка, добавив в него бобовые без изменения самого блюда и без чрезмерного увеличения количества потребляемой пищи.
Как официально подтвердила Американская академия питания и диетологии в 2003 году в аналитическом документе по вегетарианскому и веганскому питанию, веганская диета может удовлетворить потребности в белке для любого вида спорта и любого человека в любом возрасте [65]. В табл. 1 приведены дозировки белка, рекомендованные Немецким обществом питания и скорректированные на 10 % до 0,9 г и на 25 % до 1 г на 1 кг массы тела в соответствии с различными особенностями веганов. Таблица дает представление об общем суточном потреблении белка веганами в различном возрасте. Поскольку данные не свидетельствуют однозначно в пользу одного из трех вариантов, каждый человек решает сам, сколько белка ему потреблять. Золотая середина между 0,8 и 1 г, составляющая для взрослых 0,9 г на 1 кг массы тела, может представлять оптимальный вариант, который несколько превышает норму, но может быть реализован без особых усилий.

Как видно из табл. 1, во время беременности и грудного вскармливания потребность женщин в белке возрастает. Если потребность в некоторых питательных веществах во время беременности увеличивается вдвое, то в отношении белка все несколько иначе. Рекомендуемое суточное потребление белка возрастает лишь на 20 % во время беременности и на 35 % во время грудного вскармливания. Нормы были скорректированы в сторону увеличения в соответствии с рекомендациями для беременных женщин, придерживающихся веганского образа жизни [67]. Потребность в белке у младенцев, безусловно, самая высокая по отношению к их массе тела, но белок в достаточном количестве поступает с молоком матери в течение первого полугода исключительно грудного вскармливания [68].
В последующие месяцы и годы процентная потребность в белке постепенно снижается, пока в возрасте около 65 лет не падает до 0,8 г на 1 кг массы тела, не изменяясь до конца жизни человека. Официальные рекомендованные Обществами питания Германии, Австрии, Швейцарии (D-A-CH) дозировки подразумевают несколько повышенное потребление белка для людей старше 65 лет [69]. Одни источники поддерживают эту рекомендацию, а другие советуют увеличить дозировку на 30 % [70]. Некоторые ученые рекомендуют как минимум умеренное увеличение суточного потребления белка до 1 г на 1 кг массы тела при смешанном питании [71, 72]. Мы учли это в нашей таблице и соответствующим образом адаптировали к рекомендациям для веганов. Международное общество спортивного питания (ISSN) советует активным спортсменам потреблять значительно больше белка по сравнению с обычными людьми [73]. Мы рекомендуем норму белка 1,0–1,6 г на 1 кг для видов спорта, сопряженных с развитием выносливости, 1,4–1,7 г на 1 кг для видов спорта с прерывистой нагрузкой, например, виды спорта с мячом и единоборства с прерывистыми силовыми нагрузками, и 1,4–2 г на 1 кг для культуристов и тяжелоатлетов.
Минимальное и максимальное потребление белка
Хотя веганы потребляют в среднем меньше белка, чем обычные люди на смешанном питании, пониженное количество не обязательно означает слишком малое. В сравнительном исследовании, проведенном в Швейцарии, группа испытуемых, придерживающихся смешанного питания, потребляла в среднем 85 г белка в день, а группа веганов – только 65 г [74], однако это количество составляло 11 % от среднего потребления калорий и, следовательно, было достаточным для удовлетворения потребностей веганов в белке. В другом исследовании веганы потребляли в среднем 14 % калорий в виде белка, причем веганы с самым высоким потреблением белка в группе получали таким способом до 19 % калорий [75]. Даже испытуемые из группы веганов с наименьшим потреблением белка в этом исследовании все равно потребляли более 10 % калорий за счет белка, что означает, что во всех группах наблюдалось оптимальное «соотношение белка и калорий».
Для всех питательных веществ существует не только рекомендуемая минимальная, но и максимальная норма потребления, хотя для таких питательных веществ, как белок, она не такая строгая, как для некоторых минералов, терапевтическое действие которых не такое широкое. Максимальное количество питательного вещества, которое можно потреблять в течение длительного времени без риска для здоровья, называется «верхним допустимым уровнем потребления» (Tolerable Upper Intake Level, UL)[3]. По данным Европейского агентства по безопасности продуктов питания (EFSA), в связи с ограниченностью имеющейся информации, для белка не может быть определен верхний допустимый уровень потребления, однако, по мнению EFSA, в течение длительного времени без риска для здоровья можно потреблять как минимум вдвое больше официально рекомендованной нормы [76]. Официальная рекомендация для небеременных взрослых женщин составляет 0,8 г белка на 1 кг массы тела при смешанном питании, поэтому без негативных долгосрочных последствий можно потреблять не менее 1,6 г белка на 1 кг массы тела. Таким образом, испытуемая весом 60 кг может потреблять до 96 г белка в день в рамках своего рациона. Если предположить, что присутствие в рационе растительных белков несколько меньше, а рекомендованные нормы потребления белка составляют 0,9–1,0 г на 1 кг массы тела, то верхний допустимый уровень потребления для чисто растительных белков будет еще выше – 108–120 г/сут.
Выводы к главе
Как было показано в настоящей главе, можно удовлетворить потребность в белке в любом возрасте, придерживаясь исключительно растительной диеты. В предыдущих исследованиях, посвященных определению ценности белков, растительные белки получили сравнительно невысокую оценку, однако многие результаты этих тестов следует поставить под сомнение из-за их многочисленных ограничений.
Сегодня разные международные организации, занимающиеся вопросами здравоохранения и питания, сходятся во мнении, что разумно построенный рацион и внимательное отношение к потреблению аминокислот, имеющих жизненно важное значение, таких как лизин, позволяют получать оптимальное количество белка из чисто растительных источников.
Поскольку незаменимая аминокислота лизин в большом количестве содержится в основном в бобовых культурах, такие продукты должны непременно присутствовать в ежедневном рационе веганов. Чтобы обеспечить достаточное количество белка для веганов в любой ситуации, в некоторых публикациях рекомендуется увеличить потребление белка на 5-25 % при чисто растительном питании, однако не все исследователи считают такое увеличение необходимым. Вопреки прежним представлениям, не обязательно сочетать различные растительные источники белка в одном приеме пищи для получения полного спектра аминокислот. Достаточно сочетать их в течение дня.
По примеру д-ра Вернона Янга и д-ра Питера Пеллетта, чья важная работа «Значение растительных белков и аминокислот для питания человека» [77] сопровождается наглядной таблицей с перечислением наиболее распространенных мифов о белках и объяснением реальных фактов, каждая глава этой книги также завершается подобным табличным сравнением.
Мифы – Реальность
Веганская диета не обеспечивает достаточного количества белка.
Сбалансированное питание вегана обеспечивает все незаменимые аминокислоты при достаточной калорийности рациона и, следовательно, может удовлетворить потребности в белке.
Спортсмены не могут удовлетворить свои повышенные потребности в белке исключительно за счет веганства.
Аналитические документы таких организаций, как Американская академия питания и диетологии, ясно показывают, что в любом виде спорта можно получать повышенную норму белка за счет исключительно растительной пищи, и многие успешные спортсмены-веганы демонстрируют это ежедневно.
Животные белки более ценны по сравнению с растительными.
Если анализировать растительные белки отдельно, то их биологическая ценность ниже, чем у животных белков, однако многие методы оценки качества белка имеют серьезные ограничения. Комбинируя различные источники растительного белка, можно значительно расширить спектр получаемых аминокислот, и таким образом ценность растительных белков становится сопоставимой качеству животных аналогов.
Для повышения качества растительных белков необходимо использовать комплементарные белки в составе блюд.
Аминокислоты различных белков могут дополнять друг друга в течение дня и не обязательно должны присутствовать в полном объеме в одном приеме пищи.
Веганам необходимо потреблять больше белка, чтобы компенсировать более низкую усвояемость и количество растительных белков.
В настоящее время нет единого мнения о том, требуется ли веганам больше белка. Для подстраховки некоторые институты рекомендуют умеренное увеличение потребления белка примерно на 10 % при чисто веганской диете.
Глава 2. Жирные кислоты омега-3
Так же как для большинства людей молоко является идеальным источником кальция, рыба представляет собой превосходный источник полезных жиров, которые необходимы для здорового питания. Речь идет о длинноцепочечных полиненасыщенных жирных кислотах омега-3 – эйкозапентаеновой (ЭПК) и докозагексаеновой (ДГК), которые в основном содержатся в больших концентрациях в жирной холодноводной рыбе, такой как лосось, сельдь, тунец и сардины. Они встречаются и во многих других видах рыб, однако уже в меньших количествах [1].
В более ранних обсервационных клинических исследованиях человеческого организма эти жирные кислоты уже связывали со снижением риска сердечно-сосудистых заболеваний [2] и, несмотря на некоторые противоречивые результаты, с возможным положительным влиянием на умственные способности людей пожилого возраста [3].
Поэтому некоторые считают отказ от употребления рыбы вредным для здоровья, в связи с чем возникает вопрос о последствиях отказа от рыбы в рамках веганской диеты.
В обсуждении этого вопроса часто не учитывают два ключевых момента. Во-первых, рыба не является фактическим поставщиком длинноцепочечных жирных кислот омега-3 (ЭПК и ДГК), она лишь накапливает в своих тканях те жирные кислоты, которые изначально поступают в пищевую цепь из некоторых микроводорослей [4]. В этой связи необходимо подчеркнуть, что продукты животного происхождения не обладают исключительностью в плане обеспечения определенными питательными веществами и никоим образом не являются первичными источниками всех содержащихся в них питательных веществ. Подобно тому, как каждый микроэлемент сначала попадает в растение из почвы, а в организм животного только с пищей, микроорганизмы как первичный продуцент синтезируют каждый витамин, который позже попадает в ткани животного только в пределах пищевой цепи. Аналогичным образом функционирует и пищевая цепь моря, где микроводоросли в качестве продуцентов синтезируют жирные кислоты омега-3, которые затем поедаются консументами первого порядка, такими как зоопланктон. Они, в свою очередь, служат источником пищи для консументов второго порядка, таких как рыба. Консументов второго порядка затем съедают консументы третьего порядка, например, лосось. Хотя в результате этого процесса в тканях лосося накапливаются жирные кислоты омега-3, было бы неправильно приписывать им животное происхождение.
Во-вторых, человеческий организм в принципе способен самостоятельно вырабатывать эти длинноцепочечные жирные кислоты, если он получает необходимое растительное сырье при определенных условиях. Именно по этой причине ЭПК и ДГК относят не к незаменимым (т. е. жизненно важным) жирным кислотам, а лишь к полузаменимым [5]. Способность организма вырабатывать ЭПК и ДГК у каждого человека разная, и эффективность зависит от нескольких факторов, которые будут подробно рассмотрены в настоящей главе. Однако прежде важно отметить, что ЭПК и ДГК изначально содержатся в растениях, и человеческий организм способен синтезировать их самостоятельно.
Начнем с самого низа пищевой цепи
Если необходимо получать уже готовые ЭПК/ДГК из пищи в случае неспособности организма к самостоятельному синтезу, то независимо от режима питания лучше использовать в качестве источника микроводоросли, а не рыбу. Помимо этических и экологических соображений, связанных с потреблением рыбы, важную роль здесь играют и вопросы здоровья. Хотя рыба обеспечивает относительно большое количество этих жирных кислот, она может содержать ряд нежелательных побочных продуктов, которых нет в масле из микроводорослей.
В пищевой цепи моря накапливаются не только жирные кислоты омега-3, но и другие вещества, например, так называемые «стойкие органические загрязнители» – диоксины и полихлорированные бифенилы (ПХБ). Поэтому для минимизации риска для здоровья следует начинать с низкого уровня пищевой цепи.
Не все, но некоторые исследования рассматривают рыбу как крупнейший источник таких опасных веществ. Они могут иметь негативные последствия не только для здоровья взрослых, но и для младенцев, которые еще не едят рыбу. Это связано с тем, что некоторые из этих веществ также выделяются с грудным молоком матери, которая могла употребить их вместе с рыбой, и поэтому могут нанести вред ребенку в первые несколько месяцев жизни [6]. Это не означает, что вся морская рыба содержит такие вещества, однако полученные результаты должны повысить уровень осведомленности об этой важной проблеме и указать на то, что альтернативные безвредные и экологически чистые источники представляют собой оптимальный вариант.
Даже аквакультуры не гарантируют того, что выращенная в них рыба не содержит этих веществ. В ходе широкомасштабного сравнения образцов лосося из США и Европы было установлено, что как дикий, так и выращенный лосось содержат некоторое количество ПХБ и диоксинов. Концентрация этих веществ в более чем 450 образцах фермерского лосося была в среднем даже выше, чем в лососе, выловленном в дикой природе [7].
Ученые пришли к выводу, что хотя некоторые виды рыбы являются хорошим источником омега-3, они могут содержать вредные вещества, что в конечном итоге ставит под сомнение истинность пользы употребления рыбы для здоровья.
Эта идея подтвердилась и в ходе дальнейшего исследования около 600 образцов дикого и культивированного лосося [8]. Результаты исследования также показали более высокий уровень токсичных веществ в культивированном лососе по сравнению с выросшим в естественной среде. Кроме того, была установлена связь между загрязнением соответствующего корма и мяса рыбы. Таким образом, более высокий уровень токсических веществ в культивированной рыбе, по-видимому, в значительной степени обусловлен зараженным кормом.
Даже если не учитывать возможное загрязнение нежелательными веществами, имеет смысл исключить рыбу как промежуточное звено в обеспечении ЭПК и ДГК и удовлетворять потребность в этих жирных кислотах непосредственно за счет микроводорослей, которые являются их непосредственными источниками [9]. В рамках нескольких исследований была проверена переносимость, эффективность действия и безопасность масла из микроводорослей, и все ученые пришли к одному и тому же выводу: масло из различных видов водорослей, например, рода Schizochytrium, хорошо усваивается, обеспечивает чистую и биодоступную форму ЭПК/ДГК и не оказывает негативного воздействия [10, 11, 12]. Как и рыбий жир, масло из микроводорослей выпускается в виде капсул или во флаконах. Для лучшего усвоения ЭПК и ДГК из капсул с маслом микроводорослей (так же как и из капсул с рыбьим жиром) рекомендуется принимать их вместе с дополнительным источником жира. Это может быть горсть орехов или целый прием пищи с достаточным количеством жиров. На рис. 7 данная рекомендация представлена наглядно: при добавлении еще одного источника жира усвоение жирных кислот омега-3 увеличивается более чем в десять раз [13].
РИС. 7: БИОДОСТУПНОСТЬ ДОБАВОК ОМЕГА-3 С РАЗЛИЧНЫМ СОДЕРЖАНИЕМ ЖИРА

Исследования показывают, что длинноцепочечные жирные кислоты омега-3, содержащиеся в рыбе [14, 15], и короткоцепочечные жирные кислоты омега-3 из молотых семян льна [16] достаточно устойчивы к нагреванию. Однако льняное и конопляное масло, а также масло семян чиа и грецкого ореха следует использовать только для приготовления холодных блюд, поскольку они значительно менее устойчивы к высоким температурам [17]. Поэтому если вы хотите использовать такие масла для придания аромата блюдам, то следует добавлять их только в конце приготовления, уже выключив плиту. Кроме того, их можно использовать для приготовления вкусных холодных соусов и заправок.
Роль длинноцепочечных жирных кислот омега-3 в защите сердца и мозга
Здоровые диеты, такие как средиземноморская, которая эффективно способствует профилактике сердечно-сосудистых заболеваний [18], включают рыбу в свой рацион. Исследования GISSI (Итальянская группа по изучению выживаемости после инфаркта миокарда) также показали снижение смертности от сердечно-сосудистых заболеваний при ежедневном приеме ЭПК/ДГК из рыбьего жира в количествах, эквивалентных потреблению около 100 г высокожирной холодноводной рыбы [19]. В результатах DART (Исследование влияния диеты на повторный инфаркт) также сообщалось, что смертность от инфарктов была ниже в группе пациентов, употребляющих в пищу рыбу, по сравнению с контрольной группой [20]. Однако следует подчеркнуть, что, несмотря на то, что в группе пациентов, употреблявших рыбу, наблюдалось меньше летальных исходов в результате инфаркта, общее количество инфарктов в этих двух группах было идентичным. Это контрастирует с результатами исследования Lyon Diet Heart Study, когда с помощью жирных кислот омега-3 в составе средиземноморской диеты удалось снизить не только частоту смертельных инфарктов, но и общую частоту инфарктов (смертельных и несмертельных вместе взятых) [21]. После более чем двух лет наблюдения в интервенционной группе испытуемых, придерживающихся средиземноморской диеты с жирными кислотами омега-3, инфаркты с летальным исходом случались в пять раз реже по сравнению с контрольной группой. Аналогичным образом, несмертельные инфаркты наблюдались в три раза реже, чем в контрольной группе.
Интересно, что в рамках исследования контрольная и интервенционная группы потребляли практически одинаковое количество рыбы. Существенные различия наблюдались лишь в потреблении большего количества хлеба, фруктов и маргарина на основе рапсового масла, богатого омега-3, в интервенционной группе испытуемых и в потреблении меньшего количества масла, сливок, субпродуктов, мяса и мясных полуфабрикатов, таких как колбасы и бекон, по сравнению с контрольной группой. Иными словами: в этом исследовании источником жирных кислот омега-3 была не рыба, а преимущественно растительные продукты. Тем не менее они оказали определенное влияние на здоровье испытуемых, и поэтому довольно спорным остается вопрос, в какой степени длинноцепочечные жирные кислоты омега-3 из продуктов животного происхождения оказывают дополнительный положительный эффект на здоровье в сочетании с оптимальным количеством короткоцепочечных жирных кислот омега-3 из растительных источников. В Лионском исследовании также подчеркивается, что ценность средиземноморской диеты заключается прежде всего во взаимодействии всех ее полезных компонентов, и поэтому невозможно выделить какой-то один продукт рациона, например, рыбу, как единственный полезный для здоровья [22].
Основой средиземноморской диеты является употребление цельнозерновых и бобовых культур, фруктов, овощей и орехов, а также повышенного количества растительных жиров из оливкового масла и регулярное включение в рацион рыбы [23]. Трудно определить, какой именно компонент диеты защищает организм и в какой именно степени.
Однако данные не доказывают, что большая часть защитного эффекта может быть связана только с потреблением рыбы.
Исследования должны также дать ответ на важный вопрос о том, какие нездоровые продукты были исключены или ограничены в рационе питания из-за потребления конкретного ингредиента. Поскольку в сутки можно съедать только определенное количество пищи, увеличение потребления одного продукта обычно происходит за счет уменьшения другого. Если рыба заменяет в меню более вредные продукты, такие как красное и переработанное мясо, то она не только повышает ценность рациона благодаря содержащимся в ней жирным кислотам омега-3, но и снижает объем нездоровой пищи, а значит, и риск заболеваний. Поэтому всегда необходимо анализировать весь рацион, чтобы понять, какие компоненты могут повлиять на достоверность результатов и достаточно ли полно учтены другие переменные. Например, испытуемые, которые едят рыбу, могут иметь более здоровый рацион и вести более здоровый образ жизни по сравнению с мясоедами, что положительно сказывается на здоровье даже и без потребления рыбы. Поэтому важно учитывать совокупность всех факторов.
После публикации в 2012 году результатов масштабного метаанализа 20 рандомизированных контролируемых экспериментов можно задаться вопросом, в какой степени изолированные жирные кислоты омега-3 способствуют профилактике сердечно-сосудистых заболеваний [24]. Этот наиболее полный и актуальный на сегодняшний день анализ ставит под сомнение общепринятое мнение многих врачей и ученых о пользе капсул с рыбьим жиром. Изучив полученные данные, авторы метаанализа не смогли выявить непосредственной связи между приемом капсул с рыбьим жиром, содержащим жирные кислоты омега-3, и снижением общей смертности или смертности от сердечно-сосудистых заболеваний и инсультов.
Однако основанные на фактах рекомендации 2015 года Немецкого общества питания относительно потребления жиров и профилактики связанных с неправильным питанием отдельных заболеваний, например, оценивают первичную профилактику ишемической болезни сердца (ИБС) за счет потребления длинноцепочечных жирных кислот омега-3 как «вероятную» [25]. Способны ли они оказывать положительное профилактическое воздействие на сердечно-сосудистую систему самостоятельно или только в сочетании с другими питательными веществами? Мы надеемся, что получив бо́льшие объемы данных в будущем, можно будет ответить на этот вопрос более конкретно.
Даже если прием длинноцепочечных жирных кислот омега-3 ЭПК и ДГК не приведет к каким-либо значительным улучшениям состояния сердечнососудистой системы, существует еще одна важная область профилактики, где, в частности, ДГК может быть вполне полезной. Это сохранение когнитивных функций в пожилом возрасте. В 2014 году впервые были опубликованы результаты двойного слепого интервенционного плацебо-контролируемого исследования, которое показало, что длинноцепочечные жирные кислоты омега-3 могут оказывать положительный терапевтический эффект на мозговую активность пожилых людей [26]. Поэтому, вероятно, целесообразно добавлять в пищу длинноцепочечные жирные кислоты омега-3 в профилактических целях для сохранения умственных способностей в долгосрочной перспективе.
Оптимальная дозировка жирных кислот омега-3
Обычная дозировка, рекомендуемая Немецким обществом питания, Европейским агентством по безопасности продуктов питания (EFSA), ВОЗ совместно с Продовольственной и сельскохозяйственной организацией ООН (ФАО) [29] и другими профессиональными сообществами, составляет 250 мг ЭПК/ДГК, как правило, в соотношении 1:2. Некоторые диетологические организации в таких странах, как США [30], рекомендуют также дозу в 500 мг[4]. Более высокое содержание ДГК по сравнению с ЭПК объясняется тем, что самостоятельный синтез ЭПК в организме более эффективен, чем синтез ДГК [31], и при необходимости организм даже может трансформировать часть ДГК обратно в ЭПК [32]. Поэтому ДГК является более важной из двух длинноцепочечных жирных кислот и обычно рекомендуется в более высоких дозах, чем ЭПК. Хотя Европейское агентство по безопасности продуктов питания не устанавливает «верхний допустимый уровень потребления» (UL) из-за недостатка данных, в программе подчеркивается, что по имеющейся информации дозы в 1 000 мг не несут риска для здоровья даже при длительном приеме [33]. Большее количество – 2 000-6 000 мг ЭПК/ДГК – приводит к значительному повышению уровня [плохого] холестерина ЛПНП в основном за счет ДГК, однако многие вопросы относительно влияния больших дозировок остаются пока без ответа [34, 35]. Поэтому для профилактики рекомендуется придерживаться обычной дозировки 250–500 мг ЭПК/ДГК, потребляя большее количество только под присмотром специалиста.
Кроме того, в ходе четырехмесячного интервенционного исследования показатели крови веганов значительно улучшились при дозировке в 250 мг ЭПК/ДГК из микроводорослей в соотношении 1:2 [36].
В качестве индикатора содержания в организме омега-3 использовался так называемый «индекс омега-3». Если этот показатель ниже 4 %, то существует повышенный риск развития сердечно-сосудистых заболеваний. Индекс 4–8 % указывает на средний уровень профилактики сердечно-сосудистых заболеваний, а более 8 % считается оптимальной защитой [37].
В начале исследования у всех участвующих в нем веганов этот показатель был ниже 4 %. В течение четырех месяцев при приеме 250 мг ЭПК/ДГК он лишь превысил пороговое значение в 4 %. Однако, поскольку исследования показывают, что оптимальное значение по индексу омега-3 составляет более 8 %, в течение первых 6–8 недель можно временно увеличить дозировку при низких исходных значениях. В этом случае можно быстрее превысить пороговое значение в 8 %. В двойном слепом плацебо-контролируемом исследовании, проведенном в Германии, группе вегетарианцев в течение восьми недель назначалось 940 мг ДГК (без ЭПК), и средний индекс омега-3 испытуемых вырос с 4,8 до 8,4 %, что соответствовало оптимальному диапазону потребления [38].
В совместной публикации ВОЗ и ФАО беременным и кормящим женщинам рекомендуется потреблять не менее 300 мг длинноцепочечных жирных кислот. Причем соотношение ЭПК и ДГК должно составлять 1:2, чтобы обеспечить рекомендуемое минимальное потребление ДГК – 200 мг в сутки [39]. Однако метаанализ, проведенный в 2012 году, ставит под сомнение пользу приема дополнительного количества ДГК беременными или кормящими женщинами для органичного развития будущего ребенка или младенца [40]. Но не так легко применить к веганам результаты исследований, проведенных среди женщин на смешанном питании и с достаточным потреблением ДГК из рыбы и яиц. Как правило, веганы не усваивают заранее сформированную ДГК из своей чисто растительной диеты, если только не добавляют в пищу масло из микроводорослей. Следовательно, у них изначально другие условия приема жирных кислот по сравнению со многими женщинами на смешанном питании. В исследованиях женщины-вегетарианки показали более низкий уровень ДГК в плазме крови [41, 42] и более низкую концентрацию ДГК в грудном молоке [43], поэтому они могут получить больше пользы от приема БАДов с ДГК из микроводорослей по сравнению с людьми, употребляющими рыбу и яйца [44]. В связи с регистрацией фактов задержки речевого развития у младенцев с дефицитом ДГК следует учитывать все возможные обстоятельства и внимательно относиться к потреблению жирных кислот в этот важный период жизни [45].
Взаимодействие жирных кислот омега-3 и омега-6
Хотя вся глава посвящена в основном жирным кислотам омега-3, они тесно связаны с жирными кислотами омега-6, которые относятся ко второй группе незаменимых или полузаменимых жирных кислот. По этой причине мы их также кратко рассмотрим.
Впервые о существовании незаменимых жирных кислот стало известно из двух публикаций 1929 и 1930 годов. В это время супружеская пара Милдред и Джордж Бурр опубликовала две новаторские статьи о незаменимых жирных кислотах [46, 47], где они впервые предположили, что пищевой жир – это не просто источник калорий и что среди жирных кислот есть жизненно необходимые организму, но не синтезируемые самостоятельно [48]. По этой причине в настоящее время в диетологии признаются две незаменимые жирные кислоты: омега-3, или альфа-линоленовая кислота (АЛК), и омега-6, или линолевая кислота (ЛК) [49].
Обе жирные кислоты должны поступать в организм в достаточном количестве, чтобы обеспечить долгосрочную профилактику. Симптомы дефицита незаменимых жирных кислот разнообразны и варьируются от сильной жажды, частого мочеиспускания, сухости кожи и волос, перхоти и ломкости ногтей до головных болей и болей в желудке [50].
При соответствующих условиях организм может самостоятельно вырабатывать полузаменимые длинноцепочечные жирные кислоты омега-3 – эйкозапентаеновую (ЭПК) и докозагексаеновую (ДГК) – из незаменимой альфа-линоленовой кислоты (АЛК). Кроме того, из незаменимой линолевой кислоты может образовываться длинноцепочечная жирная кислота омега-6, или арахидоновая кислота (АК), которая встречается только в продуктах животного, а не растительного происхождения [51]. Дефицит в организме длинноцепочечных жирных кислот омега-3 ЭПК и ДГК связан с увеличением частоты неврологических заболеваний, таких как депрессия, шизофрения, болезнь Альцгеймера и СДВГ [52]. Кроме того, исследования показывают, что эти жирные кислоты могут быть полезны для вторичной профилактики гипертонии, сердечно-сосудистых заболеваний, диабета 2-го типа, ревматоидного артрита, болезни Крона, язвенного колита и заболеваний почек. Они также могут служить средством для укрепления иммунной системы [53].
Поэтому потребление большого количества длинноцепочечных жирных кислот омега-3 ассоциируется с положительным для здоровья противовоспалительным и сосудорасширяющим эффектом, в то время как повышенное потребление АК оказывает противоположное действие, вызывая воспаления и сужая сосуды [54]. Жирные кислоты омега-3 и омега-6 взаимно влияют друг на друга и могут рассматриваться как антагонисты. По этой причине, особенно в ранних публикациях, большое внимание всегда уделялось взаимосвязи жирных кислот омега-3 и омега-6, хотя результаты более поздних исследований указывают на необходимость дифференцированного подхода к изучению этих жирных кислот [55]. Вероятно, следует рассматривать не общее потребление и взаимное соотношение всех жирных кислот омега-3 и омега-6 в целом, а лишь соотношение и общее потребление отдельных жирных кислот из этих двух групп [56].
На рис. 8 в упрощенном виде показан синтез организмом длинноцепочечных полиненасыщенных жирных кислот. Для максимальной простоты некоторые промежуточные этапы процесса не представлены. Как видно из рисунка, повышенное потребление ЛК ингибирует превращение АЛК в ЭПК и ДГК. И наоборот, повышенное потребление АЛК ингибирует превращение ЛК в АК. Это связано с тем, что обе жирные кислоты (ЛК и АЛК) конкурируют за одни и те же ферментные системы для превращения в соответствующие длинноцепочечные жирные кислоты [58]. Эти ферментные системы ограничены в своих возможностях, поэтому высокое потребление одной из двух жирных кислот приводит к ингибированию превращения другой. Этот процесс также является причиной того, что Общества питания в Германии, Австрии и Швейцарии считают оптимальным определенное соотношение этих двух жирных кислот. Согласно их рекомендациям, соотношение ЛК и АЛК не должно превышать 5:1 [59]. Таким образом, на каждый 1 г АЛК в рационе должно содержаться не более 5 г ЛК. Такое соотношение означает, что снижение количества ЛК приводит к образованию меньшего количества АК, источника воспалений и сужения сосудов. При этом образование полезных для здоровья жирных кислот ЭПК и ДГК не снижается [60].
РИС. 8: КОНКУРЕНЦИЯ МЕЖДУ ЖИРНЫМИ КИСЛОТАМИ ОМЕГА-3 И ОМЕГА-6 В ФЕРМЕНТНОЙ СИСТЕМЕ [57]

Жирные кислоты омега-3 и омега-6 конкурируют за одни и те же ферменты, способные их разложить. Чтобы иметь возможность производить более полезные для здоровья эйкозапентоеновую и докозагексаеновую кислоты из альфа-линоленовой кислоты, потребление линолеивой должно быть низким.
По оценкам ученых, в процессе эволюции соотношение омега-6 и омега-3 в рационе человека составляло примерно 1:1 [61]. Однако в настоящее время в связи с изменением пищевого поведения соотношение в среднестатистическом западном рационе составляет 2:1 и выше.
Это может быть одной из причин развития воспалительных процессов в организме и связанных с ними хронических дегенеративных заболеваний [62]. В веганской диете такое соотношение жирных кислот, вероятно, имеет большее значение, чем в обычной смешанной диете, поскольку в растительной диете провоспалительная АК вообще не поступает из продуктов животного происхождения, а противовоспалительные ЭПК и ДГК обычно поступают в небольших количествах или вовсе не попадают без масла из микроводорослей. При таком сценарии АК в организме образуется за счет перехода из ЛК. ЭПК и ДГК образуются исключительно из АЛК. В этом случае соотношение ЛК и АЛК может существенно влиять на образование длинноцепочечных жирных кислот [63].
В условиях смешанного питания со средним количеством продуктов животного происхождения это соотношение, по-видимому, не так важно, поскольку уже готовая АК поступает в организм с высокожирными мясными и колбасными изделиями, а также с субпродуктами и яичным желтком. Поэтому гораздо более низкий уровень самостоятельного синтеза в организме АК из ЛК не так страшен [64, 65]. Если веган предпочитает потреблять уже готовые ЭПК и ДГК с маслом из микроводорослей, то это соотношение уже не будет иметь для него такого значения, как при веганской диете без масла из микроводорослей, поскольку в этом случае веган также будет получать достаточное количество предварительно сформированных длинноцепочечных жирных кислот омега-3 с противовоспалительными свойствами.
Однако в процессе обсуждения оптимального соотношения жирных кислот омега-3 и омега-6 недостаточно учитывается один важный фактор. Часто соотношение жирных кислот омега-3 и омега-6 слишком обобщают, не делая различий между отдельными классами жирных кислот. Такое обобщение жирных кислот омега-3 (АЛК, ЭПК, ДГК) и омега-6 (ЛК и АК) в некоторых работах часто ошибочно приводит к тому, что вместо оценки соотношения отдельных жирных кислот этих двух классов больше внимания уделяется общему соотношению всех жирных кислот обоих классов. Однако, несмотря на принадлежность к группе, они все абсолютно разные [66]. Различия в действии жирных кислот также является причиной того, что некоторые профессиональные организации и эксперты в настоящее время не так строго учитывают соотношение жирных кислот омега-6 и омега-3. Поддержание соотношения ЛК и АЛК, особенно при дефиците длинноцепочечных жирных кислот омега-3 и омега-6, по-прежнему важно для веганской диеты, в частности, для оптимизации синтеза ЭПК и ДГК [67].

Чтобы перейти от теории к практике, в табл. 3 приведены рекомендации по минимальному потреблению ЛК и АЛК, а также ЭПК и ДГК, а затем конкретные рекомендации по их суточному потреблению в рамках веганской диеты.
Если в период грудного вскармливания мать в достаточной степени обеспечена всеми незаменимыми жирными кислотами, а также ДГК за счет добавления масла из микроводорослей, ребенок также получает достаточно ДГК с грудным молоком [68]. Если ребенок не находится на грудном вскармливании, ему требуется отдельный источник ДГК. Чтобы обеспечить поступление ДГК в организм, ее часто добавляют в детские смеси на растительной основе. Однако если продукт не содержит ДГК, рекомендуется добавлять ее в пищу в количестве 10–12 мг на 1 кг массы тела.
Значения процентного содержания ЛК и АЛК, приведенные в табл. 3, считаются минимальными по отношению к общему количеству калорий и могут быть увеличены при необходимости. Они также действительны только при условии, что ЭПК и ДГК получены из микроводорослей, содержащихся в рационе. Поэтому Институт медицины (IOM) определил так называемый «допустимый диапазон распределения макроэлементов» (AMDR) для обеих жирных кислот относительно нормы их потребления. Этот диапазон составляет 5-10 % от общего количества калорий для ЛК и 0,6–1,2 % от общего количества калорий для АЛК [69]. Если предположить, что 40-летняя женщина весом 60 кг со средней потребностью в 1900 ккал в сутки работает в офисе, то для нее минимальное потребление незаменимых жирных кислот составляет около 5 г ЛК и около 1 г АЛК [70]. Однако в рамках общего количества калорий она может потреблять от 10 до 20 г ЛК и от 1 до 2,5 г АЛК, если получает ЭПК и ДГК отдельно с маслом из микроводорослей [71]. В публикации на тему оптимизации потребления омега-3 при отсутствии отдельного источника ЭПК/ДГК в виде масла из микроводорослей для веганской диеты рекомендуется компенсировать эту нехватку как минимум двойным количеством АЛК по сравнению с официальными рекомендациями [72]. Таким образом, можно получить минимальное достаточное количество субстрата для эндогенного образования ЭПК и ДГК. Увеличивая количество АЛК при сохранении нормы ЛК, можно также достичь более благоприятного соотношения ЛА и АЛК, как минимум 2:1. В этом случае желательно, чтобы доля АЛК составляла около 1–2 % от общего количества потребляемых калорий. Например, для женщины с нормой энергозатрат в 1900 ккал рекомендуемая норма потребления АЛК составит около 2–4 г в день. Необходимое количество АЛК зависит от потребления ЛК. Большее количество ЛК приводит к увеличению доли АЛК. Это необходимо для сохранения рекомендованного соотношения примерно 2:1. Таким образом, если человек решает потреблять 4 г АЛК, ему потребуется около 8 г ЛК в сутки.
На рис. 9 и рис. 10 представлены данные о содержании жирных кислот омега-3 и омега-6 в различных продуктах питания. На рисунках показано общее количество и соотношение жирных кислот омега-3 и омега-6 в отдельных растительных маслах и в полноценных продуктах с высоким содержанием жира. Это позволяет понять, какие продукты следует употреблять чаще в определенных условиях, а какие сократить.
Чтобы обеспечить минимальную норму ЛК в 5 г, женщина может ежедневно съедать, например, 18 г семян подсолнечника или 38 г миндаля, что уже на 100 % покрывает минимальную норму [75]. 8 г (2 ч. л.) подсолнечного масла также уже обеспечили бы минимальную норму потребления ЛК.
РИС. 9: СООТНОШЕНИЕ ЖИРНЫХ КИСЛОТ ОМЕГА-3 И ОМЕГА-6 В РАСТИТЕЛЬНЫХ МАСЛАХ [73]

РИС. 10: СООТНОШЕНИЕ ЖИРНЫХ КИСЛОТ ОМЕГА-3 И ОМЕГА-6 В ОРЕХАХ И СЕМЕНАХ [73]

Однако благодаря гибкости рекомендаций и широкому диапазону количества потребляемых жирных кислот омега-6 и омега-3 женщина может съедать в два раза больше продуктов и все равно не превышать норму.
Для удовлетворения минимальной потребности в АЛК в количестве 1 г достаточно всего 2 г льняного масла (½ ч. л.), 6 г измельченных льняных семян или 13 г грецких орехов. Из-за довольно высокого содержания ЛК в грецком орехе в 13 г содержится 4,5 г ЛК, чего достаточно для удовлетворения почти 100 % ее минимальной суточной нормы для человека. Однако если человек не знает о более богатых источниках омега-3 в своем рационе и не употребляет грецкие орехи, семена льна, чиа и конопли и их масла, он вряд ли сможет адекватно покрыть свои потребности в омега-3 в рамках калорийного баланса и с учетом максимальных ограничений по омега-6 за счет других орехов и семян.
Чтобы проиллюстрировать основные различия в составе жирных кислот, приведем несколько примеров.
Для получения 1 г незаменимой АЛК, как уже говорилось, достаточно около 6 г дробленых семян льна. Однако для получения того же 1 г АЛК потребуется почти 160 г семян кунжута или более 1 кг семян подсолнечника.
Поэтому различные семена не являются взаимозаменяемыми. То же самое относится и к орехам. Если всего 13 г грецких орехов обеспечивают 1 г АЛК, то для получения того же 1 г АЛК человеку требуется чуть менее 190 г арахиса или чуть более 380 г миндаля. Семена кунжута, подсолнечника, арахис и миндаль по-прежнему являются полезными продуктами, которые можно и нужно иметь в своем ежедневном рационе питания. Однако они не могут заменить такие богатые источники омега-3, как грецкие орехи, семена льна, чиа или конопли.
Однако следует знать не только о лучших источниках омега-3, но и о тех продуктах, которые содержат непропорционально большое количество ЛК и поэтому могут нарушить желаемое соотношение ЛК и AЛК. Необходимо уменьшить употребление таких продуктов. В первую очередь это касается масел с особенно высокой концентрацией ЛК, таких как сафлоровое, масло из виноградных косточек, тыквенных семечек, маковых семян, зародышей кукурузы и, прежде всего, подсолнечное масло. Последнее, в частности, содержится во многих продуктах питания, и лишь некоторые растительные спреды, растительные молочные смеси, готовые соусы и другие полуфабрикаты не содержат подсолнечного масла. Следует также значительно сократить количество полуфабрикатов, поскольку они часто содержат большое количество соли, жиров, муки, сахара, а также являются высококалорийными и имеют низкую энергетическую ценность.
В домашних условиях простая замена подсолнечного и кукурузного масла на рапсовое или оливковое может значительно снизить общее потребление жирных кислот омега-6.
Однако это не означает, что следует отказаться от полноценных продуктов с высоким содержанием омега-6, таких как подсолнечные или тыквенные семечки, ведь в них содержится много белка, клетчатки и других полезных веществ, а содержание омега-6 не так велико, как в обычном подсолнечном масле. Несмотря на то что спектр жирных кислот в семенах подсолнечника или тыквы аналогичен их содержанию в масле, эти семена содержат целый ряд дополнительных ценных веществ. Более того, и те и другие – не только вкусные, но и очень недорогие и легкодоступные источники питательных веществ по сравнению с орехами, которые можно продолжать включать в свой рацион. Однако употребление семян подсолнечника или тыквы не должно идти в ущерб, например, семенам льна или конопли, поскольку их ежедневное потребление является важным компонентом сбалансированной диеты с оптимальным содержанием омега-3.
Кроме того, несмотря на растущую озабоченность чрезмерным потреблением омега-6, не следует забывать о том, что ЛК также является незаменимой и ее необходимо принимать. Если в состав веганской диеты боятся включать омега-6, то это ведет к отказу от употребления ЛК и пагубно влияет на организм.
Хотя реальный дефицит ЛК маловероятен, он, несомненно, возможен. В частности, веганы, придерживающиеся низкокалорийной диеты с высоким содержанием углеводов и низким содержанием жиров, должны строго следить за приемом незаменимых жирных кислот несмотря на ограниченное количество жиров. В такой рацион для поддержания здоровья необходимо обязательно включать такие полезные источники жиров, как орехи и семена [76, 77, 78]. Они не только очень богаты питательными веществами, но и гарантируют поступление минимального количества ЛК и АЛК. Если в рамках низкокалорийной диеты отказаться от орехов, семян и масел, то вполне может возникнуть дефицит обеих незаменимых жирных кислот.
Хотя обычные растительные продукты с низким содержанием жиров, такие как капуста, шпинат и киноа, сами по себе чрезвычайно полезны, они вряд ли могут компенсировать недостаток орехов и семян в растительной диете. Чтобы получить минимальное ежедневное количество АЛК в 1 г (1000 мг), женщине весом 60 кг придется съесть около 280 г капусты, 750 г шпината или 1,5 кг вареного киноа [79]. Даже продукты с довольно высоким содержанием жиров, такие как оливки или авокадо, содержат лишь умеренное количество ЛК и очень небольшое количество АЛК, поскольку из жирных кислот в них, как правило, присутствуют мононенасыщенные. Это определенно полезно для здоровья и как минимум не приводит к избытку ЛК в рационе. Однако, в этом случае человек не получает достаточного количества АЛК. Чтобы удовлетворить суточную минимальную потребность в АЛК за счет оливок или авокадо, придется съесть почти 770 г оливок или около 630 г мякоти авокадо. Кроме того, как уже упоминалось, 1 г АЛК представляет собой минимальную норму, поэтому веган не сможет удовлетворить эту потребномть при диете, практически не содержащей орехов, семян и масел.
Получить минимальное количество ЛК без масел, орехов, семян или других продуктов с высоким содержанием жиров возможно, только если используются зерна с более высоким содержанием жира, такие как овес, псевдозерновые, например киноа или амарант, и бобовые с высоким содержанием жира, например соя.
Однако здоровым людям присутствие орехов, семян или других полезных продуктов с высоким содержанием жиров в ежедневном рационе не нанесет вреда, как показано в главе, посвященной орехам и семенам. Напротив, можно говорить только о пользе для здоровья. Поэтому ежедневное употребление орехов и семян рекомендуется практически каждому человеку в любом возрасте.
Оптимальный синтез длинноцепочечных жирных кислот омега-3 в организме
Большинство организаций, занимающихся вопросами питания и здравоохранения, согласны с тем, что отдельный прием длинноцепочечных омега-3 жирных кислот ЭПК и ДГК в дополнение к адекватному потреблению АЛК полезно для здоровья, и рекомендованная суточная нома составляет 250–500 мг. Хотя большинство людей получают эти кислоты из продуктов животного происхождения, их также можно получать благодаря маслу из микроводорослей. Тем не менее тот факт, что ЭПК и ДГК содержатся в обычных растительных продуктах в меньших количествах, является поводом для критики веганской диеты в рамках некоторых обсуждений. В настоящее время в большинстве супермаркетов, а также во многих магазинах органических продуктов и здорового питания действительно нет продуктов, обогащенных маслом из микроводорослей, а сами масла все еще относительно дорогие из-за ограниченных объемов производства.
Однако в ближайшие годы ситуация может измениться, и масло из микроводорослей будет все чаще появляться на полках супермаркетов, магазинов органических продуктов и магазинов здорового питания как чистый, экологичный и эффективный источник омега-3.
Помимо поступления из продуктов, организм, по-видимому, способен вырабатывать достаточное количество ЭПК, а при определенных условиях иногда и ДГК за счет потребления оптимального количества одной только АЛК.
Однако традиционная западная диета и образ жизни препятствуют выработке длинноцепочечных жирных кислот омега-3, в результате чего во многих случаях способности организма к собственному синтезу недостаточны и значительно ограничены. Кроме того, в ходе ряда исследований результаты показали лишь ограниченный синтез ЭПК, а иногда и едва заметный синтез ДГК. Поэтому рекомендация о приеме ЭПК/ДГК из продуктов питания остается актуальной. Однако важно понимать, что при благоприятных условиях можно было бы получать минимальную дозу кислот и без микроводорослей за счет самостоятельного синтеза из АЛК. Тем не менее изменение пищевого поведения за последние несколько столетий и ограниченный ассортимент продуктов, представленный в супермаркетах и рассчитанный на смешанное питание, во многих случаях делают это затруднительным или невозможным. Мы подробно расскажем о факторах, положительно и отрицательно влияющих на самостоятельный синтез. Прежде всего, стоит выяснить, насколько высока реальная скорость превращения АЛК в ЭПК и ДГК в рамках западной смешанной или веганской диеты.
Количество ЭПК и ДГК, производимое организмом из АЛК, у половозрелых женщин обычно выше, чем у мужчин того же возраста. Точные значения для мужчин и женщин в постменопаузе варьируются в разных источниках, но в среднем коэффициент трансформации АЛК в ЭПК составляет 5–8 %. Также организм может вырабатывать ДГК из ЭПК, при этом в ДГК преобразуется около 0,1–0,5 % от исходного количества АЛК [80, 81, 82]. Хотя одни исследования указывают на более высокую степень перехода АЛК в ДГК – 2–4 %, в других также отмечается, что степень преобразования в ЭПК составляет менее 1 %, а в случае с ДГК часто вообще не поддается измерению [83, 84]. Таким образом, данные в отношении самосинтеза далеко не однозначны и, вероятно, обусловлены индивидуальными особенностями человека.
Самосинтез длинноцепочечных жирных кислот омега-3 у половозрелых женщин протекает более благоприятно. Исследование показало, что они способны преобразовать в среднем 21 % АЛК в ЭПК и до 9 % в ДГК [85, 86]. По мнению ученых, более высокие показатели у половозрелых женщин могут быть связаны с тем, что в случае беременности их метаболизм должен обеспечивать хотя бы минимальный процент ЭПК и ДГК для развития плода, а затем и младенца, даже при недостаточном потреблении ЭПК/ДГК с пищей. В другом исследовании сравнивалась способность организма к преобразованию жирных кислот у веганов, вегетарианцев и людей на смешанной диете. В результате было установлено, что вегетарианцы и веганы более способны к конверсии по сравнению с людьми, придерживающимися смешанной диеты [87]. Это говорит о некотором увеличении скорости превращения без приема уже готовых длинноцепочечных жирных кислот омега-3 с пищей или о снижении в случае их постоянного потребления с продуктами питания. Данную гипотезу подтверждает и 90-дневное исследование. В нем две группы испытуемых получали высокие (6500 мг/сут) или низкие (‹1000 мг/сут) дозы ДГК, и через 90 дней образование длинноцепочечных жирных кислот омега-3 и омега-6 замедлилось более чем на 70 % после приема ЛК и АЛК [88].
Даже если мы считаем, что при аутосинтезе АЛК в ЭПК происходит переход около 5 %, то при отсутствии в рационе продуктов с ЭПК и ДГК всего 30 г дробленых семян льна или 10 г льняного масла может быть достаточно организму для выработки необходимого количества ЭПК, чтобы удовлетворить суточную потребность в более чем 250 мг.
Это наглядно показывает, насколько легко получить суточную норму ЭПК, если получать необходимое количество АЛК из растительных источников. Увеличение содержания ЭПК после приема семян льна также было определено экспериментально. В одном исследовании 110 респондентов-гипертоников в течение полугода ежедневно съедали по 30 г дробленых семян льна, что теоретически должно покрыть потребность в ЭПК даже при обычном уровне преобразования жирных кислот. Однако было неясно, достаточно ли этого количества для синтеза ДГК. Фактически в конце исследования участники показали рост значений для ЭПК более чем на четверть. Однако уровень ДГК остался прежним [89]. Тем не менее не наблюдалось и снижения уровня ЛК. Возможно, полгода – это слишком короткий срок для проверки влияния определенных продуктов на концентрацию ДГК в плазме, и, как будет показано далее, гипертония также может являться еще одним ограничивающим фактором самосинтеза длинноцепочечных жирных кислот [90]. Следовательно, это и многие другие исследования скорости преобразования жирных кислот не отражают истинные возможности организма и поэтому лишь в ограниченной степени служат источником информации о возможности образования жирных кислот в контексте полноценного, хорошо сбалансированного рациона веганов.
Поскольку в настоящее время не исследуются способности организма к собственному синтезу жирных кислот на примере молодых, абсолютно здоровых веганов с оптимальным, полноценным растительным питанием и здоровым образом жизни, поступление ЭПК и ДГК с продуктами питания является скорее мерой предосторожности из-за недостатка данных, чем абсолютной необходимостью. Особенно это рекомендуется группам с потребностями в повышенном количестве жирных кислот, таких как беременные женщины, кормящие матери и дети.
Чтобы проверить возможность повысить уровень преобразования АЛК в ЭПК и ДГК, можно изменить веганский рацион, подняв индекс омега-3 выше 8 %. Такая корректировка веганского питания и образа жизни могут привести к оптимизации синтеза. Помимо диеты, образа жизни и ряда неконтролируемых факторов, таких как генетика, пол и возраст, существует также ряд заболеваний, оказывающих влияние на процесс синтеза. Ниже мы остановимся на них более подробно.
РИС. 11: ФАКТОРЫ, ВЛИЯЮЩИЕ НА ЭФФЕКТИВНОСТЬ ПРЕОБРАЗОВАНИЯ ЖИРНЫХ КИСЛОТ ОМЕГА-3

Предположительно, люди, ведущие здоровый образ жизни, гораздо лучше усваивают ЭПК и ДГК. Хотя существует несколько факторов, влияющих на коэффициент преобразования. На них вы не можете существенно повлиять, но они полностью зависят от ваших особенностей. Так, коэффициент преобразования снижается в течение жизни, то есть у молодых людей он, как правило, выше по сравнению с пожилыми [91]. Помимо предполагаемых генетических особенностей, у женщин этот показатель выше, чем у мужчин аналогичного возраста, по крайней мере, в период фертильности [92].
Помимо этих факторов, существует ряд заболеваний, которые могут влиять на метаболизм незаменимых жирных кислот ЛК и АЛК и тем самым ограничивать способность организма к синтезу собственных длинноцепочечных жирных кислот омега-3. Однако с помощью полноценного питания и здорового образа жизни можно вести профилактику этих заболеваний, а лечение позволит значительно улучшить состояние организма.
Такие заболевания, как ожирение, диабет, метаболический синдром, атеросклероз, гипертония, ишемическая болезнь сердца, болезнь Альцгеймера, рак и другие, негативно сказываются на метаболизме незаменимых жирных кислот [93].
Кроме вышеуказанных факторов, все остальные являются переменными, и вы всегда можете изменить их себе во благо. Отказ от табака, алкоголя, чрезмерного употребления кофеина, низкий уровень стресса положительно влияют на выработку ЭПК и ДГК [94, 95]. Существует также целый ряд других факторов, связанных с питанием.
В первую очередь необходимо обеспечить поступление в организм АЛК, поскольку без основного субстрата для образования ЭПК и ДГК они не могут быть синтезированы даже в самых оптимальных условиях. Этого можно легко добиться, увеличив потребление продуктов, содержащих омега-3. Например, можно взять за правило включать в свой ежедневный рацион определенные источники омега-3, такие как семена льна, конопли, чиа или грецкие орехи. Как уже упоминалось, следует также сократить потребление антагониста омега-3 – ЛК, поскольку избыток ЛК может сократить образование ЭПК и ДГК из АЛК на 40 % [96].
Эти результаты были подтверждены и в другом исследовании, в котором анализировалась скорость превращения АЛК в ЭПК и ЛК в АК. Было показано, что по сравнению с соотношением 10:1 ЛК и АЛК синтез ЭПК значительно возрастает при соотношении 4:1. С другой стороны, при таком соотношении снижается количество синтезированной провоспалительной AК [97]. Однако, вероятнее всего, максимальная скорость преобразования жирных кислот омега-3 достигается только при соотношении ЛК и АЛК 1:1 [98, 99]. В рамках другого исследования вполне оптимальное соотношение 4:1 было скорректировано до 1:1, что позволило увеличить скорость превращения АЛК в ЭПК и ДГК у пожилых японских мужчин и женщин в течение десятимесячного периода исследования. Рост скорости синтеза ЭПК составил более 40 %, ДГК – более 20 % [100].
Для оптимизации способности организма к синтезу необходимо также обеспечить базовую норму всех важных питательных веществ. Только при рекомендованном потреблении калорий, белков, витаминов и минералов метаболические процессы, связанные с синтезом длинноцепочечных жирных кислот, могут протекать максимально эффективно [101]. Как показывает практика, дефицит незаменимых аминокислот, витаминов, таких как С, B6, B7, B3, а также минералов, таких как цинк, магний и медь, может снижать активность ферментов, необходимых для образования ЭПК и ДГК [102, 103]. Кроме того, потребление трансжиров, насыщенных жирных кислот, холестерина и слишком калорийная диета также могут тормозить работу ферментов [104].
Высококалорийная диета также может оказывать вредное воздействие на процесс обмена веществ, это же относится и к рациону с пониженным количеством калорий, поэтому всегда важно обеспечить оптимальный баланс калорий [105]. Поскольку веганская диета не содержит холестерина и, как правило, включает лишь небольшое количество насыщенных жирных кислот, эти два вредных фактора в питании на основе растительных продуктов незначительны. Количество трансжиров в рационе веганов в первую очередь зависит от присутствия промышленно обработанных продуктов питания, производство которых может приводить к образованию трансжиров. По данным Федерального института оценки рисков (BfR), в Германии повышенное количество трансжирных кислот может содержаться в хлебобулочных изделиях, продуктах, обжаренных во фритюре, некоторых видах маргарина, а также в различных кондитерских изделиях и готовых блюдах [106]. Несмотря на то что в последние годы производители снизили содержание трансжиров в продуктах питания [107], польза для здоровья при отказе от таких продуктов не ограничивается только отсутствием трансжирных кислот в организме, поэтому следует стремиться к исключению таких блюд из своего рациона.
Кроме того, в продуктах питания помимо витаминов и минералов есть вещества, которые могут повышать скорость превращения АЛК в ЭПК и ДГК. В этой области еще предстоит провести большое количество исследований, но ученые уже обнаружили как минимум в одной специи потенциальное вещество, улучшающее собственный синтез организма ЭПК и ДГК. Речь идет о вторичном растительном веществе куркумине, содержащемся в куркуме. Ученые предполагают, что куркумин может повышать активность некоторых ключевых ферментов, участвующих в процессе превращения АЛК в ЭПК и ДГК, что, в свою очередь, приводит к улучшению синтеза [108]. Поскольку куркума и так очень богата питательными веществами, такое открытие становится еще одним стимулом для ежедневного употребления этой специи в виде свежего корня или порошка.
Важно отметить, что куркуму всегда следует использовать в сочетании с черным перцем, поскольку пиперин, одно из биологически активных веществ черного перца, усиливает действие куркумина, содержащегося в куркуме [109].
Кроме того, эффективность самостоятельного синтеза ДГК, по-видимому, зависит от поступления в организм уже сформированной ДГК из продуктов питания [110]. Об этом уже говорилось выше в рамках гипотезы, согласно которой у вегетарианцев и веганов показатели превращения жирных кислот могут быть выше, чем у тех, кто придерживается смешанного питания и включает рыбу в рацион [111]. Это объясняется ингибирующим влиянием ДГК из пищи на самосинтез ДГК в организме [112]. Таким образом, организм способен самостоятельно вырабатывать меньшее количество ДГК, если она в достаточном количестве поступает с пищей. И, наоборот, эффективность самосинтеза возрастает при недостатке длинноцепочечных жирных кислот омега-3. Конечно, обязательным условием всегда является наличие исходного субстрата в виде АЛК.
Во многих исследованиях у веганов наблюдалось значительное снижение концентрации длинноцепочечных жирных кислот ЭПК и ДГК в плазме крови по сравнению с теми, кто придерживался смешанной диеты [113, 114, 115]. Этот факт свидетельствует о том, что веганская диета, не нацеленная на оптимизацию самосинтеза и высокое содержание АЛК, априори не сможет помочь в этом отношении. Интересно, что в другом исследовании, использовавшем данные EPIC-Norfolk, было показано, что концентрация ЭПК и ДГК в плазме крови веганов была несущественно ниже концентрации в крови участников со смешанной диетой, употреблявших рыбу [116]. И это несмотря на отсутствие диетического питания. Однако доля веганов в исследовании была очень мала, и до настоящего времени результаты других экспериментов не смогли подтвердить эти значения. Тем не менее это, безусловно, согласуется с мнением, что в оптимальных условиях организм способен синтезировать достаточно жирных кислот при соответствующем потреблении АЛК.
Неутешительные результаты интервенционных исследований по введению более высоких доз АЛК без заметного повышения уровня ДГА также, как правило, были получены в ходе очень коротких экспериментов, продолжительностью 2–6 недель [117, 118, 119]. Некоторые ученые критикуют тот факт, что достоверные данные об истинной способности организма к преобразованию жирных кислот в условиях веганской диеты с достаточным потреблением АЛК могут быть получены только на основании исследований с большей продолжительностью и длительным пониженным потреблением ЛК [120, 121]. Данное предположение подтверждается и ранее упомянутым исследованием с участием пожилых японских мужчин и женщин, в котором оптимальное соотношение ЛК и АЛК равное 1:1, позволило повысить в плазме крови концентрацию не только ЭПК, но и ДГК. Однако для роста потребовалось десять месяцев [122]. Таким образом, если бы это исследование было рассчитано только на две или четыре недели или на шесть недель, то соответствующие результаты не были бы получены. Невозможно ответить на вопрос о том, могла ли концентрация ДГК в плазме крови повыситься гораздо раньше при таком оптимальном соотношении омега-6 и омега-3 у молодых людей, пока не будут опубликованы результаты дальнейших исследований. Тем не менее в целом авторы согласны с тем, что результаты краткосрочных исследований по оценке уровня ДГК при одном только потреблении АЛК не являются убедительными и что для изучения реальных изменений в самосинтезе ДГК эксперименты должны длиться как минимум год.
Выводы к главе
Состояние человеческого организма зависит от поступления незаменимых жирных кислот, поскольку он не способен вырабатывать их самостоятельно. В рамках обычной веганской диеты жизненно необходимая жирная кислота омега-6, или линолевая кислота (ЛК), поступает в достаточном количестве. Проблема может возникнуть только с потреблением жирной кислоты омега-3, или альфа-линоленовой кислоты (АЛК), которой явно не хватает в рационе некоторых веганов. Несмотря на то что роль различных жирных кислот омега-3 в поддержании здоровья сердца и качества умственных способностей еще окончательно не выяснена, разумно было бы обеспечить их потребление в достаточном количестве. Этого можно добиться за счет ежедневного потребления источников омега-3, представленных в настоящей главе, таких как семена льна, конопли или чиа, а также грецкие орехи.
Потребление длинноцепочечных жирных кислот омега-3, эйкозапентаеновой кислоты (ЭПК) и докозагексаеновой кислоты (ДГК) также может иметь решающее значение. Хотя их продуцентом являются микроводоросли, обычно они ассоциируются с употреблением жирной холодноводной рыбы.
Поскольку веганы не едят рыбу, им рекомендуется получать эти две жирные кислоты в виде масла из микроводорослей или обогащенных им продуктов.
Это скорее мера предосторожности, чем абсолютная необходимость, поскольку сбалансированная веганская диета, вероятно, способна в долгосрочной перспективе обеспечить минимальную выработку организмом этих длинноцепочечных жирных кислот из АЛК. Однако, поскольку это может произойти только при определенных условиях и многие не готовы что-то менять в своем рационе или в чем-то себя ограничивать, прием ЭПК и ДГК из растительных источников является более простым и безопасным способом обеспечить достаточный уровень жирных кислот. Это особенно актуально, пока полученных данных недостаточно для обоснованных заявлений о долгосрочной выработке ДГК самим организмом при сбалансированной веганской диете.
При поступлении длинноцепочечных жирных кислот омега-3 с пищей соотношение жирных кислот омега-6 и омега-3 уже не так важно, поэтому к нему можно относиться не так серьезно. Соотношения ЛК и АЛК от 4:1 до 5:1 вполне достаточно для разработки ежедневного рациона. При минимальном присутствии АЛК в количестве 0,5 % от общего количества калорий, в форме ЛК может быть получено до 2,5 % калорий. Это соотношение может быть пропорционально увеличено при повышенном приеме АЛК. Норма ЭПК/ДГК, составляющая 250–500 мг, также является оптимальной для взрослых, согласно рекомендациям различных профессиональных сообществ. Если человек потребляет недостаточно ЭПК и ДГК, то концентрация АЛК должна быть существенно выше и составлять 2–4 % от общего количества калорий, а норма ЛК должна быть максимум вдвое больше количества АЛК в пище. Кроме того, следует также принять во внимание все факторы, упомянутые в главе, для повышения скорости превращения АЛК в ЭПК и ДГК.
Мифы – Реальность
Чтобы получить достаточное количество полезных для здоровья жирных кислот омега-3, необходимо есть рыбу.
Жирные кислоты омега-3 ЭПК и ДГК, содержащиеся в микроводорослях, накапливаются в мясе рыбы, проходя по пищевой цепи. Поэтому можно получать названные жирные кислоты из растений в виде масла микроводорослей, а при определенных условиях организм человека способен и к самостоятельному производству.
Рыба и рыбий жир способствуют эффективной профилактике сердечно-сосудистых заболеваний.
Данные о влиянии рыбы и рыбьего жира на состояние сердечно-сосудистой системы неоднозначны, и многие ученые сомневаются, что именно рыба в значительной степени положительно влияет на здоровье, что наблюдается в рамках средиземноморской диеты. С точки зрения здоровья совершенно неважно, поступают ли длинноцепочечные жирные кислоты из рыбы, микроводорослей или вырабатываются организмом самостоятельно.
Каждый веган обязательно должен пополнять свой рацион ЭПК и ДГК.
Каждому вегану просто необходимо обеспечить себя этими длинноцепочечными жирными кислотами. Проще всего это сделать, принимая непосредственно растительные добавки ЭПК и ДГК из микроводорослей. Однако некоторые исследования показывают, что здоровый человек, особенно женского пола, способен самостоятельно вырабатывать эти жирные кислоты, если последовательно оптимизирует свой веганский рацион в соответствии с представленными рекомендациями. Тем не менее беременным и кормящим женщинам, а также детям обязательно рекомендуется принимать БАДы.
ЭПК и ДГК в масле из микроводорослей хуже усваиваются организмом по сравнению с рыбьим жиром.
Результаты исследований показывают, что масло из микроводорослей усваивается так же хорошо и эффективно, как и рыбий жир. Оно представляет собой экологически чистую и устойчивую альтернативу ЭПК и ДГК из рыбьего жира и поэтому должно стать предпочтительным источником этих жирных кислот для тех, кто придерживается смешанных диет.
Веганы автоматически обеспечены всеми важными жирными кислотами за счет разнообразного питания.
Полезная и разнообразная растительная пища должна быть основным требованием для всех веганов. Такой рацион отвечает большинству потребностей в питании. Однако в каждом рационе должны присутствовать определенные важные питательные вещества, которые необходимо учитывать. Разнообразная веганская диета не гарантирует автоматическое оптимальное потребление жирных кислот. Этого можно добиться исключительно за счет включения в ежедневный рацион богатых источников омега-3, что совсем не сложно.
Глава 3. Витамин В12
Продукты животного происхождения не обладают монополией на отдельные питательные вещества, и все основные нутриенты, содержащиеся в них, могут быть получены и из растений. Однако витамин B12 стал своего рода исключением. Именно поэтому Немецкое общество питания (DGE) справедливо называет витамин B12 наиболее важным питательным веществом в веганской диете [1].
Как показывают исследования, получить B12 из растительной пищи можно, но в современных условиях большинству людей это пока недоступно. Поэтому веганы просто принимают БАДы, содержащие B12.
Это обстоятельство не должно приводить к поспешному отказу от веганской диеты или навешиванию на нее ярлыка ненатуральности. В настоящей главе мы объясним, что прием добавок, содержащих B12, ни в коем случае не является веской причиной для сомнений в выборе растительного питания.
БАД с B12 – это единственная добавка, которую настоятельно рекомендуется принимать всем веганам без исключения независимо от состава рациона. В некоторых ситуациях будут полезны и другие добавки, но без B12 обойтись невозможно, поскольку, за исключением очень немногих видов водорослей, влияние которых на людей еще недостаточно изучено, и некоторых растительных продуктов, ферментированных при правильных условиях, только продукты животного происхождения содержат достаточные для человека количества B12. Крайне низкие концентрации содержатся также в некоторых грибах, но с их помощью очень сложно получить суточную норму [2]. В продуктах животного происхождения, напротив, содержится достаточно много B12. Однако его концентрация и биодоступность из продуктов существенно варьируются.
Веганство – это прекрасная диета с большим количеством плюсов для человека, животных и окружающей среды. Тем не менее эта замечательная концепция питания не должна побуждать нас к ее защите с помощью порой надуманных аргументов.
Даже если проблема с B12 дает основание критиковать веганство в определенных аспектах, мы не должны пытаться во что бы то ни стало найти способы получения B12 естественным путем из растений или других источников, потому что хотим избежать ненатуральных добавок. Ведь если источники еще недостаточно изучены, то это может только навредить здоровью.
При обсуждении натуральности и ненатуральности веганской диеты на основе приема B12 не учитываются два важных момента. Во-первых, следует отметить, что натуральность чего-либо сама по себе не является ни хорошим, ни плохим свойством и поэтому не может служить убедительным основанием для аргументации «за» или «против». Во-вторых, часто забывают о том, как именно образуется B12, а ведь это не классический компонент продуктов животного происхождения, а продукт жизнедеятельности микроорганизмов [3]. Бактерии, способные вырабатывать B12, действительно присутствуют в пищеварительном тракте человека, а также в пищеварительном тракте многих животных. Однако, в отличие от жвачных животных, мы вряд ли сможем обеспечить себя B12, вырабатываемым кишечными бактериями [4]. Раньше, когда гигиена практически отсутствовала, B12 можно было, вероятно, обнаружить во многих местах, например, в грязной питьевой воде и в остатках почвы на продуктах питания. Исследования, проведенные в 1950-х годах на пробах воды из различных водоемов, на образцах корней и почвы, в некоторых случаях показали наличие в них значительного количества B12 [5]. Тем не менее загрязненная вода, почва или другие негигиеничные источники не должны использоваться для получения B12, даже если они могут показаться некоторым людям натуральными.
А как же быть с натуральностью пищевых добавок? Является ли отсутствие натуральности веским аргументом против веганской диеты?
Так называемое «заблуждение о натуральности» заключается во мнении, что все натуральное безупречно и исключительно полезно, а все ненатуральное автоматически плохое [6]. Многое из натурального, например вредоносные вирусы и бактерии, не является чем-то хорошим. Лекарства или противоядия, напротив, менее натуральны, однако во многих случаях чрезвычайно полезны.
Это правда, что в рационе современных веганов не хватает B12. Однако они не единственные, кому не хватает определенных микроэлементов, которые приходится принимать в виде пищевых добавок. По данным Национального обследования здоровья и питания II (NVS II), в Германии чуть менее 28 % всего населения принимают пищевые добавки, содержащие различные витамины и минералы [7]. Поскольку веганов и вегетарианцев в Германии не так много, то, по-видимому, значительная часть населения, придерживающегося смешанного питания, также дополняют свой рацион пищевыми добавками. В этом нет ничего плохого, если принимать их в правильной дозировке и не пытаться компенсировать ими нездоровый рацион питания. БАДы должны лишь обеспечивать поступление отдельных важнейших питательных веществ в организм в рамках здорового питания. Несмотря на то что некоторые люди ничего не имеют против добавок и даже выступают за них в случае дефицита питательных веществ, БАДы часто ошибочно используются в качестве аргумента против веганской диеты. Между прочим, дефицит B12 наблюдается и у многих людей, придерживающихся смешанного питания, и отнюдь не является исключительной проблемой веганской диеты. Однако с недостатком B12 обычно связывают только веганов.
В 2000 году данные Фрамингемского кардиологического исследования (Framingham Offspring Study) показали, что в группе из почти 3000 обследованных американцев в возрасте 26–83 лет у 39 % участников на смешанной диете уровень B12 в сыворотке также был ниже нормы. У 17 % испытуемых на смешанной диете концентрация была уже на грани дефицита, а у 9 % наблюдался явный дефицит. Хотя измеренные концентрации B12 в сыворотке снижались с возрастом у всех испытуемых, в группе участников со смешанной диетой в возрасте до 30 лет дефицит был выявлен у 8 %, то есть показания данной возрастной группы также лишь незначительно отличались от данных по старшим возрастным группам. Особенно интересно, что доли испытуемых с выраженным дефицитом B12 в двух группах участников с наибольшим и наименьшим содержанием мяса в рационе существенно не различались. Это еще раз подчеркивает важность способности к усвоению B12 для удовлетворения потребностей организма. Наилучшие показатели в сыворотке были определены не у испытуемых на смешанной диете с наибольшим потреблением продуктов животного происхождения, а у участников, регулярно включающих в рацион пищевые добавки, содержащие B12, или продукты, обогащенные B12 [8]. Это неудивительно, поскольку концентрация B12 в пищевых добавках обычно намного выше. Кроме того, витамин из БАДов усваивается даже лучше, чем витамин, получаемый с пищей [9]. У большинства участников на смешанной диете с пониженным уровнем B12 наблюдалось нарушение всасывания витамина (мальабсорбция), поэтому они получали достаточное количество B12 из пищи, но не могли усвоить его в полном объеме [10]. Однако таким людям обычно помогают более высокие дозы свободного B12 из пищевых добавок, поскольку в БАДах этот витамин не связан с белками и поэтому легче усваивается. Кроме того, некоторые продукты, содержащие синтетические формы B12, подвергаются еще большей критике за их ненатуральность. Однако синтетический B12, или цианокобаламин, не только более стабилен, но и лучше изучен, чем встречающиеся в природе формы B12 [11]. Это не призыв к тому, чтобы люди принимали витамин в виде БАДов, а не пищевых продуктов, однако это демонстрирует, что ненатуральные компоненты иногда могут быть очень полезными и что в конечном итоге важно, чтобы питательное вещество было получено в рекомендуемом объеме. Организму все равно, поступает ли B12 из печени или из пищевой добавки, главное, чтобы его количество было соответствующим. Возможно, это не относится в равной степени ко всем питательным веществам, однако, похоже, это как раз случай с B12.
Таким образом, Фрамингемское кардиологическое исследование показывает, что, независимо от рациона питания и возраста, дефицит B12 наблюдается у большего количества людей, нежели предполагалось ранее. Поскольку в данном исследовании измерялся только общий уровень витамина B12 в организме участников, а не более чувствительный показатель активного B12 (голотранскобаламина), о котором мы расскажем позже, можно даже предположить, что при использовании более точных методов исследования дефицит был бы диагностирован у еще большего числа людей. Однако было бы преувеличением говорить о дефиците B12 как о «болезни нации», как его называют в некоторых работах. Этот факт доказывает недальновидность причисления дефицита B12 к исключительно веганским проблемам.
Эта глава призвана не только развеять сомнения невеганов в отношении растительной диеты из-за дефицита B12. Она также побуждает веганов воздержаться от смелых непроверенных идей по приему B12.
Как будет показано в настоящей главе, подавляющее большинство якобы природных источников B12 оказываются ложными, и слишком много людей уже нанесли необратимый вред своему здоровью, поверив в них и получив в результате серьезный дефицит витамина.
Список людей с тяжелым дефицитом B12 и серьезными, иногда необратимыми нарушениями в литературе по диетологии уже длинный, и он не должен расширяться [12, 13].
Основные сведения о витамине B12
Прежде чем мы рассмотрим различные источники B12 и развеем некоторые мифы об этом витамине, обсудим некоторые основные моменты, касающиеся B12.
Строго говоря, собирательный термин «витамин B12» (кобаламин) охватывает целый ряд различных кобаламинов, тесно связанных друг с другом химически. Все они имеют одну и ту же базовую структуру, на основе которой создаются различные формы. Как следует из названия кобаламина, центральным атомом в его основе является атом кобальта, к которому присоединены различные боковые группы. В зависимости от того, какая остаточная группа присоединена к основе, различают несколько форм кобаламинов. В настоящей главе представлены четыре наиболее важные формы.
Чаще всего различают метилкобаламин и цианокобаламин, поскольку это две формы, наиболее популярные в препаратах. Однако к кобаламинам относятся также гидроксокобаламин и аденозилкобаламин. Они встречаются как в природе, так и в некоторых пищевых добавках [14].
Цианокобаламин является синтетическим соединением, которое не встречается в природе в такой форме и не является биологически активным. Это означает, что организм должен сначала преобразовать его в активную форму B12. Однако преимущество цианокобаламина состоит в том, что это не только самая дешевая, но и самая стабильная форма из всех видов B12 [15]. Метилкобаламин и в еще большей степени аденозилкобаламин и гидроксокобаламин содержатся в продуктах питания в различных соотношениях [16]. Метилкобаламин и аденозилкобаламин являются двумя активными формами B12, в то время как гидроксокобаламин необходимо сначала преобразовать в активную форму.
Суточная норма витамина B12
По данным Немецкого общества питания, фактическая суточная потребность в B12 составляет всего 2 мкг (микрограмма). Однако Немецкое общество питания рекомендует взрослым принимать более высокую дозу – 4 мкг в день [17][5]. Это связано с тем, что люди обычно не могут усвоить весь витамин B12 из пищи или добавок, а также способность к усвоению снижается с возрастом и существуют индивидуальные различия в способности к усвоению. Рекомендация актуальна и в рамках смешанного питания. Но объективно это количество также незначительно и показывает, насколько мало на самом деле нужно организму витамина B12: 4 мкг – всего лишь три миллионные доли грамма.
Таким образом, даже если бы вы дожили до 100 лет, за всю жизнь вам потребовалось бы всего 0,1 г витамина B12.
Однако в 2006 году одно из исследований поставило под сомнение официальные рекомендации, по крайней мере, для людей преклонного возраста, поскольку данные по итогам анализов 100 датских женщин в период постменопаузы показали, что количество витамина в крови можно оптимально повысить в результате ежедневного приема 6 мкг B12 [81]. Затем, в 2010 году, была обследована более многочисленная группа, состоящая из почти 300 американских мужчин и женщин в возрасте 18–50 лет. Установлено, что показатели крови всех тестируемых достигали оптимального значения при приеме 4–7 мкг B12 в сутки [19]. Однако даже при суточной потребности в 6 мкг человек за сто лет жизни может усвоить лишь около 0,25 г B12.
Вопреки распространенному мнению, витамин B12 относительно стабилен при нагревании. Потери B12 в продуктах животного происхождения варьируются в пределах 10–30 % при обычных способах приготовления пищи в домашних условиях [20, 21, 22, 23]. Во время таких процессов, как пастеризация молока, разрушается 5-10 % витамина [24]. Даже когда молоко нагревается до сверхвысоких температур, теряется лишь около трети [25]. Термостойкость витамина распространяется и на B12, который, например, в некоторых странах добавляют в муку. Хлебное тесто, обогащенное B12, теряет в процессе выпечки также лишь треть от первоначального содержания витамина [26].
Краткий экскурс в анатомию человека
Важно получать достаточное количество витамина B12 с пищей или соответствующими добавками. Кроме того, большую роль играет и то, насколько хорошо витамин усваивается организмом. Люди по разным причинам нередко страдают от легкой и тяжелой формы дефицита витамина B12, несмотря на достаточное потребление пищи. Чтобы лучше разобраться в этой важной теме, необходимо кратко рассказать об устройстве и функционировании пищеварительного тракта человека. Это единственный способ получить лучшее представление о сложных путях, которые B12 должен пройти в организме, прежде чем он сможет полностью выполнить свои функции. Рис. 12 помогает наглядно представить, где могут возникнуть проблемы, препятствующие оптимальному усвоению и действию витамина B12.
B12, который иногда также называют внешним фактором Кастла, преимущественно связан с белками пищи, и поэтому еще одно его название – комплекс B12-белок. В желудке B12 отделяется от белка ферментами, содержащимися в желудочной кислоте (так называемыми протеазами) и продолжает свой путь уже в виде свободного B12. Часть свободного кобаламина в пищевых добавках связывается с транспортными белками в ротовой полости, с которыми B12 из комплекса B12-белок может связаться только после отделения от пищевого белка в желудке. Этот транспортный белок, называемый гаптокоррином (ГК), вырабатывается в слюнных железах слизистой оболочки полости рта с целью защиты B12 от воздействия желудочной кислоты сразу после его попадания в желудок. Различные типы протеаз с разными названиями активны в разных местах пищеварительного тракта человека. В желудочной кислоте за расщепление B12 из пищевого белка отвечает так называемый пепсин.
РИС. 12: УСВОЕНИЕ ВИТАМИНА B12 В ОРГАНИЗМЕ ЧЕЛОВЕКА [27, 28, 29, 30]

Попадая в желудок, связанный с белком B12 отщепляется от него с помощью фермента пепсина. Теперь этот свободный, но чувствительный к кислоте B12 нуждается в защите от желудочной кислоты, чтобы попасть из желудка в тонкий кишечник без повреждений. Поэтому, как и свободный B12, он связывается с защитными транспортными белками (гаптокоррином) из слизистой оболочки полости рта, попавшими в желудок вместе с пищевой целлюлозой, образуя комплекс B12-гаптокоррин. Это позволяет защитить витамин от воздействия желудочной кислоты. В желудке, точнее в слизистой оболочке желудка, также есть париетальные клетки, которые выделяют чрезвычайно важный внутренний фактор Кастла (ВФК) – еще один специальный транспортный белок, имеющий огромное значение для последующего всасывания B12 в тонком кишечнике.
После того как комплекс B12-гаптокоррин покидает желудок и попадает в первый отдел тонкого кишечника (двенадцатиперстную кишку), в игру вступает другой фермент, расщепляющий белок. На этот раз он выделяется поджелудочной железой и попадает в тонкий кишечник. Этот фермент называется трипсин. Он расщепляет исходный комплекс B12-гаптокоррин, в результате чего B12 снова высвобождается. Это позволяет ему присоединиться ко второму транспортному белку, внутреннему фактору, вырабатываемому в желудке. Этот транспортный белок проходит тот же путь от желудка в тонкий кишечник. Теперь комплекс B12-внутренний фактор защищен от протеолитических ферментов и может передвигаться по тонкому кишечнику. Когда он достигает третьего, последнего отдела тонкого кишечника, так называемой подвздошной кишки, он прикрепляется к специальным рецепторам внутренних факторов слизистой оболочки тонкого кишечника и всасывается в кровь. Ограниченное количество рецепторов является главной причиной того, что за единицу времени всасывается только около 1,5–2,5 мкг B12 и полная способность к всасыванию B12 восстанавливается только через 4–6 часов, когда ранее прикрепленный B12 отсоединяется от рецепторов и попадает в кровоток.
После того как B12 абсорбируется рецепторами внутренних факторов, он попадает в клетки слизистой оболочки тонкого кишечника, и здесь комплекс B12-внутренний фактор вновь расщепляется, чтобы B12 мог связаться с другими транспортными белками для его попадания в кровь. Около 20 % всасываемого B12 связано с так называемым транскобаламином II, который образуется в клетках слизистой оболочки тонкого кишечника. Этот комплекс B12-транскобаламин II называется голотранскобаламином II (Holo-TC). В отличие от комплексов B12 с другими транспортными белками крови, это единственный комплекс, поглощаемый клетками, и, следовательно, он является активным.
Многим людям голотранскобаламин уже знаком по анализам крови, поскольку именно его концентрацию определяют, если хотят узнать количество активного B12 в организме.
После того как комплекс B12-транскобаламин II поступает в клетки-мишени, например, в печень или костный мозг, он соединяется с имеющимися там рецепторами транскобаламина II и таким образом усваивается в клетке. Остальные 80 % витамина B12, которые не присутствуют в крови в виде голотранскобаламина II, связаны с другими транспортными белками и не являются биологически активными. Их точная функция пока не установлена.
В зависимости от места действия B12 он преобразуется в ту или иную форму. Не каждый тип B12 может выполнять все необходимые функции, и, например, метилкобаламин не может играть роль аденозилкобаламина и наоборот. Гидроксокобаламин и цианокобаламин неактивны в организме, и оба должны сначала быть преобразованы в соответствующую форму (метилкобаламин или аденозилкобаламин), чтобы стать биологически активными и иметь возможность выполнять свои функции.
В цитоплазме клетки метилкобаламин образуется из различных кобаламинов, поступающих с пищей или из пищевых добавок. Хотя метилкобаламин выполняет несколько функций, одна из них особенно важна для организма. Он расщепляет токсичную аминокислоту гомоцистеин, которая образуется при употреблении продуктов, содержащих метионин. Поэтому в некоторых случаях повышенный уровень гомоцистеина может косвенно свидетельствовать и о дефиците B12. Но, в отличие от метилкобаламина, B12 выполняет еще одну важную задачу. Для обеспечения организма достаточным количеством энергии в цитоплазме клеток есть митохондрии, которые функционируют как электростанции для клетки и обеспечивают ее энергией за счет биохимических реакций. Важную роль в этом сложном процессе играет B12 в форме аденозилкобаламина. Поэтому, в отличие от цитоплазмы, в митохондриях из различных кобаламинов образуется не метилкобаламин, а аденозилкобаламин. Если в митохондриях слишком мало аденозилкобаламина, то увеличивается количество так называемой метилмалоновой кислоты. Это, в свою очередь, также может служить косвенным маркером дефицита B12. Гомоцистеин и метилмалоновая кислота подробно рассматриваются в разделе, посвященном параметрам, с помощью которых можно оценить обеспеченность организма B12.
История витамина B12
Что касается витамина B12, то начало веганства было несколько неудачным в этом отношении. В ноябре 1944 года Дональд Уотсон, пионер веганского движения, организовал встречу с Элси Шринли и четырьмя другими «немолочными вегетарианцами». На ней они обсудили свою диету и образ жизни как «строгих вегетарианцев без молочных продуктов и яиц» и ввели термин «веган». Так они заложили основу веганства в его современном виде [31].
Однако концепция веганства как диеты, состоящей исключительно из растительных продуктов и совершенно исключающей продукты животного происхождения, возникла гораздо раньше. Документы этого периода могут дать интересное представление о раннем неустановленном дефиците витамина B12 после длительного соблюдения исключительно растительной диеты. В публикации World Veganism – past, present, and future историк Джон Дэвис дает подробный обзор ранней истории веганства и называет «отцом веганского питания» [32] британского врача доктора Уильяма Ламбе, который в 1806 году в возрасте 41 года по состоянию здоровья перешел на чисто растительную диету. Затем он постоянно поддерживался такого питания в течение 41 года, пока не умер в 1848 году. По словам членов его семьи, незадолго до своей смерти он отлично себя чувствовал. Через девять лет после перехода на веганскую диету в 1815 году он опубликовал революционный труд о своих успехах в отношении собственного здоровья и здоровья некоторых своих пациентов, достигнутых благодаря растительной диете, под названием Additional Reports on the Effect of a Peculiar Regimen in cases of Cancer, Scrofula, Consumption, and оther Chronic Diseases.
Под «особым режимом питания» подразумевалась полезная, чисто растительная диета, и, таким образом, это было первое в истории конкретное упоминание о веганстве.
Уже в 1850 году стало ясно, что в первые несколько лет после изменения рациона многие люди смогли добиться значительного улучшения здоровья и излечения хронических заболеваний с помощью такой диеты [33]. Но в книге также подчеркивается и то, что через некоторое время после перехода на чисто растительную диету у многих наблюдалось ухудшение состояния здоровья, и улучшение наступало только тогда, когда они снова начинали есть мясо.
В предисловии говорится, что это, видимо, связано с разбавлением первоначально очень здоровой и строгой растительной диеты. В книге предполагается, что со временем новые веганы включали в свой рацион все больше нездоровой растительной пищи и слишком много калорий и, таким образом, стали тем, кого сейчас называют «веганами нездоровой растительной пищи».
Однако почему их состояние улучшилось, когда они снова стали есть мясо? Поскольку в то время B12 еще не открыли, люди не знали, что в продуктах животного происхождения содержится необходимый витамин, которого может постоянно не хватать при чисто растительной диете. Без знаний о B12 в то время не могли дать объяснение такому ухудшению здоровья. Поэтому в качестве причины указывалось разбавление здорового растительного питания нездоровыми блюдами из растительных продуктов. При современном уровне знаний более очевидно, что такое ухудшение во многих случаях можно объяснить продолжительным дефицитом B12. Ни доктор Ламбе в 1818 году, ни Дональд Уотсон в 1944 году не могли ничего знать о B12, поскольку этот последний на сегодняшний день известный нам витамин был открыт только в 1948 году, а его точную структуру установили лишь в 1955 году [34].
Еще в 1926 году ученые смогли вылечить смертельно опасную во многих случаях пернициозную анемию, назначая сырую или быстро приготовленную печень. Это было первым заболеванием, которое связали с дефицитом витамина B12.
У пациентов с пернициозной анемией наблюдаются серьезные нарушения всасывания B12, что приводит к его дефициту несмотря на оптимальное потребление продуктов животного происхождения. Но благодаря высокому содержанию витамина в таком продукте, как печень, организм тех пациентов смог усвоить достаточное для выздоровления количество B12 [35].
В то время еще не установили, что смертельно опасную пернициозную анемию удалось вылечить именно благодаря веществу, которое спустя годы было названо витамином B12, поскольку необходимые знания еще отсутствовали. Было известно лишь то, что в печени содержится некое вещество, которому в то время еще не дали название. Поэтому его временно назвали «печеночным фактором» и стали использовать печень для целенаправленного лечения пернициозной анемии. Конечно, о других многочисленных функциях «печеночного фактора» (B12) в то время ничего не было известно, и прошло много лет, прежде чем этот витамин и все его функции в организме человека изучили в полном объеме. В 1944 году, когда было основано Веганское общество, впервые был представлен внутренний фактор (ВФ), необходимый для усвоения B12. В то время термина «витамин B12» еще не существовало, и в качестве аналога «внутреннего фактора» его называли просто «внешним фактором», относящимся к категории витаминов. Это означало, что как минимум один важный этап метаболизма витамина уже был установлен, и это дало ученым возможность дальнейшего изучения B12. Только спустя четыре года, в 1948 году, двум разным исследовательским группам независимо друг от друга удалось выделить витамин B12 и впоследствии сделать его доступным для широких слоев населения [36].
Таким образом, прошло много лет истории веганства, прежде чем люди узнали о B12 и его значении в веганской диете. Поэтому неудивительно, что спустя некоторое время от перехода на растительную диету многие первые веганы начинали страдать от последствий дефицита B12. Даже после появления B12 в качестве биологически активной добавки она далеко не сразу стала популярной среди веганов. Даже через 45 лет после открытия B12 опрос веганов, проведенный в 1993 году, показал, что около 66 % респондентов по-прежнему считают, что веганская диета обеспечивает их всеми необходимыми витаминами только за счет растительных источников. Однако авторы уже тогда пришли к выводу, что B12 необходимо включать в рацион веганов в виде пищевой добавки [37].
В ходе опроса, проведенного Федеральным институтом оценки рисков (BfR) в 2016 году, в очередной раз оценивался уровень знания о необходимости приема B12 в веганской диете, и результаты, к счастью, оказались гораздо лучше: 95 % опрошенных веганов знали, что B12 в веганской диете недостаточно, а 79 % также принимали его в виде добавок [38]. Федеральный институт оценки рисков пришел к выводу, что, судя по результатам опроса, уровень осведомленности веганов о питании выше среднего [39]. В средствах массовой информации также появились многообещающие сообщения под заголовком «Веганская диета: фактор риска ниже, чем ожидалось» [40].
Несмотря на положительную динамику, все еще существует несколько процентов веганов, которые не подозревают о недостатке этого питательного вещества. Даже сегодня некоторые люди, сбитые с толку спорами о витамине, все еще задаются вопросом, следует ли им принимать пищевые добавки с B12. Кроме того, разница между опрошенными веганами, которые знают о потенциальном дефиците, и теми, кто действительно принимает добавки, свидетельствует о том, что помимо незнания существует и определенная небрежность. Более того, некоторые призывают к естественному поступлению B12 в организм через немытые овощи, самостоятельное получение его из собственных кишечных бактерий и другие непроверенные источники, тем самым ставя под угрозу здоровье многих людей.
Синтез B12 в организме
В рубце жвачных животных, таких как коровы, козы и овцы, содержится достаточное количество бактерий, продуцирующих B12 [41]. Таким образом, они могут обеспечивать себя этим витамином при условии, что в их корма поступает достаточное количество кобальта. Поэтому в книгах, журналах и блогах неоднократно поднимается вопрос о том, способен ли человеческий организм самостоятельно производить B12 несмотря на существенные анатомические различия. Так, тема затрагивается и в статье Mythos B12, где по поводу выработки этого витамина человеческим организмом написано следующее: «Может ли быть такое, что наш организм идеально устроен, но матушка-природа допустила такую странную ошибку? Конечно, нет. Это было бы нелогично. ‹…› Ни одно животное в природе не заботится о таких деталях – это делает только человек» [42]. Однако предположение об идеальном функционировании всего природного и нелогичности всего остального является ложным выводом.
Никто не оспаривает, что человек является носителем микроорганизмов, воспроизводящих B12. Есть лишь разумные сомнения в том, что они могут способствовать поступлению B12 в организм как человека, так и жвачного животного.
Об этом также свидетельствует исследование 1950-х годов, в котором анализ кала испытуемых с дефицитом B12 показал, что витамин B12 все еще присутствует в фекалиях участников, несмотря на его отсутствие в их рационе. Это подчеркивает тот факт, что в кишечнике человека живут бактерии, вырабатывающие B12. Однако низкий уровень витамина в крови говорил о том, что B12, вероятно, не всасывается, а выводится в неусвоенном виде с калом.
Ученые, проводившие это исследование в 1950-х годах, также организовали необычный эксперимент по компенсации дефицита B12. Они извлекали B12 из кала, подготавливали его и вводили испытуемым. Как оказалось, B12 был биодоступным, и эти инъекции успешно компенсировали дефицит B12 у испытуемых [43]. Этот нетрадиционный метод исследования не только показал, что бактерии, живущие в кишечнике человека, вырабатывают достаточное количество биодоступного B12, но и то, что он не усваивается в месте своего производства. В противном случае у испытуемых не было бы дефицита B12. Причина парадокса заключается в том, что B12 всасывается в тонком кишечнике, а вырабатывающие его бактерии находятся в толстом кишечнике [44]. Именно поэтому вырабатываемый B12 не может всасываться и выводится из организма в неусвоенном виде.
Тот факт, что травоядным животным в дикой природе не приходится беспокоиться о своих запасах B12, также мало что говорит о получении витамина веганами. Травоядные животные удовлетворяют свои потребности в витамине как минимум четырьмя способами, которыми вряд ли воспользуется подавляющее большинство веганов. Во-первых, травоядные жвачные животные покрывают свои потребности в B12 за счет собственного производства, поскольку микроорганизмы, живущие в рубце, вырабатывают B12, который, в отличие от человека, жвачные животные способны усваивать [45].
Другие травоядные, не относящиеся к жвачным животным, предположительно получают достаточное количество B12 иным пособом – через загрязненную воду, почву или другие загрязняющие вещества [46]. Кроме того, копрофагия, т. е. поедание собственных экскрементов, наблюдается у многих видов как третий способ получения витамина в животном мире. К животным-копрофагам относятся грызуны, птицы, насекомые и обезьяны. Причем некоторые из них способны получать B12, вырабатываемый бактериями их кишечной флоры, но ни одно из этих животных не может непосредственно усвоить витамин [47]. Четвертый способ получения витамина B12 травоядными животными заключается в том, что многие из них не являются чисто травоядными и получают витамин за счет периодического употребления в пищу насекомых и другой животной пищи [48]. Насекомые могут находиться и в диких фруктах, которыми питаются животные, что косвенно делает фрукты хорошим источником B12 [49]. Однако некоторые приматы, например шимпанзе, которых иногда ошибочно относят к травоядным, активно охотятся на других животных и таким образом потребляют мясо в качестве источника B12 [50].
Поскольку люди не являются жвачными животными, а загрязненная вода или экскременты не могут стать альтернативой источника В12 для веганов, нам приходится беспокоиться о получении B12.
В 1970-х [51], 1980-х [52] и 1990-х [53] годах, а также в последние два десятилетия [54, 55] многочисленные сообщения о нехватке витамина неоднократно показывали, что у веганов, не принимающих добавки B12, в долгосрочной перспективе развивается дефицит, иногда с серьезными последствиями, и что их организм не способен выработать витамин самостоятельно. Согласно другой теории, чистая или преимущественно сырая пища и в целом здоровый и естественный образ жизни могут перестроить работу кишечника таким образом, что, в отличие от остальных, веганы смогут сами обеспечивать себя B12. Научной литературы по этому вопросу не так много. Было проведено исследование, в котором приняли участие сторонники этой теории, придерживающиеся, по их мнению, особенно здорового растительного рациона, который включал в себя преимущественно термически необработанные фрукты и овощи в сочетании с орехами и проростками. Результаты показали, что у 92 % испытуемых все равно наблюдался дефицит B12 [56]. Перед началом исследования они также заявили, что не принимают добавки, поскольку, по их мнению, здоровое и естественное питание создает здоровую кишечную флору, которая, в свою очередь, способствует самообеспечению B12. Однако результаты эксперимента говорят о другом.
Обогащение растений витамином B12
Еще в 1988 году в одной публикации утверждалось: «Ни в одном продукте, растущем из земли, не содержится полезного витамина B12» [57]. Однако в книге о средиземноморской диете д-ра Дугласа Грэма, упомянутой в главе о белках, говорится, что через корни растения поглощают питательные вещества, в том числе и витамин B12 [58]. Это, конечно, верно. Однако сколько B12 должно содержаться в почве, чтобы растение накопило его в достаточном количестве? В отличие от человека и животных метаболизм растений не требует присутствия B12 [59], и это, вероятно, одна из причин того, что в подавляющем большинстве исследований в растениях не было обнаружено существенного количества B12, которое было бы полезно для человека. Независимо от того, нуждаются ли растения в этом витамине, возникает вопрос о том, в какой степени они вообще способны его усваивать и накапливать. В одном из исследований, посвященном именно этому вопросу, использовались ростки редиса, чтобы проверить, изменяется ли содержание витамина B12 в растениях при добавлении его в питательную среду для ростков [60].
Результаты исследования показали фактическое повышение уровня B12. Исследуемые ростки редиса содержали значительное его количество: 1,28 мкг на 1 г свежих ростков при добавлении B12 в питательную среду. Таким образом, ученые пришли к выводу, что ростки, выращенные в питательной среде, обогащенной B12, могут быть богатым чисто растительным источником этого витамина. Означают ли результаты эксперимента, что растения, как предсказывает д-р Грэм, могли бы поглощать достаточное количество B12 из природной почвы, если бы микроорганизмы производили его прямо в земле?
Для сравнения: количество B12, необходимое для обогащения ростков, во много раз превышает его содержание в естественной среде, то есть в почве. Ученым потребовался питательный раствор с 200 мкг витамина B12 на 1 мл, чтобы получить 1,28 мкг витамина на 1 г свежих ростков. При более низких концентрациях B12 в воде для замачивания (25 мкг/мл) концентрация в ростках все еще составляла 0,3 мкг/г. Однако даже эти более низкие концентрации не обнаружены в исследованных на сегодняшний день образцах почвы природного происхождения, где витамина содержится от 0,002 до 0,015 мкг на 1 г [61].
Такие высокие концентрации, которые использовались в этом исследовании, могли быть достигнуты только путем специального добавления B12 в почву, а это означает, что для получения «натурального» витамина B12 в любом случае придется в больших количествах добавлять в почву или воду для замачивания «ненатуральный» B12.
Кроме того, при накоплении его в растении могут возникнуть большие потери витамина B12 из исходной добавки. Такой способ нельзя считать ни натуральным, ни эффективным, поэтому гораздо разумнее добавлять соответствующее количество витамина непосредственно в пищу. Часто утверждается, что B12 был бы более биодоступным, если бы он поступал в организм с помощью растительных или животных источников, а не через пищевые добавки. Однако это утверждение не подтверждается какими-либо результатами исследований, и похоже, что на самом деле все обстоит как раз наоборот. Во Фрамингемском кардиологическом исследовании именно люди, принимавшие добавки B12 или обогащенные им продукты, имели более высокие концентрации витамина в сыворотке крови, чем участники на смешанной диете [62].
Какова концентрация витамина в растениях, которые были удобрены на поле коровьим навозом, содержащим B12? Достаточно ли в них витамина для наших ежедневных потребностей? Как и человеческие фекалии, коровий навоз также содержит большое количество B12, поэтому теоретически возможно, что он обогащает растения этим витамином. В исследовании, проведенном в 1994 году, содержание B12 в шпинате и ячмене при удобрении их навозом увеличилось в два и три раза соответственно. Поэтому результаты этого исследования неоднократно приводились в качестве доказательства того, что причиной недостаточного поступления B12 в организм является лишь неправильное удобрение и в целом неплодородная почва в промышленном сельском хозяйстве [63].
Однако часто не учитывают, что, несмотря на удвоение или утроение концентрации, количество витамина в растениях оставалось все еще недостаточным для удовлетворения суточных потребностей человека в B12.
Так, в шпинате, выращенном на удобренной почве, она по-прежнему была довольно низкой, всего 0,14 мкг/100 г [64]. Это означает, что придется съедать почти 3 кг шпината в день, чтобы удовлетворить потребность в 4 мкг. Для получения более высокой рекомендуемой нормы в 6 мкг в день потребуется более 4 кг шпината.
Несмотря на то что мы часто слышим и читаем о пользе ферментированных продуктов в качестве источника витамина B12, таких как квашеная капуста и йогурт, сами по себе они не должны рассматриваться как адекватные источники B12, поскольку не все бактериальные культуры могут производить одинаковое количество витамина [65]. Например, исследование кимчи (корейского блюда из ферментированных овощей) показало, что содержание в нем B12 составляет всего 0,2 мкг/100 г [66]. Авторы также отмечают, что этот витамин, содержащийся в кимчи, предположительно поступает из рыбного соуса, входящего в состав блюда, а не возникает в результате ферментации. Поэтому сомнительно, что веганские кимчи вообще содержат существенное количество B12. Однако другие многообещающие исследования показывают, что при использовании правильных бактериальных культур квашеная капуста может содержать поразительные 7,2 мкг преимущественно биодоступного B12 на 100 г блюда за счет ферментации так называемыми пропионибактериями [67]. В 2015 году были получены даже более высокие результаты при добавлении в соевый йогурт молочнокислых бактерий Lactobacillus reuteri. Полученный продукт содержал 18 мкг витамина B12 на 100 мл. При этом только 10 % составляли неактивные формы B12, поэтому в йогурте было более 16 мкг биодоступного B12 на 100 мл [68]. Однако необходимо какое-то время для запуска промышленного производства таких продуктов по приемлемым ценам и проверки их эффективности на людях, поэтому пока лучше принимать проверенные добавки с витамином B12.
Из всех потенциальных кандидатов на роль растительного источника B12 водоросли представляются наиболее перспективными. Однако, поскольку существует более 40 000 различных видов водорослей, трудно сделать общий вывод о них как об однородной группе растений. Не все водоросли вообще являются растениями. Если зеленые водоросли, такие как хлорелла, относят к растениям, то красные, такие как нори, являются лишь их родственниками. Сине-зеленые водоросли, например, спирулина, на самом деле вовсе не водоросли, а бактерии, хотя они до сих пор считаются водорослями [69].
При изучении 326 различных видов водорослей было обнаружено, что, в отличие от наземных растений около половины из них нуждаются в B12 для правильного метаболизма. Следовательно, они могут накапливать значительное количество этого витамина [70].
Однако тот факт, что растение содержит B12, не делает его богатым источником витамина. Помимо биодоступных форм B12, существует ряд небиодоступных кобаламинов, известных как аналоги B12. Они не только не приносят пользы человеку, но и могут снижать усвоение активного B12, поступающего одновременно с ним [71]. Однако важное различие между биодоступным для человека B12 и его аналогами не может быть учтено при использовании некоторых методов исследования. Популярный способ определения содержания B12 в продуктах питания предполагает использование бактерий, которым также нужен B12. В этом эксперименте в экстракт продукта, в котором определяют количество витамина, вводят молочнокислые бактерии Lactobacillus Leichmannii, и по их росту рассчитывают уровень кобаламина. Однако скорость роста бактерий не всегда является адекватным показателем количества B12, усваиваемого человеком, поскольку эти бактерии могут всасывать некоторые кобаламины, недоступные человеку. Отсутствие различий между биодоступными кобаламинами, полезными для человека, и аналогами B12 привело к тому, что в прошлом для некоторых продуктов питания было неправильно рассчитано количество витамина. Однако во многих случаях до 80 % кобаламинов, содержащихся в растительных продуктах, не являются биодоступными для человека [72].
По этой причине результаты лабораторных исследований продуктов питания могут быть неверными, если используются устаревшие экспериментальные методы, не учитывающие различия между биодоступными кобаламинами и аналогами B12. В частности, некоторые продукты, такие как спирулина, которые до сих пор рекламируются как B12-содержащие продукты, в соответствии с устаревшими результатами исследований, согласно последним данным, практически не содержат биодоступного B12 [73]. Реклама спирулины как богатого источника B12 была признана актом недобросовестной конкуренции, по крайней мере, с того момента, как это решение было вынесено Высшим земельным судом Хамма в 2010 году [74]. Зонтичная организация потребительских центров также поясняет, что наряду со спирулиной в качестве источника B12 не следует использовать сине-зеленые водоросли (Afa) [75]. Результаты тестов на содержание B12 в таких водорослях противоречивы [76, 77], однако их не рекомендуют употреблять, независимо от содержания B12, поскольку они склонны к образованию токсинов, опасных для человека [78]. В то же время спирулина богата питательными веществами и безопасна при правильном производстве.
Для более точного различения кобаламинов и их пользы для человека исследователь водорослей Йорг Ульман рекомендует в качестве лучшей альтернативы метод «жидкостной хроматографии с тандемной масс-спектрометрией» (ЖХ/МС) [79]. Этот метод уже дал очень точные дифференцированные результаты для различных типов кобаламина в исследованиях по измерению концентрации B12 в детских молочных смесях [80]. Такой же дифференцированный подход может быть использован и для других предполагаемых источников B12, таких как водоросли и ферментированные продукты. Обработка водорослей также, по-видимому, играет важную роль в отношении биодоступности содержащегося в них витамина. Например, в одном исследовании было обнаружено 73 % биодоступного витамина B12 в сырых нори, в то время как 65 % кобаламинов в сушеных нори были аналогами B12. Таким образом, ученые пришли к выводу, что в процессе сушки кобаламины в нори превращаются из преимущественно биодоступных в преимущественно небиодоступные [81]. Это обстоятельство может послужить дополнительным объяснением противоречивых результатов измерений содержания B12 в водорослях.
Несовершенство методов измерения, трансформация кобаламинов водорослей в процессе переработки и другие факторы воздействия приводят к сложностям при определении активности B12 в водорослях. Однако в итоге исследования с участием людей должны доказать, что водоросли, в которых предполагается наличие активного B12, действительно эффективны.
Один вид микроводорослей уже много лет занимает совершенно особое место среди всех потенциальных источников B12. Речь идет о хлорелле.
С каждым годом становится все более очевидным, что она содержит большое количество биодоступного витамина B12. Этот вид является одним из наиболее изученных растений в мире. Помимо большого количества белка с высокой биологической ценностью, он содержит самую высокую долю хлорофилла среди всех растений, изученных к настоящему моменту [82].
Исследование различных кобаламинов в хлорелле показало, что в 100 г этой микроводоросли может содержаться до 200 мкг биодоступного B12. Доля аденозилкобаламина была самой высокой – 76 %, далее метилкобаламин – 14 % и гидроксокобаламин – 10 % [83]. Однако в других исследованиях в хлорелле было обнаружено большое количество метилкобаламина [84]. В первом небольшом исследовании эффективности хлореллы на людях трем испытуемым в течение года ежедневно давали по 8 г сушеной хлореллы и каждые три месяца измеряли показатели крови. Оказалось, что прием хлореллы повышает уровень общего B12 и гомоцистеина в крови [85]. Однако оба показателя подвержены влиянию искажающих факторов, поэтому, помимо слишком малого числа испытуемых, это исследование не дало четких результатов из-за отсутствия данных по голотранскобаламину или метилмалоновой кислоте для определения B12. В другом исследовании с участием 17 веганов уровень метилмалоновой кислоты возрос примерно на треть в течение 60 дней при приеме 9 г хлореллы, а измеренный уровень гомоцистеина также увеличился на 10 % [86].
Тем не менее следует сказать, что это не означает, что вся хлорелла является богатым источником B12. Уровень витамина, измеренный в ходе изучения хлореллы, варьировался от нуля до нескольких сотен микрограммов (мкг) на 100 г. Таким образом, при соответствующих условиях хлорелла может содержать большое количество B12, но это не значит, что вся имеющаяся в продаже хлорелла содержит его в таких количествах [87]. Особо важную роль играет выращивание хлореллы. Поскольку существуют различные типы культивирования, то и показатели B12 сильно различаются в зависимости от метода выращивания в открытых резервуарах или ферментаторах [88]. Так как большинство остальных видов водорослей еще недостаточно изучены на предмет содержания в них B12, только будущие исследования в ближайшие годы смогут предоставить более полную информацию. До тех пор, пока мы не получим новые достоверные данные о водорослях и B12 в рамках более масштабных и спланированных исследований, определенно рекомендуется простой, безопасный, дешевый и хорошо изученный способ получения витамина с помощью пищевых добавок. Тем не менее такие результаты имеют большое значение. Как только в будущем в качестве естественного растительного источника B12 появятся растительные йогурты, ферментированные соответствующими бактериями, ферментированные овощи и некоторые водоросли, сомнительный аргумент в пользу ненатуральности веганского образа жизни станет еще более ложным.
Ложные источники B12
Поскольку B12 выполняет в организме множество различных функций, его дефицит может проявляться в самых разных формах. Распространенными легкими симптомами дефицита являются слабость, истощение, перепады настроения, бессонница и иммунодефицит. Если дефицит сохраняется, то это может привести к таким тяжелым симптомам, как спутанность сознания, онемение конечностей и даже паралич, а также нарушения координации и зрения [89].
Хотя дефицит витамина B12 не является широко распространенным заболеванием в западных странах, как это пытаются представить в некоторых публикациях, не только веганы должны следить за его достаточным количеством в организме. Если использовать чувствительные методы исследования, такие как анализ на голотранскобаламин, которые позволяют более точно диагностировать развивающийся дефицит на ранних стадиях, то субклинический дефицит B12 более распространен, чем предполагалось ранее [90]. Тем не менее организм обладает очень большим запасом B12, который человек может использовать в течение длительного времени при условии его достаточного пополнения. Общий запас витамина в организме человека составляет около 3 000 мкг у взрослых и около 30–50 мкг у детей в зависимости от возраста [91].
Поскольку организм довольно эффективно усваивает B12, первые симптомы его дефицита могут проявиться у взрослых через несколько лет, если поступление B12 в организм с пищей или добавками будет отсутствовать, а запасы этого витамина в организме изначально будут полны [92].
Считается, что во избежание проявления дефицита запасы B12 в организме должны содержать не менее 300 мкг витамина [93]. При уровне витамина 3 000 мкг с учетом средней суточной нормы запасы истощатся до минимума примерно за шесть лет.
Однако если до перехода на веганскую диету в организме уже не хватало запасов B12, например, человек долго был вегетарианцем или употреблял очень мало продуктов животного происхождения, то дефицит может возникнуть гораздо раньше. В любом случае не стоит рисковать – нужно начинать прием пищевых добавок сразу же после перехода на вегетарианскую или веганскую диету. Вегетарианцы, в частности, часто не задумываются о приеме добавок с B12, поскольку считают, что автоматически получают достаточное количество витамина из молока и яиц. Однако при средней суточной норме 1,7–2,5 мкг вегетарианцы получают лишь минимальную рекомендованную дозу. А в рамках исследований они потребляли лишь треть от того количества B12, которое получали участники на смешанной диете [94]. Яйца также не являются идеальным источником этого витамина.
Хотя в яйце содержится 0,9–1,4 мкг витамина B12, большая часть которого находится в желтке, его биодоступность крайне низка. Общее количество биодоступного B12 в яйце составляет всего 4–9 % при потреблении 100 г. Его уровень снижается при большем потреблении яиц за один прием пищи из-за насыщения рецепторов [95, 96]. Таким образом, биодоступность витамина в яйцах во много раз ниже, чем в молоке (55–65 %), мясе (56–77 %) или рыбе (38–42 %) [97]. Исходя из этих данных, для получения даже минимальной рекомендованной нормы в 4 мкг в день необходимо ежедневно съедать несколько килограммов яиц. Поэтому вегетарианцам также рекомендуется следить за уровнем B12 в организме и на всякий случай принимать пищевые добавки для перестраховки.
Кроме того, Национальные институты здоровья (NIH) [98] и Институт медицины (IOM) [99] США рекомендуют всем людям старше 50 лет получать большую часть B12 из обогащенных продуктов питания или пищевых добавок независимо от количества потребляемого мяса. Причиной этого является ухудшение усвоения B12 из пищи с возрастом. Витамин, содержащийся в продуктах питания, в основном связан с белком и для дальнейшего метаболизма должен сначала отделиться от него в процессе пищеварения. В пожилом возрасте это может происходить лишь в ограниченной степени, поэтому рекомендуется принимать пищевые добавки с B12. В них витамин не связан с белками. Наоборот, он доступен в свободной форме и поэтому обычно лучше усваивается пожилыми людьми. Кроме того, в пищевых добавках, как правило, присутствуют более высокие концентрации витамина, что компенсирует любые потери в процессе усвоения.
Также усвоение B12 снижается при приеме некоторых лекарственных препаратов, и тогда требуется увеличение его потребляемого количества. Людям, которые длительно принимают один или несколько таких препаратов, следует обратить особое внимание на уровень B12.
Среди лекарств, снижающих количество витамина B12 в организме, следует отметить следующие [100, 101]:
• Ингибиторы протонной помпы, подавляющие секрецию желудочной кислоты, например омепразол.
• Антагонисты Н2-гистаминовых рецепторов для подавления секреции желудочной кислоты, например циметидин.
• Препараты для снижения уровня сахара в крови при диабете, например метформин.
• Препараты, снижающие артериальное давление (ингибиторы АПФ), например каптоприл.
• Противоаритмические средства, например бета-блокаторы.
• Препараты, снижающие уровень холестерина, например статины.
• Лекарства от подагры, например холецицин.
• Антациды для нейтрализации желудочной кислоты при изжоге.
• Противоэпилептические препараты.
• Оральные контрацептивы (противозачаточные таблетки).
• Антибиотики широкого спектра действия, такие как неомицин, хлорамфеникол и т. д.
• Противовоспалительные препараты для лечения болезни Крона и язвенного колита, например асакол.
Существуют также данные о том, что очень высокие дозы витамина С могут снижать всасывание B12, поскольку витамин С разрушает часть витамина B12 или превращает его в неактивные формы. Впервые предположение о том, что высокие дозы витамина C, принимаемые одновременно с B12, могут отрицательно сказываться на последнем, было высказано в 1974 году [102], а в 2014 году его вновь подтвердили [103]. Для подстраховки пищевые добавки с высокими дозами витамина С следует принимать не менее чем через четыре часа после приема витамина B12. В первую очередь это касается добавок, содержащих несколько суточных норм витамина, а не продуктов питания с небольшим количеством витамина С. Кроме того, некоторые заболевания могут снижать усвоение B12 или увеличивать потребность в нем. Как следствие, необходимо принимать большее количество B12.
Болезни, сокращающие количество витамина B12 [104]:
• Целиакия.
• СПИД.
• Онкологические заболевания органов ЖКТ.
• Болезнь Крона.
• Хронический гастрит.
• Гастрэктомия или резекция желудка (частичное или полное удаление желудка).
• Алкоголизм.
• Паразитарные заболевания, вызванные личинками ленточных червей.
• Печеночная недостаточность.
• Панкреатическая недостаточность.
Как видно из списка, прием различных лекарств на постоянной основе во многих случаях приводит к снижению запасов B12, но на упаковках большинства медицинских препаратов это в ряду побочных эффектов не указывают. Более подробную информацию о действии распространенных лекарственных средств на наиболее важные питательные вещества можно найти в книге Уве Гребера Arzneimittel und Mikronähr stoffe («Лекарства и микроэлементы») [105].
Кроме того, малоизвестно, что применение закиси азота для наркоза приводит к резкому сокращению количества витамина B12 [106]. Это не является серьезной проблемой, если запасы витамина сделаны заранее и быстро восполняются после анестезии. В противном случае действие закиси азота может иметь огромные последствия, что объясняет некоторые нетипичные осложнения после операции. Для проверки способности пациентов усваивать B12 врач д-р Роберт Шиллинг, автор так называемого «теста Шиллинга» [107], еще в 1986 году задал в своей статье важный вопрос: «Опасна ли анестезия закисью азота для пациентов с дефицитом витамина B12?» [108] На основе историй болезни за последние 30 лет на этот вопрос следует ответить утвердительно, и многие необратимые расстройства, вероятно, можно было бы предотвратить или вылечить, если бы о них знало большее количество пациентов.
В 2000 году в одном медицинском журнале сообщалось о 69-летнем пациенте. Ранее он работал мясником. Пациенту была проведена плановая операция на предстательной железе под наркозом с использованием закиси азота. В течение первых двух недель после операции его походка стала неустойчивой, а ноги начали неметь. Из-за проблем с желчным пузырем в последующие недели ему пришлось сделать еще одну операцию под наркозом с закисью азота. Несмотря на симптомы после первой операции тест на B12 не проводился. После второй анестезии он очнулся в спутанном сознании, а первоначальное легкое онемение ног усиливалось с каждой неделей. В течение следующих четырех месяцев онемение усилилось до такой степени, что это привело к полному параличу ниже пояса. Он стал страдать недержанием мочи, забывчивостью. В итоге у него проявились первые признаки начальной стадии деменции. Наконец, спустя еще три месяца мучений ему поставили диагноз «острый дефицит B12», который отчасти был вызван действием анестезии. Несмотря на прием больших доз витамина и активную физиотерапию, из-за слишком долгого периода дефицита B12 последствия не удалось устранить полностью, поэтому даже более чем через год пациент был способен самостоятельно передвигаться лишь на небольшие расстояния [109].
История 47-летней пациентки, бывшей балерины, которая во время косметической операции в течение восьми часов находилась под действием закиси азота, закончилась довольно удачно. В последующие недели она быстро восстановилась после операции. Однако примерно через шесть недель у нее начались проблемы с равновесием, она ощущала странное онемение конечностей и сильную слабость в теле. После того как она упала из-за неустойчивой походки и прошла обследование, у нее диагностировали острый дефицит B12, вызванный закисью азота. В качестве лечения врачи немедленно назначили инъекции высоких доз витамина. К счастью, в этом случае дефицит был выявлен достаточно рано. После 16 недель лечения из всех симптомов осталась только легкая усталость [110].
Эти и другие документально подтвержденные случаи пациентов, многие из которых не были вегетарианцами или веганами, показывают, насколько важно адекватное потребление витамина В12.
Примеры четко дают понять, что дефицит этого витамина может стать проблемой и для людей на смешанном питании, особенно если они и не подозревают о своем расстройстве всасывания или других нарушениях усвоения витамина.
Правильный тест для перестраховки
Существует четыре потенциальных биомаркера, с помощью которых можно определить уровень B12 в организме. Для лучшего понимания наиболее распространенных способов измерения необходимо знать несколько основных моментов. Как уже упоминалось ранее, в крови существует только один транспортный белок для B12, который фактически доставляет витамин в клетку, тем самым делая его биодоступным. Этот белок называется транскобаламин II (TКII), а его комплекс с B12 – голотранскобаламин II (голо-ТК). Он является единственной формой B12, которая усваивается клетками организма, производящими ДНК, поэтому его называют активным B12 [111].
Однако около 80 % циркулирующего в крови витамина не являются голотранскобаламином и, следовательно, биологически не активны [112].
Поэтому способы измерения, не учитывающие это важное различие, подходят для оценки запасов B12 лишь в очень ограниченной степени.
Определение концентрации витамина B12 в сыворотке крови (общий уровень витамина B12): если врач проводит анализ на концентрацию B12 без особых назначений, то, скорее всего, необходимо просто определить общий уровень витамина в крови. Это наиболее оптимальный и распространенный вид анализа на содержание витамина B12. Основная проблема заключается в том, что определяемое общее количество витамина B12 в сыворотке крови – это сумма активного голотранскобаламина II и неактивного, а, следовательно, неэффективного B12. Хотя общий уровень витамина B12 может служить приблизительным ориентиром, при неправильной интерпретации результаты могут ввести в заблуждение. Кроме того, при недостаточном поступлении в организм концентрация B12 в сыворотке падает гораздо медленнее, чем другие показатели. Поэтому этот вид анализа не позволяет выявить ранние стадии дефицита витамина B12 [113].
Голотранскобаламин II (голо-ТК): анализ на голотранскобаламин обеспечивает более точные результаты, чем тест на общий B12, поскольку с его помощью определяют только ту часть B12, которая связана с транспортным белком транскобаламином II и, следовательно, является активной. Если результаты определения уровня B12 в сыворотке крови весьма размыты, следует проводить именно этот анализ. Однако целесообразнее проводить его сразу вместо теста на общий витамин B12 или вместе с ним [114]. При недостаточном поступлении в организм витамина B12 уровень голотранскобаламина падает быстрее, чем общий уровень B12, что делает его лучшим маркером для ранней диагностики дефицита [115]. Однако лабораторный тест на голотранскобаламин можно проводить и с другой целью. Он быстро сигнализирует не только о недостаточном, но и о повышенном потреблении витамина. Поэтому у людей с адекватным всасыванием витамина его уровень может быстро увеличиться с началом приема добавок. Если этого не происходит, то можно говорить о мальабсорбции B12 [116].
Метилмалоновая кислота (ММК): поскольку при дефиците B12 скапливается метилмалоновая кислота (ММА), ее выведение с мочой может использоваться в качестве косвенного маркера недостаточного поступления B12. В отличие от общего анализа на B12 и анализа на голотранскобаламин, где высокие значения свидетельствуют об оптимальном поступлении витамина в организм, достаточность витамина B12 подтверждает пониженный уровень ММК. Анализ на уровень ММК представляется наилучшим способом определения количества B12 в клетках организма [117]. Однако с его помощью дефицит можно выявить уже на поздних стадиях, поэтому он не подходит в качестве профилактического маркера для ранней диагностики нехватки витамина. В одном исследовании у 30 испытуемых наблюдался очень низкий общий уровень B12, что свидетельствовало о явном дефиците витамина. Однако у них не было обнаружено повышенного уровня метилмалоновой кислоты [118]. Если бы дефицит можно было установить только на основе метилмалоновой кислоты и определенных симптомов, то было бы невозможно сделать это на ранней стадии. Однако по сравнению с гомоцистеином метилмалоновая кислота имеет то преимущество, что она не зависит от потенциального дефицита других витаминов. Поэтому повышенное значение метилмалоновой кислоты в анализе мочи почти наверняка указывает на дефицит именно B12 [119]. Метилмалоновую кислоту можно также измерить в сыворотке крови, однако анализ мочи является более показательным [120].
Гомоцистеин: гомоцистеин – это аминокислота, которая вырабатывается в организме из незаменимой аминокислоты метионина. В физиологических дозах гомоцистеин безвреден для нашего организма, однако в повышенных концентрациях он может оказывать токсическое воздействие на нервные клетки и сосуды. B12 участвует в расщеплении или превращении гомоцистеина обратно в метионин. Повышенный уровень гомоцистеина может указывать на дефицит B12. Поскольку в расщеплении гомоцистеина помимо B12 участвуют также фолиевая кислота (B9) и пиридоксин (B6), повышенный уровень гомоцистеина в принципе может указывать и на дефицит одного из этих двух других витаминов [121]. Определение гомоцистеина в крови проводят натощак [122]. Однако, как и ММК, гомоцистеин поздно реагирует на недостаток поступления витамина в организм и поэтому не подходит в качестве профилактического маркера для ранней диагностики [123]. Как и в случае с метилмалоновой кислотой, необходимо поддерживать низкий уровень гомоцистеина. Это важно для здоровья человека в целом, поскольку его повышенный уровень является независимым фактором риска сердечно-сосудистых заболеваний. Метаанализ 18 исследований показал, что каждое повышение уровня гомоцистеина на 5 мкмоль/л увеличивает риск сердечно-сосудистых заболеваний в среднем на 20 % [124]. Поэтому если исследования показывают, что веганы страдают сердечно-сосудистыми заболеваниями чаще ожидаемого, то это, среди прочего, можно объяснить увеличением уровня гомоцистеина в результате дефицита B12. В рамках исследования веганов в Германии (DVS) участники, придерживающиеся исключительно растительной диеты, демонстрировали более высокий уровень гомоцистеина, чем те, кто включал в свой рацион небольшое количество молока и яиц [125]. Однако это не значит, что молоко и яйца необходимы сами по себе. Это лишь показывает, что они обеспечивали хотя бы часть необходимого B12, который веганы должны были получать через пищевые добавки.
Если вы решите пройти один или несколько из вышеперечисленных анализов, то можете всегда оценить результаты с помощью референсных значений, приведенных в таблице 5.
Показатель крови – Референсное значение
Сыворотка крови (общий уровень витамина В12) – от 400 нг/л (нанограмм/литр)
Голотранскобаламин (голо-ТК) – от 50 пмоль/л (пикомоль/литр)
Метилмалоновая кислота – не более 271 нмоль/л (наномоль/литр)
Гомоцистеин – не более 12 мкмоль/л (микромоль/литр)
Дефицит B12 можно разделить на четыре стадии. В первой и второй стадии концентрация активного витамина B12 падает, что приводит к снижению уровня голотранскобаламина. Это, в свою очередь, должно рассматриваться как первый важный сигнал раннего предупреждения и призыв к действию. Однако большинство людей не замечают дефицита на этих этапах. На третьей стадии концентрации гомоцистеина и метилмалоновой кислоты постепенно увеличиваются. Как правило, также отсутствует явная симптоматика, хотя в этот период необходимо срочно ввести в рацион пищевые добавки в целях предотвращения последствий. Только на четвертой, заключительной стадии, когда запасы витамина B12 в организме уже сильно истощены, у большинства людей появляются некоторые из симптомов дефицита, о которых говорилось в предыдущем подразделе [128].
На рис. 13 представлен простой и понятный способ определения уровня B12 в организме. Можно начать с шага 1, определив общий уровень B12, и если результат неоднозначен, перейти к шагу 2, анализу на голотранскобаламин. Однако можно также начать непосредственно с шага 2 и, если результат неоднозначен, перейти к шагу 3, измерению концентрации метилмалоновой кислоты в моче. Кроме того, для подстраховки и экономии времени и образцов крови можно сдать сразу три анализа. Выбор варианта зависит также от текущего состояния здоровья, предыдущего опыта сдачи анализов и, в конечном итоге, от финансовых возможностей.
РИС. 13: АЛГОРИТМ ОПРЕДЕЛЕНИЯ УРОВНЯ B12 [129]

* Если общий уровень B12 находится в диапазоне 200–400 нг/л, его достаточность не может быть точно определена. Ситуацию помогут исправить последующие тесты: Holo-TC и MMA.
Наиболее часто измеряемым биомаркером уровня B12 является значение общего B12 в сыворотке крови. Однако его критикуют за слишком большие погрешности и неточность. Тем не менее это самый недорогой способ определения уровня B12, который, как правило, назначают в поликлинике по полису [130]. Даже если он дает не самые точные результаты, значение B12 в сыворотке крови не так уж маловажно, как принято считать. Если предельные значения, которые часто устанавливают слишком низкими, скорректировать в сторону увеличения, то уровень витамина в сыворотке крови может дать полезную информацию.
Как показано на рис. 13, общий уровень B12 в сыворотке крови более 400 нг/л считается надежным показателем достаточного наличия B12, даже несмотря на неточность метода измерения. В этом случае следует просто продолжать принимать добавки в целях профилактики. Однако в некоторых случаях для групп риска стоит провести дополнительный анализ на голотранскобаламин. Значения общего уровня B12 между 200 и 400 нг/л – это серая зона, и чем ближе показатель к 200 нг/л, тем более вероятен дефицит витамина в организме. В этом случае следует немедленно провести анализ на голотранскобаламин для дальнейшего уточнения, если он еще не проводился. Если общий уровень B12 в сыворотке крови ниже 200 нг/л, перед следующими анализами следует немедленно пополнить запасы B12. Пока организм не получит достаточное количество B12, с такими низкими показателями любой анализ на голотранскобаламин будет пустой тратой денег, поскольку дефицит B12 уже подтвержден на уровне 200 нг/литр.
После достаточного приема пищевых добавок необходимо проверить их эффективность.
Цена анализа на голотранскобаламин превышает стоимость теста на общий уровень B12, но дешевле теста на метилмалоновую кислоту. Поскольку этот анализ определяет только активный B12, он гораздо более точен. Кроме того, показатели активного B12 снижаются или повышаются гораздо быстрее, нежели общий уровень витамина. Если уровень голотранскобаламина превышает 50 пмоль/л, дефицит B12 маловероятен, и следует лишь продолжить прием пищевых добавок в целях профилактики. Однако при уровне ниже 35 пмоль/л дефицит весьма вероятен, и для его устранения следует немедленно повысить количество принимаемой добавки. Если значение находится в серой зоне от 35 до 50 пмоль/л, третий шаг – это измерение уровня метилмалоновой кислоты в моче для получения полной картины. Притом еще до анализа прием добавок следует продолжать или срочно начать. Этот тест является самым дорогостоящим, и не каждая лаборатория проводит его. Если уровень метилмалоновой кислоты ниже 271 нмоль/л, дефицит маловероятен. Если же результат выше 271 нмоль/л, то дефицит на лицо. Если есть основания полагать, что у обследуемого нарушены функции почек, то при повышенном уровне метилмалоновой кислоты это также лучше установить на основе показателей креатинина [131].
Анализ на гомоцистеин также предлагался в качестве способа определения уровня B12, однако из-за того, что на результаты влияет дефицит любого другого витамина группы В, он не так эффективен, как тесты на голотранскобаламин и ММК. В определенных случаях он вполне информативен, но лишь в очень ограниченной степени подходит в качестве единственного способа оценки уровня B12 без других лабораторных исследований.
Кроме того, можно упомянуть и пятый параметр, по которому иногда можно определить уровень B12 в организме: средний объем эритроцитов – MCV. Это один из нескольких показателей, используемых для диагностики анемии, которая, помимо прочего, может указывать на дефицит B12 [132]. При дефиците B12 и/или фолатов MCV растет. Увеличение MCV более чем на 100 фл (фемтолитров) называется макроцитозом [133]. Однако, поскольку на значение MCV влияют фолаты, витамин B12 и ряд других факторов, сам по себе этот параметр не показателен для определения уровня B12 в организме. Так как здоровые веганы часто потребляют большое количество фолатов с зелеными листовыми овощами, апельсинами, бобовыми и другими растительными продуктами, содержащими фолиевую кислоту, значение MCV может оставаться низким, несмотря на фактический недостаток B12, и таким образом маскировать возможный дефицит витамина [134].
Дыхательный тест для определения уровня B12 еще не получил широкого распространения, однако он также является очень перспективным. Этот анализ не только безболезненный, но и более дешевый и точный, чем общий анализ на B12 в сыворотке крови. Потенциально он может даже заменить его в будущем. Дыхательный тест на B12, представленный группой ученых из Флориды в 2011 году, измеряет объем выдыхаемого углекислого газа после приема пропионата натрия [135]. Это вещество в небольших количествах содержится в таких продуктах, как кофейные зерна, а наибольшая его концентрация – в зрелом сыре и моллюсках [136]. B12 расщепляет это вещество в организме, в результате чего в качестве продукта распада образуется углекислый газ. Чем меньше углекислого газа после приема пропионата натрия выдыхает испытуемый, тем ниже уровень B12, поскольку объем выдыхаемого углекислого газа пропорционален уровню B12 в организме [137].
Пищевые добавки: какие и сколько?
Первое, на что следует обращать внимание при выборе пищевой добавки, – это ее форма. Существует огромное разнообразие – это пастилки, капсулы, капли, зубная паста, жевательная резинка, назальные спреи, инъекции и различные обогащенные продукты питания. В большинстве случаев выбор способа приема B12 зависит от личных предпочтений, поскольку вышеперечисленные варианты подходят практически всем. Капли очень удобны для детей, которым еще трудно глотать таблетки. Те, кто склонен к забывчивости и поэтому не способен регулярно принимать пищевые добавки, могут выбрать зубную пасту с содержанием B12. Назальные спреи, жевательная резинка и некоторые другие формы добавок значительно реже встречаются в Германии, Австрии и Швейцарии, поэтому выбор в этом сегменте относительно невелик. Инъекции являются хорошим способом увеличить запасы B12 в организме в случаях острого, тяжелого дефицита из-за неспособности организма усваивать витамин естественным образом. Однако исследования показывают, что для подавляющего большинства людей таблетки или капли не менее эффективны. Кроме того, их прием гораздо быстрее и более приятен, нежели уколы [138].
Капсулы и пастилки чаще всего также являются более дешевым вариантом. Плюсы капель и пастилок заключаются в том, что поступающий с ними B12