2. ОБЩАЯ ХАРАКТЕРИСТИКА ОБЪЕКТОВ И МЕТОДОВ ИСПЫТАНИЯ ПИЩЕВЫХ ПРОДУКТОВ
2.1. Объекты испытаний
2.1.1. Состав и пищевая ценность продуктов питания
Пищевые продукты представляют собой сложные многокомпонентные системы, состоящие из сотен химических соединений. Эти соединения можно условно разделить на следующие 3 группы:
1. Соединения, имеющие алиментарное значение. Это необходимые организму нутриенты: белки, жиры, углеводы, витамины, минеральные вещества.
2. Вещества, участвующие в формировании вкуса, аромата, цвета, предшественники и продукты распада основных нутриентов, другие биологически активные вещества. Они носят условно не алиментарный характер. К этой группе относят также природные соединения, обладающие антиалиментарными (препятствуют обмену нутриентов, например, антивитамины) и токсическими свойствами (фазин в фасоли, соланин в картофеле).
3. Чужеродные, потенциально опасные соединения антропогенного или природного происхождения. Согласно принятой терминологии, их называют контаминантами, ксенобиотиками, чужеродными химическими веществами. Эти соединения могут быть неорганической и органической природы, в том числе микробиологического происхождения.
Важнейшим параметром пищевых продуктов является их качество, под которым понимают совокупность свойств продукта, обеспечивающих потребности организма человека в пищевых веществах, органолептические характеристики продукта, безопасность продукта для здоровья потребителя, надежность в отношении стабильности состава и сохранения потребительских свойств.
Важным показателем, относящимся к понятию качества пищевых продуктов, служит их пищевая ценность. Она отражает все полезные свойства пищевых продуктов, включая степень обеспечения физиологических потребностей человека в основных пищевых веществах и энергии. Пищевая ценность определяется химическим составом пищевого продукта с учетом его потребления в общепринятых количествах.
Пищевая ценность продуктов, в свою очередь, включает понятия энергетической ценности пищи (калорийности) и биологической ценности белков пищи. Энергетическая ценность или калорийность пищевых продуктов характеризуется количеством энергии, которая высвобождается из пищевых веществ в процессе биологического окисления и используется для обеспечения физиологических функций организма. Ориентировочно усвояемую энергию 1 г белков или углеводов принимают равной 16,7 кДж (4 ккал), а 1 г жиров – равной 37,7 кДж (9 ккал), хотя энергетическая ценность различных групп углеводов и жиров неодинакова.
Суточная норма калорий при активном образе жизни для мужчин – 3000 ккал, для женщин – до 2500 ккал.
Пищевая ценность продуктов характеризуется их:
– доброкачественностью (безвредностью);
– массовой долей пищевых веществ и биологически активных веществ, а также их соотношением;
– энергетической ценностью;
– органолептической ценностью;
– энергетической ценностью;
– физиологической ценностью.
На этикетке продукции указывается пищевая ценность, которая включает белки (вместе с аминокислотами), жиры и жирные кислоты, углеводы, витамины, минералы. Показатели указываются в граммах на порцию или на 100 гр. Энергетическая ценность указывается в калориях (ккал) и килоджоулях (кДж) тоже на порцию или на 100 гр. Также на этикетке должна присутствовать информация о процентных долях витаминов и минералов от их суточной нормы.
2.1.2. Классификация пищевых продуктов
1. Продукты растительного происхождения – это все те виды продуктов питания, что дарят нам именно растения (грибы и водоросли сюда не относятся). Среди них выделяют виды:
– фрукты;
– овощи;
– зерновые продукты;
– ягоды;
– орехи;
– травы;
– соки.
2. Продукты животного происхождения, богатые белками, жирами и витаминами:
– мясо и субпродукты;
– рыбные продукты;
– яйца;
– икра;
– молочные продукты;
– моллюски: кальмары, улитки, осьминоги.
3. Грибы
Этот вид продуктов питания необходимо вынести в отдельный список, поскольку сегодня учёные едины во мнении, что к растениям грибы не относятся. К их пищевым особенностям стоит отнести большое количество белков и углеводов, наличие витаминов и очень часто – сильных ядов, расщепляющихся только при приготовлении в условиях высокой температуры. В целом по степени усваивания грибы уступают большинству продуктов растительного и животного происхождения.
4. Водоросли
Они по многим свойствам близки к растениям, но имеют более примитивное строение. Из-за водного образа жизни имеют специфический состав, богаты углеводами и витаминами. Их главная особенность заключается в огромной биомассе, способной прокормить всё человечество, только вот добыть их сложнее, чем вырастить картошку на грядке.
5. Дрожжи и микроорганизмы
Они используются не как самостоятельный продукт питания, а как добавка, улучшающую другие изделия, используемые человеком в питании. Например, благодаря дрожжам мы получаем спирт и пышный хлеб, а молочнокислые бактерии сквашивают для нас молоко.
6. Неорганические продукты
К ним относятся различные виды солей, сахаров и минеральных компонентов, необходимым нам для нормального протекания всех химических реакций в организме или улучшения качества пищи.
7. Пищевые добавки
Пищевые добавки – вещества, добавляющиеся в технологических целях в пищевые продукты в процессе производства, упаковки, транспортировки или хранения для придания им желаемых свойств, например, определённого аромата (ароматизаторы), цвета (красители), длительности хранения (консерванты), вкуса, консистенции и т. п.
Международные стандарты на пищевые добавки и примеси определяются Объединенным комитетом экспертов Международной сельскохозяйственной организации (JECFA) и Кодексом Алиментариус (Codex Alimentarius), принятым Международной комиссией ФАО/ВОЗ и обязательным к исполнению странами, входящими в ВТО.
Пищевые добавки можно разделить на следующие категории:
– пищевые красители: добавки с индексом (E-100 – E-199) придают продуктам питания цвет, восстанавливают цвет продукта, утраченный при обработке. Могут быть естественными, как бета-каротин, или химическими, как тартразин;
– консерванты: добавки с индексом (E-200 – E-299) отвечающие за сохранность продуктов, предотвращая размножение бактерий или грибков, а также химические стерилизующие добавки для остановки созревания вин, дезинфектанты;
– антиоксиданты: добавки с индексом (E-300 – E-399) защищают продукты питания от окисления, прогоркания и изменения цвета. Представляют собой как природные соединения (аскорбиновая кислота, витамин Е), так и химически синтезированные соединения. Добавляют в жировые и масляные эмульсии (например, майонез);
– стабилизаторы: добавки с индексом (E-400 – E-499) сохраняют консистенцию продуктов, повышают их вязкость;
– эмульгаторы: добавки с индексом (E-500 – E-599) создают однородную смесь из несмешиваемых в природе веществ, таких как вода и масло, вода и жир;
– усилители вкуса и аромата: добавки с индексом (E-600 – E-699) усиливают вкус и аромат, могут скрывать неприятный естественный вкус продуктов питания;
– антифоминги (глазирующие агенты): добавки с индексом (E-900 – E-999) предотвращают образование пены, помогают достичь однородной консистенции продуктов;
– глазирователи, подсластители, разрыхлители, регуляторы кислотности и другие не классифицированные добавки: коды добавок в этой группе Е-1000 и более;
– ферменты, биологические катализаторы: добавки в диапазоне Е1100 – Е1105;
– модифицированные крахмалы: добавки в диапазоне Е1400 – Е1450, применяются для создания необходимой консистенции продуктов питания;
– химические растворители с кодами Е1510 – Е1520.
На комбинатах системы государственного резерва России, кроме продуктов питания, хранится хозяйственное мыло. Методы испытания качества хозяйственного мыла будут также рассмотрены в данном курсе лекций.
2.1.3. Характеристика безопасности пищевой продукции
Качество пищевой продукции – совокупность свойств, отражающих способность продукции обеспечивать органолептические характеристики, потребность организма в пищевых веществах, безопасность его для здоровья, надежность при изготовлении и хранении.
Медико-биологические требования к качеству пищевой продукции —комплекс критериев, определяющих пищевую ценность и безопасность продовольственного сырья и пищевой продукции.
Безопасность пищевой продукции – отсутствие токсического, канцерогенного, тератогенного, мутагенного или любого другого неблагоприятного действия пищевой продукции на организм человека при употреблении в общепринятых количествах. Безопасность гарантируется установлением и соблюдением регламентируемого уровня содержания загрязнителей химического, биологического и (или) природного происхождения.
Под тератогенным действием подразумевают аномалии в развитии плода, вызванные структурными, функциональными и биохимическими изменениями в организме матери и плода.
Мутагенным действием называют качественные и количественные изменения в генетическом аппарате организма. Различают два основных типа генетических повреждений – хромосомные и генные мутации. К мутагенным веществам относятся радиоактивные изотопы, радионуклиды и некоторые сильные химические вещества, относящиеся к группе отравляющих веществ.
Канцерогены – это вещества, которые при длительном воздействии (употреблении в пищу, вдыхании, попадании на кожу и т.д.) способны вызывать в организме человека возникновение злокачественных заболеваний.
Ксенобиотики (от греч. xenos – чужой и bios – жизнь) – любые чуждые для организма вещества (пестициды, токсины, поллютанты), способные вызвать нарушение биологических процессов. Попадая в среду жизни, ксенобиотики могут:
– вызвать аллергические реакции или гибель организмов;
– изменить наследственность;
– снизить иммунитет;
– исказить обмен веществ;
– нарушить естественный ход природных процессов в экосистемах, вплоть до уровня биосферы в целом;
– вызывать специфические заболевания.
2.1.4. Государственное регулирование качества и безопасности пищевой продукции
В Российской Федерации, с целью создания общих обязательных требований, обеспечивающих безопасность пищевых продуктов при их производстве и обращении, действует Технический регламент Таможенного союза «О безопасности пищевой продукции» ТР ТС 021/2011 (далее – ТР ТС).
Технический регламент Таможенного союза «О безопасности пищевой продукции» устанавливает:
– объекты технического регулирования;
– требования безопасности (включая санитарно- эпидемиологические, гигиенические и ветеринарные) к объектам технического регулирования;
– правила идентификации объектов технического регулирования;
– формы и процедуры оценки (подтверждения) соответствия объектов технического регулирования требованиям настоящего технического регламента.
При применении ТР ТС должны учитываться требования технических регламентов Таможенного союза и ЕАЭС, дополняющие и (или) уточняющие требования ТР ТС. В настоящее время в сфере обеспечения безопасности пищевой продукции приняты Технические регламенты Таможенного союза:
– ТР ЕАЭС 044/2017 «О безопасности упакованной питьевой воды, включая природную минеральную воду»;
– ТР ЕАЭС 040/2016 «О безопасности рыбы и рыбной продукции»;
– ТР ТС 034/2013 «О безопасности мяса и мясной продукции»;
– ТР ТС 033/2013 «О безопасности молока и молочной продукции»;
– ТР ТС 029/2012 «Требования безопасности пищевых добавок, ароматизаторов и технологических вспомогательных средств»;
– ТР ТС 027/2012 «О безопасности отдельных видов специализированной пищевой продукции, в том числе диетического лечебного и диетического профилактического питания»;
– ТР ТС 024/2011 «Технический регламент на масложировую продукцию»;
– ТР ТС 023/2011 «Технический регламент на соковую продукцию из фруктов и овощей»;
– ТР ТС 022/2011 «Пищевая продукция в части ее маркировки»;
– ТР ТС 015/2011 «О безопасности зерна»;
– ТР ТС 007/2011 «О безопасности продукции, предназначенной для детей и подростков»;
– ТР ТС 005/2011 «О безопасности упаковки».
Производственный контроль за соответствием пищевой продукции требованиям безопасности должны осуществлять предприятия-изготовители.
Надзор за безопасностью пищевой продукции и биологически активных добавок к пище осуществляется территориальными органами Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека.
2.1.5. Идентификация пищевой продукции как объекта технического регулирования
Для целей отнесения пищевой продукции к объектам технического регулирования, в отношении которых применяется технический регламент, заинтересованными лицами осуществляется идентификация пищевой продукции. Идентификация пищевой продукции проводится по ее наименованию и (или) ее признакам, изложенным в определении такой продукции в ТР ТС или в технических регламентах Таможенного союза на отдельные виды пищевой продукции, и (или) визуальным и (или) органолептическим, и (или) аналитическими методами.
Идентификация пищевой продукции проводится следующими методами:
– по наименованию – путем сравнения наименования и назначения пищевой продукции, указанных в маркировке на потребительской упаковке и (или) в товаросопроводительной документации, с наименованием, указанным в определении вида пищевой продукции в ТР ТС и (или) в технических регламентах Таможенного союза на отдельные виды пищевой продукции;
– визуальным методом – путем сравнения внешнего вида пищевой продукции с признаками, изложенными в определении такой пищевой продукции в ТР ТС и (или) в технических регламентах Таможенного союза на отдельные виды пищевой продукции;
– органолептическим методом – путем сравнения органолептических показателей пищевой продукции с признаками, изложенными в определении такой пищевой продукции в ТР ТС или в технических регламентах Таможенного союза на отдельные виды пищевой продукции. Органолептический метод применяется, если пищевую продукцию невозможно идентифицировать методом по наименованию и визуальным методом;
– аналитическим методом – путем проверки соответствия физико- химических и (или) микробиологических показателей пищевой продукции признакам, изложенным в определении такой пищевой продукции в ТР ТС или в технических регламентах Таможенного союза на отдельные виды пищевой продукции. Аналитический метод применяется, если пищевую продукцию невозможно идентифицировать методом по наименованию, визуальным или органолептическим методами.
Оценка (подтверждение) соответствия пищевой продукции требованиям ТР ТС и (или) технических регламентов Таможенного союза на отдельные виды пищевой продукции проводится в формах:
– подтверждения (декларирования) соответствия пищевой продукции;
– государственной регистрации специализированной пищевой продукции;
– государственной регистрации пищевой продукции нового вида;
– ветеринарно-санитарной экспертизы.
2.1.6. Причины загрязнения пищевой продукции
Основные причины загрязнения пищевой продукции:
– использование неразрешенных красителей, консервантов, антиокислителей или их применение в повышенных дозах;
– применение новых нетрадиционных технологий производства пищевой продукции или отдельных пищевых веществ, в том числе, полученных путем химического и микробиологического синтеза;
– загрязнение сельскохозяйственных культур и продуктов животноводства пестицидами, используемыми для борьбы с вредителями растений и в ветеринарной практике для профилактики заболеваний животных;
– нарушение гигиенических правил использования в растениеводстве удобрений, оросительных вод, твердых и жидких отходов промышленности и животноводства, сточных вод, осадков очистных сооружений и т.д.;
– использование в животноводстве и птицеводстве неразрешенных кормовых добавок, консервантов, стимуляторов роста, профилактических и лечебных медикаментов или применение разрешенных добавок и т. д. в повышенных дозах;
– миграция в продукты питания токсических веществ из пищевого оборудования, посуды, инвентаря, тары, упаковок, вследствие использования неразрешенных полимерных, резиновых и металлических материалов;
– образование в пищевых продуктах эндогенных токсических соединений в процессе теплового воздействия, кипячения, жарки, облучения, других способов технологической обработки;
– несоблюдение санитарных требований в технологии производства и хранения пищевых продуктов, что приводит к образованию бактериальных токсинов (микотоксины, батулотоксины и др.);
– поступление в продукты питания токсических веществ, в том числе радионуклидов из окружающей среды – атмосферного воздуха, почвы, водоемов.
2.1.7. Классификация загрязнения пищевой продукции ксенобиотиками химического и биологического происхождения
Классификация вредных и посторонних веществ в сырье, питьевой воде и продуктах питания представлена на рис. 2.1. Наибольшую опасность с точки зрения распространенности и токсичности имеют следующие контаминанты:
1. Токсические элементы (тяжелые металлы). Основной источник загрязнения – угольная, металлургическая и химическая промышленности.
2. Антибиотики получили распространение в результате нарушений их применения в ветеринарной практике. Остаточные количества антибиотиков обнаруживаются в 15 – 26% продукции животноводства и птицеводства. Методы контроля и нормативы разработаны только для нескольких применяемых препаратов. Обращает внимание большой уровень загрязнения левомицетином – одним из наиболее опасных антибиотиков.
3. Пестициды – это химические или биологические препараты, используемые для борьбы с вредителями и внешними паразитами растений, сорными растениями. Они накапливаются в продовольственном сырье и пищевых продуктах вследствие бесконтрольного использования химических средств защиты растений. Особую опасность вызывает одновременное наличие нескольких пестицидов, уровень которых превышает предельно – допустимые концентрации.
Таблица 2.1.
Загрязнители, подлежащие контролю в различных группах продовольственного сырья и пищевой продукции
4. Нитраты, нитриты, нитрозоамины. В настоящее время N – нитрозоамины встречаются практически во всех мясных, молочных и рыбных продуктах, при этом 36% мясных и 51% рыбных продуктов содержат их в концентрациях, превышающих гигиенические нормативы.
5. Диоксины и диоксиноподобные соединения – хлорорганические, особо опасные контаминанты, основными источниками которых являются предприятия, производящие хлорную продукцию.
6. Полициклические ароматические углеводороды образуются в результате природных и техногенных процессов.
7. Радионуклиды. Причиной загрязнения может быть небрежное обращение с природными и искусственными источниками радиации.
Определен перечень приоритетных загрязнителей, подлежащих контролю в различных группах продовольственного сырья и пищевых продуктов (табл. 2.1.).

2.1.8. Меры токсичности чужеродных химических веществ
На основе токсических критериев международными организациями – ВОЗ, ФАО и др., а также органами здравоохранения отдельных государств приняты базисные (основные) показатели – гигиенические нормативы. В большинстве случаев реализация того или иного эффекта зависит от концентрации. При повышении оптимальной физиологической концентрации элемента в организме может наступить интоксикация, а дефицит многих элементов в пище и воде может привести к достаточно тяжелым и трудно распознаваемым явлениям недостаточности.
Предельно-допустимая концентрация (далее – ПДК) – предельно-допустимые количества чужеродных веществ в атмосфере, воде, продуктах питания с точки зрения безопасности их для здоровья человека. ПДК в продуктах питания – установленное законом предельно-допустимое с точки зрения здоровья человека количество вредного чужеродного вещества. ПДК – это такие концентрации веществ, которые при ежедневном воздействии в течение сколь угодно длительного времени не могут вызывать заболеваний или отклонений в состоянии здоровья, обнаруживаемых современными методами исследований, в жизни настоящего и последующего поколений.
Допустимая суточная доза (далее – ДСД) – ежедневное поступление вещества, которое не оказывает негативного влияния на здоровье человека в течение всей жизни.
Допустимое суточное потребление (далее – ДСП) – величина, рассчитываемая как произведение ДСД на среднюю величину массы тела (60 кг).
Количественная характеристика токсичности веществ достаточно сложна и требует многостороннего подхода. Судить о ней приходится по результатам воздействия веществ на живой организм, для которого характерна индивидуальная реакция, индивидуальная вариабельность, поскольку в группе испытуемых животных всегда присутствуют более или менее восприимчивые к действию изучаемого токсина индивидуумы.
Существуют две основные характеристики токсичности: ЛД 50 и ЛД 100.
Летальная доза (далее – ЛД), т.е. доза вызывающая при однократном введении гибель 50% или 100% экспериментальных животных. Дозу обычно определяют в размерности концентрации. Токсичными считают те вещества, для которых ЛД мала. Принята следующая классификация веществ по признаку острой токсичности (ЛД 50 для крысы при пероральном введении, мг/кг):
Чрезвычайно токсичные ……………………..……менее 5
Высокотоксичные ………………………………………..5 —50
Умеренно токсичные ………………………………….50 —500
Малотоксичные ……………………………………….500 – 5000
Практически нетоксичные …………………. ……5000 – 15000
Практически безвредные …………………..……более 15000
Величина t0,5 характеризует время полувыведения токсина и продуктов его превращения из организма. Для разных токсинов оно может составлять от нескольких часов до нескольких десятков лет.
2.1.9. Показатели качества и безопасности пищевой продукции
Пищевая продукция, находящаяся в обращении на таможенной территории Таможенного союза в течение установленного срока годности при использовании по назначению должна быть безопасной.
Показатели безопасности пищевой продукции установлены в Приложениях к ТР ТС №№1, 2, 3, 4, 5 и 6. Показатели безопасности (кроме микробиологических) для пищевой продукции смешанного состава определяются по вкладу отдельных компонентов с учетом массовых долей и показателей безопасности для данных компонентов, установленных ТР ТС, если иное не установлено Приложениями к ТР ТС №№1, 2, 3, 4, 6 и (или) техническими регламентами Таможенного союза на отдельные виды пищевой продукции.
Безопасность пищевой продукции оценивается по гигиеническим нормативам, которые включают биологические объекты, потенциально опасные химические соединения, радионуклиды и вредные растительные примеси. Присутствие их в пищевых продуктах не должно превышать допустимых уровней содержания в заданной массе (объеме) исследуемой продукции. Указанные показатели безопасности установлены для 11 групп продуктов:
1. Мясо и мясопродукты, мясо птицы, яйца и продукты их переработки.
2. Молоко и молочные продукты.
3. Рыба, нерыбные продукты промысла и продукты, вырабатываемые из них.
4. Зерно (семена), мукомольно-крупяные и хлебобулочные изделия.
5. Сахар и кондитерские изделия.
6. Плодоовощная продукция.
7. Масличное сырье и жировые продукты.
8. Напитки.
9. Другие продукты.
10. Биологически активные добавки к пище.
11. Продукты детского питания.
Безопасность пищевых продуктов, как животного, так и растительного происхождения определяется, прежде всего, по микробиологическим показателям.
Во всех видах продовольственного сырья и пищевых продуктов нормируются токсичные элементы: свинец, мышьяк, кадмий, ртуть. Дополнительно к перечисленным элементам в консервированных продуктах (консервы из мяса мясорастительные; консервы из субпродуктов; консервы птичьи; консервы молочные; консервы и пресервы рыбные; консервы из печени рыб; консервы овощные, фруктовые, ягодные; консервы грибные; соки, нектары, напитки, концентраты овощные, фруктовые, ягодные в сборной жестяной или хромированной таре) нормируется олово и хром. Информация об анализируемых вредных и токсичных веществах приведена в таблице 2.2.
Во всех видах продовольственного сырья и пищевых продуктов нормируются так называемые «глобальные» пестициды: гексахлорциклогексан, ДДТ и его метаболиты; в рыбе и продуктах ее переработки дополнительно нормируются 2,4-Д-кислота, ее соли и эфиры; в зерне и продуктах его переработки – гексахлорциклогексан, ДДТ и его метаболиты, гексахлорбензол, ртутьорганические пестициды, 2,4-Д-кислота, ее соли и эфиры.

Радиационная безопасность продуктов животного и растительного происхождения определяется их соответствием допустимым уровням удельной активности радионуклидов цезия-137 и стронция-90.
В продуктах животного происхождения регламентируется содержание ветеринарных препаратов: стимуляторов роста животных антибиотиков (в том числе гормональных препаратов), лекарственных средств (в том числе антибиотиков), применяемых в животноводстве для целей откорма, лечения и профилактики заболеваний скота и птицы. При этом контроль за ветеринарными препаратами основывается на информации, представляемой изготовителем.
«МР 2.3.7.0168—20 Оценка качества пищевой продукции и оценка доступа населения к отечественной пищевой продукции, способствующей устранению дефицита макро- и микронутриентов. Методические рекомендации» в приложении 2 устанавливает Перечень рекомендуемых методов исследований для определения показателей качества пищевой продукции.
Перечень методов исследований для определения показателей безопасности пищевой продукции приведен в «Перечне стандартов, содержащих правила и методы исследований (испытаний) и измерений, в том числе правила отбора образцов, необходимые для применения и исполнения требований технического регламента «О безопасности пищевой продукции» (ТР ТС 021/2011).
Таблица 2.2
Вредные и токсичные вещества, анализируемые в пищевой продукции
2.2. Общие сведения о методах определения качества и безопасности пищевых продуктов
2.2.1. Сенсорные методы
Полноценность, пищевые и биологические свойства продуктов питания сохраняются при условии их высокого качества. Для определения доброкачественности применяются разнообразные методы: органолептические, химические, физические, микробиологические, биологические, радиометрические и др. Стандарты предусматривают те или иные методы исследования пищевых продуктов. Однако довольно сложно установить уровень качества, если его показатель не может быть измерен инструментально. Это особенно характерно для оценки качества по органолептическим показателям.
Качество продукта органолептическим методом определяется на основании ощущений человека. С помощью органов чувств (зрения, обоняния, осязания) проводится органолептический или сенсорный (лат. sensus – ощущение, чувство) анализ. Особенностью сенсорного анализа является то, что в роли прибора для измерения выступает сам человек, поэтому такая оценка по своей природе субъективна. Тем не менее, с помощью сенсорных методов оценки можно сделать достаточно точное заключение о качестве продукта без привлечения дорогостоящих приборов, оборудования и реактивов.
Объективность сенсорных исследований можно существенно повысить за счет обучения специалистов методам дегустационного исследования с использованием количественной оценки органолептических показателей по балльным шкалам при создании соответствующих условий для работ дегустаторов, обеспечении специалистов методическими материалами и др.
Сенсорные методы исследования позволяют довольно точно и с незначительными затратами средств и времени выявить имеющиеся недостатки пищевой продукции. Основываясь на знаниях сенсорики, можно получить необходимую информацию о качестве продуктов питания при разработке новых и изменении существующих рецептур, синтезе аналогов пищи и создании ароматизаторов, установить предел приемлемости продукта. Даже после полного перехода на инструментальные методы оценки качества органолептика остается посредником между прибором и чувственным восприятием свойств продукта потребителем.
В последнее время появились высокочувствительные приборы для изучения органолептических свойств продукции. Интеллектуальные сенсорные системы («электронный нос» и «электронный язык») созданы на основе неселективных сенсоров с последующей обработкой результатов измерений методом распознавания образов с применением искусственных нейронных сетей.
«Электронный язык» представляет собой аналитическое устройство для качественного и количественного анализа многокомпонентных растворов различной природы, состоящее из массива неспецифических химических сенсоров, обладающих перекрестной чувствительностью. Это означает, что каждый из них «запоминает» свой отклик на анализируемый объект, а все вместе они создают достаточно представительный его образ. Сложная программа, «обучившись» предварительно на эталонных объектах, позволяет сравнить результаты анализа с эталоном и выдать результат.
«Электронным носом» называют мультисенсорную систему распознавания компонентов газовых смесей, работающие на различных физических принципах (проводимость, приращение массы, измерение емкостных зарядов, флуоресценция и др.). Принцип работы прибора заключается в измерении электропроводности сенсоров при их взаимодействии с парами летучих веществ. В результате адсорбции молекул исследуемого вещества электропроводность чувствительных материалов сенсоров увеличивается. Величина отклика каждого сенсора из набора на разные газы должна быть индивидуальна. Математическая обработка данных сенсорного массива позволяет сформировать уникальный химический образ анализируемого объекта.
2.2.2. Качественный анализ
Качественный и количественный анализ являются предметом аналитической химии. Определение состава веществ включает выявление природы компонентов, из которых состоит исследуемое вещество, и установление количественных соотношений этих компонентов.
Сначала устанавливают качественный состав исследуемого объекта, т.е. решают вопрос, из чего он состоит, а затем приступают к определению количественного состава, т.е. узнают, в каких количественных соотношениях обнаруженные составные части находятся в объекте исследования.
Качественный анализ вещества можно проводить химическими, физическими, физико-химическими методами. Химические методы анализа основаны на применении характерных химических реакций для установления состава анализируемого вещества. Химический анализ вещества проводят двумя способами: «сухим путем» или «мокрым путем».
Анализ сухим путем – это химические реакции, происходящие с веществами при накаливании, сплавлении и окрашивании пламени.
Анализ мокрым способом – это химические реакции, протекающие в растворах электролитов. Анализируемое вещество предварительно растворяют в воде или других растворителях. В зависимости от массы или объема взятого для анализа вещества, от применяемой техники различают макро-, полумикро- и микрометоды.
Макрометод. Для проведения анализа берут 1—2 мл раствора, содержащего не менее 0,1 г вещества, и добавляют не менее 1 мл раствора реактива. Реакции проводят в пробирке, осадок отделяют фильтрованием. Осадок на фильтре промывают от примесей.
Полумикрометод. Для анализа берут в 10—20 раз меньше вещества (до 0,01 г). Так как в этом методе работают с малыми количествами вещества, то пользуются микропробирками, часовыми или предметными стеклами. Для отделения осадка от раствора применяют центрифугирование.
Микрометод. При выполнении анализа данным методом берут одну-две капли раствора, а сухого вещества – в пределах 0,001 г. Характерные реакции проводят на часовом стекле или фарфоровой пластинке.
При проведении анализа пользуются следующими операциями: нагревание и выпаривание, осаждение, центрифугирование, проверка полноты осаждения, отделение раствора центрифуга от осадка, промывание и растворение осадка.
2.2.3. Количественный анализ
Количественный анализ – совокупность химических, физико-химических и физических методов определения количественного соотношения компонентов, входящих в состав анализируемого вещества.
Для определения количественного состава вещества или продукта используются реакции нейтрализации, осаждения, окисления—восстановления, комплексообразования. Количество вещества можно определить по его массе или объему раствора, затраченного на взаимодействие с ним, а также по показателю преломления раствора, его электрической проводимости или интенсивности окраски и т. п.
Количественный анализ позволяет установить:
– количественные соотношения составных частей неизвестного индивидуального соединения, т.е. установить его формулу;
– содержание или концентрацию определяемого вещества в исследуемом образце;
– содержание всех или некоторых главных компонентов анализируемой смеси;
– содержание определенных форм того или иного элемента;
– содержание не главных компонентов смеси;
– содержание микропримесей в особо чистых веществах;
– содержание определенных радикалов, активных атомов, функциональных групп вещества, состав отдельных фаз смеси.
2.3. Методы количественного анализа
2.3.1. Классификация методов количественного анализа
Методами количественного анализа проверяют правильность технологических процессов, решают многие вопросы исследовательского и прикладного характера: оценивают содержание ценных веществ в биологических объектах, присутствие токсических веществ в продуктах питания, воде и т. д.
Методы количественного анализа являются измерительными методами, так как они базируются на информации, получаемой с использованием средств измерений и контроля. В основе всех методов анализа лежит измерение либо химического, либо физического свойства вещества, называемого аналитическим сигналом, зависящего от природы вещества и его содержания в пробе.
По количеству вещества, взятого для анализа, различают макро-, полумикро-, микро- и ультрамикрометоды количественного анализа. В макрометодах масса пробы составляет обычно> 100 мг, объём раствора> 10 мл; в ультрамикрометодах – соответственно 1—10—1 мг и 10—3—10-6 мл.
В зависимости от объекта исследования различают неорганический и органический количественный анализ. Органический количественный анализ подразделяется на элементный, функциональный и молекулярный анализ.
Элементный анализ позволяет установить содержание элементов (ионов).
Функциональный анализ – содержание функциональных (реакционноспособных) атомов и групп в анализируемом объекте.
Молекулярный количественный анализ предусматривает анализ индивидуальных химических соединений, характеризующихся определенной молекулярной массой.
Важное значение имеет фазовый анализ – совокупность методов разделения и анализа отдельных структурных (фазовых) составляющих гетерогенных систем.
Важная характеристика методов количественного анализа – точность, то есть значение относительной ошибки определения. Точность и чувствительность в количественном анализе выражают в процентах.
Точность химических методов количественного анализа находится обычно в пределах 0,005—0,1%; ошибки определения инструментальными методами составляют 5—10%, а иногда и значительно больше.
Точность физико-химических методов сильно колеблется в зависимости от метода. Наиболее высокой точностью (до 0,001%) обладает кулонометрия, основанная на измерении количества электричества, которое затрачивается на электрохимическое окисление или восстановление определяемых ионов или элементов. Большинство физико-химических методов имеют погрешность в пределах 2—5%, что превышает погрешность химических методов анализа. Однако, такое сравнение погрешностей не вполне корректно, так как оно относится к разным концентрационным областям. При небольшом содержании определяемого компонента (около 10—3% и менее) классические химические методы анализа вообще непригодны; при больших концентрациях физико-химические методы успешно соперничают с химическими методами. К числу существенных недостатков большинства физико-химических методов относится обязательное наличие эталонов и стандартных растворов.
Чувствительность некоторых методов количественного анализа приведена ниже (%):
Объёмный…10—1
Гравиметрический…10—2
Эмиссионный спектральный…10—4
Абсорбционный рентгеноспектральный…10—4
Масс-спектрометрический…10—4
Кулонометрический…10—5
Люминесцентный… 10—6—10-5
Фотометрический колориметрический…10—7—10-4
Полярографический…10—8—10-6
Активационный…10—9—10-8
Чтобы результаты количественного анализа были верны, необходимо соблюдать ряд условий:
– подбор подходящей аналитической реакции или физического свойства вещества;
– правильное выполнение всех аналитических процедур;
– применение достаточно надежных способов измерения результатов анализа.
В зависимости от принципа получения аналитического сигнала все количественные методы аналитической химии делятся на следующие основные группы:
1. Химические методы анализа основаны на использовании химических реакций. При этом проводят реакцию, а затем наблюдают аналитический эффект или измеряют аналитический сигнал. В качестве аналитического сигнала в химических методах выступает либо масса вещества (гравиметрический метод анализа), либо объем реактива – титранта (титриметрические методы). Химические методы применяют для определения состава и количества входящих в продукцию веществ. Они подразделяются на количественные и качественные – это методы аналитической, органической, физической и биологической химии.
2. Биологические методы анализа основаны на измерении интенсивности развития микроорганизмов в зависимости от количества анализируемого вещества. Биологические методы используют для определения пищевой и биологической ценности продукции. Их подразделяют на физиологические и микробиологические. Физиологические применяют для установления степени усвоения и переваривания питательных веществ, безвредности, биологической ценности. Микробиологические методы применяют для определения степени обсемененности продукции различными микроорганизмами.
3. Физические методы анализа основаны на измерении физических свойств веществ, зависящих от химического состава. Физические методы – методы, при реализации которых регистрируется аналитический сигнал каких-либо физических свойств (ядерные, спектральные, оптические) без проведения химической реакции. При этом наблюдение аналитического эффекта или измерение аналитического сигнала выполняют непосредственно с анализируемым веществом. Химические реакции либо совсем не проводят, либо они играют вспомогательную роль. Основной упор делают на измерение аналитического сигнала.
Физические методы применяют для определения физических свойств – коэффициента рефракции, вязкости, липкости и др. К таким методам относятся микроскопия, поляриметрия, колориметрия, рефрактометрия, спектроскопия, реология, люминесцентный анализ и другие. Также, с помощью физических методов определяют относительную плотность и удельную массу, температуру плавления и затвердевания, концентрацию водородных ионов, показатель преломления света, механическую устойчивость и прочность, эластичность и пористость, наличие примесей и другие показатели. В физических методах химические реакции отсутствуют или имеют второстепенное значение, хотя в спектральном анализе интенсивность линий всегда существенно зависит от химических реакций в угольном электроде или в газовом пламени. Поэтому иногда физические методы включают в группу физико-химических методов, так как достаточно строгого однозначного различия между физическими и физико-химическими методами нет, и выделение физических методов в отдельную группу не имеет принципиального значения.
4. Физико-химические методы анализа основаны на регистрации аналитического сигнала какого-то физического свойства (потенциала, тока, количества электричества, интенсивности излучения света или его поглощения и т. д.) при проведении химической реакции. При этом сначала проводят реакцию, а затем измеряют физическое свойство продукта реакции или используют измерение физического свойства в ходе реакции для установления конечной точки титрования.
Деление методов на физические и физико-химические часто условно, так как бывает трудно отнести метод к той или иной группе. Физические и физико-химические методы называют еще инструментальными методами анализа, поскольку они требуют использования специальной аппаратуры. Кроме того, деление методов на химические и инструментальные осуществляют на основе типа взаимодействия: в химических методах – взаимодействие вещества с веществом, в инструментальных – вещества с энергией. В зависимости от вида энергии в веществе происходит изменение энергетического состояния составляющих его частиц (атомов, молекул, ионов); при этом меняется физическое свойство, которое может быть использовано в качестве аналитического сигнала.
Физико-химические методы анализа стали применять позднее, чем химические методы анализа, когда была установлена и изучена связь между физическими свойствами веществ и их составом.
Химические методы анализа иначе называют классическими, а физические и физико-химические методы анализа – инструментальными, т. к., проведение анализа с привлечением этих методов невозможно без использования измерительной аппаратуры.
Применяемые в настоящее время инструментальные методы исследования состава и свойств пищевых продуктов основываются на использовании физических, химических, биохимических и других эффектов взаимодействия исследуемого объекта с первичными преобразователями (датчиками). Сигналы от датчиков воспринимаются вторичными приборами и преобразуются в информацию (табл. 2.3.)
Таблица 2.3.
Классификация инструментальных методов исследования состава и свойств вещества

По способам определения различают прямые и косвенные методы анализа. В прямых методах количество вещества находят непосредственным пересчётом измеренного аналитического сигнала в количество вещества (массу, концентрацию) с помощью уравнения связи. В косвенных методах аналитический сигнал используется для установления конца химической реакции (как своеобразный индикатор), а количество определяемого вещества, вступившего в реакцию, находят с помощью закона эквивалентов, т.е. по уравнению, непосредственно не связанному с названием метода.
По способу количественных определений различают безэталонные и эталонные инструментальные методы анализа.
Безэталонные методы основаны на строгих закономерностях, формульное выражение которых позволяет пересчитать интенсивность измеренного аналитического сигнала непосредственно в количестве определяемого вещества с привлечением только табличных величин. В качестве такой закономерности может выступать, например, закон Фарадея, позволяющий по току и времени электролиза рассчитать количество определяемого вещества в растворе при кулонометрическом титровании. Безэталонных методов очень мало, поскольку каждое аналитическое определение представляет собой систему сложных процессов, в которых невозможно теоретически учесть влияние каждого из многочисленных действующих факторов на результат анализа. В связи с этим при анализах пользуются определёнными приёмами, позволяющими экспериментально учесть эти влияния.
Наиболее распространённым приёмом является применение эталонов, т.е. образцов веществ или материалов с точно известным содержанием определяемого элемента (или нескольких элементов). При проведении анализа измеряют определяемое вещество исследуемого образца и эталона, сравнивают полученные данные и по известному содержанию элемента в эталоне рассчитывают содержание этого элемента в анализируемом образце. Эталоны могут быть изготовлены промышленным способом (стандартные образцы) или приготовляются в лаборатории непосредственно перед проведением анализа (образцы сравнения). Если в качестве стандартных образцов применяют химически чистые вещества (примесей меньше 0.05%), то их называют стандартными веществами.
На практике количественные определения инструментальными методами осуществляют по одному из трёх способов: градуировочной функции (стандартных серий), стандартов (сравнения) или стандартных добавок.
При работе по методу градуировочной функции с помощью стандартных веществ или стандартных образцов получают ряд образцов (или растворов), содержащих различные, но точно известные количества определяемого компонента. Иногда этот ряд называют стандартной серией. Затем проводят анализ этой стандартной серии и по полученным данным вычисляют значение чувствительности (в случае линейной градуировочной функции). После этого измеряют интенсивность аналитического сигнала в исследуемом объекте и вычисляют количество (массу, концентрацию) искомого компонента с помощью уравнения связи или находят по градуировочному графику.
Метод сравнения (стандартов) применим только для линейной градуировочной функции. Определение данного компонента проводят в стандартном образце (стандартном веществе), потом определяют в анализируемом объекте. Делением первого на второе вычисляют результат анализа.
Метод стандартных добавок применим тоже только к линейной градуировочной функции. В этом методе сначала проводят анализ навески исследуемого объекта, затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают результат.
К инструментальным методам, используемым для оценки качества пищевых продуктов, предъявляется ряд требований:
– высокая чувствительность;
– хорошая селективность и разрешающая способность;
– высокая точность и воспроизводимость;
– быстрота проведения анализа;
– широкая область проведения анализа;
– возможность одновременного определения нескольких веществ;
– простота подготовки проб;
– легкость и простота работы с приборами;
– максимальная автоматизация процессов подготовки пробы и измерения;
– возможность работы в производственных условиях;
– приемлемая стоимость прибора.
Результаты определений показателей инструментальными методами не зависят от индивидуальных особенностей исследователя, отличаются точностью и выражаются в количественных показателях (процентах, граммах и др.).
2.3.2. Общая характеристика химических методов анализа
Химические методы анализа широко используются в экспертизе для установления химического состава пищевых продуктов и их соответствия требованиям техническим нормативным правовым актам. Ими определяют показатели качества сырья, а также изменения, происходящие в пищевых продуктах при транспортировании, хранении и реализации. Это методы аналитической, органической и биологической химии, основанные на химических свойствах веществ, способности их принимать участие в какой-либо специфической химической реакции.
К классическим химическим методам количественного анализа относятся:
1. Гравиметрический анализ, основанный на определении измерения массы анализируемого вещества или его составных частей, выделяемых в химически чистом состоянии или в виде соответствующих соединений.
2. Объёмный анализ. Различают следующие виды объёмные методы анализа:
– титриметрический количественный анализ – измерение объёма израсходованного на реакцию реактива точно известной концентрации;
– газовый объёмный количественный анализ – анализ газовых смесей, основанный на избирательном поглощении из анализируемой газовой смеси определяемого компонента подходящими поглотителями;
– седиментационный объёмный количественный анализ основан на расслоении дисперсных систем под действием силы тяжести, сопровождающемся отделением дисперсной фазы в виде осадка и последующем измерении объёма осадка в градуированной центрифужной пробирке. Основными достоинствами химических методов анализа являются простота выполнения и достаточно высокая точность (0,10—0,01%).
К недостаткам химических методов анализа относятся большая продолжительность и высокий предел обнаружения.
Гравиметрический (весовой) метод является одним из наиболее точных и универсальных методов. Сущность его состоит в том, что определяемый компонент осаждается в виде малорастворимого соединения и после прокаливания взвешивается на аналитических весах (метод осаждения) или выделяется в чистом виде и взвешивается (метод выделения), или отгоняется при прокаливании или высушивании и по разности в весе до прокаливания и после него определяется содержание летучего компонента (метод отгонки).
В практике товароведения гравиметрический метод чаще всего применяется для определения гигроскопической влаги и летучих веществ в пищевых продуктах.
Титриметрический метод. Сущность титриметрического (объемного) анализа заключается в определении количества вещества путем измерения объема другого вещества, вступающего с анализируемым веществом в реакцию.
В зависимости от типа реакции, лежащей в основе количественного определения, титриметрический анализ подразделяется на ряд методов (нейтрализация, окисление-восстановление, осаждение).
К методу нейтрализации относятся все объемные определения, в основе которых лежит реакция нейтрализации (Н+ + ОН— = НОН). В практике товароведения этот метод применяется при определении кислотности пищевых продуктов.
К методам окисления-восстановления (оксидиметрии) относятся все объемные определения, в основе которых лежат окислительно-восстановительные реакции. В зависимости от применения рабочего раствора оксидиметрия делится на ряд методов:
– перманганатометрия, использующая окислительные свойства перманганата калия. В товароведной практике применяется для определения редуцирующих сахаров, нитритов, ионов металлов-восстановителей);
– йодометрия, использующая окислительно-восстановительные свойства пары I—/2I—. Этот метод применяется для определения концентра-ции сульфатов в сухих веществах или в растворе;
– дихроматометрия, использующая окислительные свойства бихромата калия.
В методах осаждения используются реакции, в результате которых образуются труднорастворимые соединения. В товароведной практике для определения содержания поваренной соли в пищевых продуктах чаще всего применяют метод Мора, согласно которому раствор хлорида натрия титруют раствором нитрата серебра в присутствии индикатора хромата калия с образованием труднорастворимого соединения серебра – аргентометрия.
Комплексонометрия относится к методам комплексообразования, основанных на применении реакции образования прочных комплексных соединений. Реакция комплексообразования – взаимодействие ионов металла с молекулами или ионными частицами, имеющими по меньшей мере один атом с неподеленной парой электронов, т.е. с веществами, являющимися донорами электронов. Наибольшее значение из методов комплексонометрии имеет трилонометрия, которая широко применяется для количественного определения щелочноземельных металлов, жесткости воды, микроэлементов в пищевых продуктах.
2.3.3. Общая характеристика физических методов анализа
В исследованиях качества пищевых продуктов чаще всего применяются оптические и реологические методы.
К оптическим методам относятся рефрактометрический и поляриметрический методы.
В основе рефрактометрии лежит способность сред преломлять проходящие через них лучи света. В товароведении рефрактометрический анализ применяют для определения количества сухих веществ в пиве, томатных продуктах, варенье, джеме, соках; содержания жира в продуктах и сахаров в сахарных сиропах и др. Для измерения показателей преломления используются рефрактометры и интерферометры.
Поляриметрический метод основан на измерениях, связанных с поляризацией света. Метод широко используется в пищевой промышленности. В сахарной промышленности его применяют для определения сахаристых веществ, в масложировой промышленности – для идентификации масел. Поляриметрический метод анализа проводится с помощью поляриметра.
Реологические методы применяются не только для изучения физических величин и расчета движения продуктов в рабочих органах машин, но и для оценки ряда технологических, в том числе и качественных, показателей продуктов, управления ими и получения заранее заданных технологических характеристик (упругой вязкости теста, липкости мясного фарша, прочности макаронных изделий, сахара-рафинада, вязкости майонеза и др.).
Для измерения сдвиговых характеристик продуктов применяются ротационные вискозиметры, капиллярные вискозиметры Оствальда и Убеллоде, пенетрометры.
Поверхностные свойства – адгезия и внешнее трение – измеряются при помощи адгезиометров, которые предназначены для тестовых продуктов, кондитерских масс, колбасного (мясного) фарша.
К физическим методам относится также метод определения температурных констант. Его проводят при исследовании качества жиров, установления их природы, чистоты, отсутствия примесей.
2.3.4. Общая характеристика физико-химических методов анализа
По виду энергии возмущения и измеряемого свойства (аналитического сигнала) физико-химические методы анализа можно классифицировать следующим образом (табл. 2.4.).

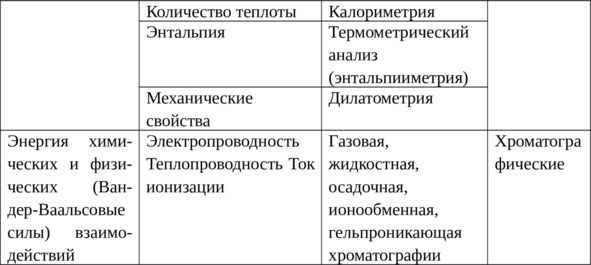
Кроме перечисленных в таблице существует множество других частных физико-химических методов анализа, не подпадающих под данную классификацию.
Физико-химические методы характеризуются быстротой выполнения анализа, высокой степенью точности и малым количеством пробы при анализе.
Из фотометрических методов для исследования качества продуктов сырья и пищевых продуктов применяют метод сравнения оптических плотностей стандартного и исследуемого окрашенных растворов с использованием фотоэлектроколориметра, цветометрический метод с применением спектроколориметра, трансформационную инфракрасную спектрометрию с Фурье-преобразователем и др.
Колориметрия предназначена для определения концентрации вещества в растворе по поглощению света. Этим методом устанавливают содержание аммиака, нитратов и нитритов в мясных продуктах; альдегидов, сивушных масел и фурфурола – в спирте; меди и олова – в консервах; железа, некоторых витаминов, величину рН – в продуктах; содержание антоцианов – в виноградных винах; кофеина – в чае и кофе; теобромина – в какао и др.
Таблица 2.4
Классификация физико-химических методов анализа пищевой продукции
Цветометрический метод предназначен для оценки цвета продо-вольственных товаров при их идентификации, экспертизе, разработке новых продуктов питания. Для отдельных товаров цвет нормируется действующими стандартами. По цвету пищевых продуктов можно судить об их свежести, ингредиентном составе, наличии или отсутствии фальсификации. Оценка цвета позволяет выявить дефекты сырья и нарушение технологии производства.
Спектрофотометрия основана на тех же законах светопоглощения, что и фотоколориметрия, но в этом методе используется поглощение света определенной длины волны. Метод характеризуется высокой точностью.
Инфракрасная спектроскопия служит для определения состава и чистоты продукта или сырья. Полученные спектры сопоставляют со спектральными таблицами различных соединений. В настоящее время применяется более прогрессивная технология – Фурье-преобразование инфракрасного спектра.
Нефелометрия основана на определении количества света, рассеянного частицами суспензии. Этим методом устанавливают степень мутности раствора с помощью нефелометра.
Люминесцентный анализ основан на том, что при облучении ультрафиолетовыми лучами пищевых продуктов, не обработанных или обработанных специальными реактивами, некоторые составные их части выделяют лучистую энергию разных оттенков. Этот анализ предназначен для определения некоторых витаминов, содержания белков и жиров в молоке, исследования свежести мяса и рыбы, диагностики порчи овощей, плодов и обнаружения в продуктах консервантов, канцерогенных веществ, пестицидов. С его помощью можно обнаружить в исследуемом образце присутствие вещества в концентрации 10—11 г/г.
Атомно-абсорбционный спектральный анализ основан на резонансном поглощении световой энергии свободными атомами анализируемых веществ, возникающем при пропускании пучка света через слой атомного пара. Метод атомной абсорбции обеспечивает рекордно низкие пределы обнаружения по многим элементам (в 1 см3 раствора пробы можно определить содержание элемента в диапазоне 10—12—10—4 г). Атомно-абсорбционный спектральный анализ применяется для определения тяжелых металлов при проведении сертификации продовольственного сырья и пищевых продуктов. Используют однолучевые и двухлучевые атомно-абсорбционные спектрофотометры фирм Hitachi, Varian, Bekman, Techtron, Perkin-Elmer.
Для контроля качества продовольственных товаров также широко используются электрохимические методы. Наиболее распространенным для анализа водных экстрактов пищевых продуктов и воды является потенциометрический (ионометрический) метод. Этот метод широко используется для измерения рН, по величине которого можно судить о свежести мяса, молока, соков и других продуктов, а также для количественного определения нитратов в свежей продукции растениеводства. Метод привлекает простотой, быстротой выполнения, возможностью вести определения в мутных и окрашенных средах.
Для количественного определения антиоксидантов в пищевых продуктах наиболее надежным представляется амперометрический метод. В условиях амперометрического детектирования возможен предел в интервале 10—9—10—12 г, а иногда и на уровне 10—15 г. В комбинации с высокоэффективной жидкостной хроматографией этим методом определяют содержание полифенолов в пищевых продуктах и напитках.
Хроматографические методы широко применяются при оценке пищевых продуктов, проведении сертификационных испытаний. Это наиболее эффективные методы разделения и анализа сложных смесей веществ. Они основаны на различии в распределении компонентов смеси между двумя фазами. Одна из фаз – это неподвижный слой твердого вещества или жидкости с большой поверхностью, другая фаза – подвижная – поток жидкости или газа, фильтрующегося через неподвижный слой. Процесс состоит из повторения большого числа элементарных актов сорбции (поглощения) – десорбции (выделения). Поскольку скорость сорбции и десорбции хоть немного, но отличается, то после повторения большого числа элементарных актов происходит разделение смеси на отдельные компоненты.
Существуют различные способы классификации хроматографических методов:
1. В зависимости от выбранного типа подвижной и неподвижной фаз – газовая, жидкостная хроматография.
2. В зависимости от механизма распределения веществ между подвижной и неподвижной фазами – адсорбционная, распределительная, ионообменная, осадочная, аффинная, эксклюзивная, молекулярная и хемосорбционная хроматография.
3. По технике выполнения – колоночная, плоскостная (бумажная и тонкослойная), капиллярная, хроматография в полях (электрических, магнитных и др.).
4. В зависимости от цели проведения хроматографического процесса – аналитическая, неаналитическая, препаративная, промышленная хроматография.
Надежным способом исследования липидов, аминокислот, нуклео-тидов, сахаров, витаминов, алкалоидов и других соединений служит тонкослойная хроматография.
С помощью газовой хроматографии можно разделить смеси на отдельные компоненты и определить их количественное содержание. Применяется она для обнаружения токсичных примесей (мышьяка, свинца, кадмия, алюминия и др.) в продовольственном сырье и пищевых продуктах.
Жидкостная хроматография высокого разрешения (высокоэффективная жидкостная хроматография) является компьютеризированным методом, позволяющим определить активные вещества и их соотношение с точностью до миллионных долей. Разновидностью жидкостной хроматографии, основанной на обмене ионов раствора на ионы твердой фазы, является ионообменная хроматография с кондуктометрическим детектированием. Метод широко используется для решения биохимических проблем в научных исследованиях. Для практических целей ионообменную хроматографию применяют для анализа аминокислот.
Для анализа применяют хроматографы различных марок и произ-водителей: «Цвет» (Россия), «Хром» (Чехия), Varian (США), SEC-3000 (Италия).
2.4. Выбор метода анализа и отбор пробы
2.4.1. Выбор метода анализа
Физико-химические методы анализа пищевой продукции позволяют сделать окончательный вывод о безопасности пищевой продукции и оценить ее пищевую ценность. Наибольшее распространение в испытательных лабораториях получили оптические, потенциометрические, хроматографические и радиологические методы. Выбор наилучшего метода анализа диктуется многими соображениями и представляет трудную задачу. Имеет значение химический состав анализируемого образца, оснащенность лаборатории необходимой аппаратурой, наличие соответствующих реактивов и многое другое. В том случае, если концентрация определяемого компонента мала, для анализа пригодны адсорбционные, электрофотометрические и кинетические методы.
При выборе метода важное значение имеют такие параметры, как точность анализа, время, затрачиваемое на подготовку к проведению анализа, количество анализируемых проб.
Предел обнаружения – минимальное содержание определяемого компонента в анализируемой пробе, которое может быть обнаружено данным методом с заданной вероятностью. Чаще всего предел обнаружения выражают в процентах или приводят его абсолютное значение в нанограммах (10—9 г). При расчете предела обнаружения применяемого метода учитывают аналитический сигнал холостой пробы (фон), чувствительность метода, минимальное значение аналитического сигнала, который может быть зарегистрирован прибором в данном методе.
Реально определяемые концентрации элементов на один-два порядка выше предела обнаружения. Поэтому важной характеристикой метода является диапазон определяемых концентраций, т. е. интервал содержания компонента, в котором возможно его определение данным методом. Наименьшее значение концентрации называют нижним пределом определяемых содержаний (Сн), а максимальное значение – верхним пределом (Св).
Физико-химические методы анализа сложных материалов состоят из следующих этапов:
1 – отбор пробы для анализа;
2 – разложение пробы и переведение ее в раствор;
3 – проведение химической реакции, при которой на определяемый компонент Х воздействуют реагентом Р, в результате чего образуется продукт реакции П;
4 – измерение какого-либо физического параметра продукта реакции, реагента или самого определяемого вещества. На основе этого измерения судят о количестве или о содержании определяемого компонента в анализируемом материале.
2.4.2. Общие требования по отбору и упаковке пробы
Порядок отбора проб для анализа установлен «Правилами отбора образцов (проб) для проведения исследований (испытаний) и измерений пищевой продукции при применении и исполнении требований технических регламентов Евразийского экономического союза» (приложение к Рекомендации Коллегии Евразийской экономической комиссии от 31.07. 2018 г. №13).
Отбор образцов (проб) производится в соответствии с требованиями, устанавливающими методы отбора и испытаний, в количестве, необходимом для проведения исследований (испытаний) и измерений.
Процедура проведения отбора образцов (проб) включает в себя:
– отбор образцов (проб);
– оформление сопроводительной документации (акт отбора образцов);
– транспортирование отобранных образцов (проб).
При отборе каждая проба индивидуально упаковывается таким образом, чтобы исключить возможность подмены содержимого. Упаковка должна обеспечить неизменность свойств отобранной пробы в соответствии с рекомендациями изготовителя на всем протяжении транспортирования и проведения испытаний.
При отборе проб пищевых продуктов, методики исследования которых установлены соответствующими нормативными документами (ГОСТ, ОСТ, ТУ, СТО), следует руководствоваться указаниями раздела «Отбор проб», а в случае отсутствия – специальным стандартом по правилам отбора проб.
Перед отбором проб продуктов специалист, который будет проводить отбор, должен ознакомиться с имеющейся на данную партию продукта документацией (накладные, сертификаты и т.п.) и произвести наружный осмотр всей партии, обращая внимание на состояние тары (исправность, деформации, загрязнение и т.п.), внешний вид продукта, условия хранения.
После осмотра партии производится вскрытие отдельных единиц упаковки и выемка проб для исследования в лаборатории.
Порядок отбора проб пищевых продуктов включает в себя: выделение однородной партии, определение числа и отбор точечных проб (при необходимости), составление объединенной пробы и формирование из нее средней пробы, которая направляется на лабораторные испытания.
Значения массы точечных проб продуктов и необходимое количество проб зависят от требуемого значения массы объединенной пробы, при расфасовке в мелкую потребительскую тару (бутылки, пакеты, пачки и т.п.) эти фасовки рассматривают как точечные пробы.
Массу (объем) пробы продукта устанавливают в соответствии с нормативно – технической документацией на конкретный вид продукции, и она должна быть достаточной для проведения испытаний. Пробы в виде коробок, банок, плиток, пачек и др. завертывают в плотную бумагу. Пробы, отобранные от весовых продуктов в транспортной таре: ящиках, мешках, контейнерах и др., помещают в чистые сухие банки с притертыми стеклянными или хорошо пригнанными резиновыми крышками, или заворачивают в пергамент, целлофан, полимерную пленку, одноразовые мешочки или упаковывают в пластмассовые коробки с крышками. Пробы, требующие особых условий хранения (при пониженных температурах) – скоропортящиеся продукты, помещают в сумку-холодильник или обкладывают сухим льдом.
Отобранные пробы транспортируют в соответствии с условиями, установленными в нормативно – технической документации на конкретный вид продукции. В процессе транспортирования пищевых продуктов следует соблюдать меры предосторожности, чтобы предотвратить воздействие неприятных запахов, прямого солнечного света и других неблагоприятных условий. Температура хранения после отбора проб должна быть достигнута как можно быстрее. В отдельных случаях для лучшей сохранности проб возможно их консервирование, если это не противоречит требованиям нормативной документации на продукцию или методики выполнения измерений. Пробы замороженных продуктов укладывают в сумки-холодильники, обеспечивающие сохранение проб в замороженном состоянии. Пробы скоропортящихся продуктов транспортируют при температуре плюс 5°С не более 6 час, за исключением продуктов, на которые предусмотрены специальные условия согласно нормативно—технической документации на конкретный вид продукции. Отобранные пробы маркируются, заполняется сопроводительная документация, в которой указывается наименование образца, масса (объем), время и место отбора, условия отбора и транспортировки, ставятся подписи специалистов, проводивших отбор проб и представителей заказчика.
2.4.3. Отбор пробы газов
Смеси газов гомогенны, поэтому генеральная проба может быть относительно небольшой и ее отбор не представляет трудностей. Пробу газа отбирают, измеряя его объем при помощи вакуумной мерной колбы или бюретки с соответствующей запорной жидкостью; часто конденсируют газ в ловушках разного типа при низких температурах. В замкнутой емкости (например, цех предприятия) пробу газа отбирают в разных точках, объемы газа смешивают или анализируют отдельно каждую пробу.
При отборе пробы из потока газа используют метод продольных струй и метод поперечных сечений. Метод продольных струй применяют, когда состав газа вдоль потока не меняется. Если состав газа вдоль потока меняется, то пробы берут на определенных расстояниях (часто через специальные отверстия в трубах) вдоль потока. Поскольку состав анализируемых газов часто меняется во времени в зависимости от состояния атмосферы, температуры в помещениях и других условий, то пробы усредняют или анализируют отдельно объемы газов, отобранные в разное время.
2.4.4. Отбор пробы жидкости
Пробу гомогенной жидкости отбирают при помощи соответствующих пипеток, бюреток и мерных колб из общей емкости после тщательного перемешивания. При анализе большого объема жидкости отбор пробы проводят на разной глубине и в разных местах емкости. Для отбора проб на разной глубине используют специальные пробоотборные устройства – батометры различной конструкции (цилиндрический сосуд вместимостью 1—3 л, закрывающийся сверху и снизу крышками). Отбор гомогенной жидкости из потока проводят через определенные интервалы времени и в разных местах.
Пробы гетерогенных жидкостей отбирают не только по объему, но и по массе. В одних случаях жидкость гомогенизируют, в других – добиваются полного ее расслоения. Гомогенизацию проводят, изменяя температуру, перемешивая жидкость или подвергая ее вибрации. Если гомогенизировать жидкость невозможно, то ее расслаивают и отбирают пробу каждой фазы, используя при этом специальные пробоотборники с большим числом забирающих камер. Размер генеральной пробы жидкости обычно невелик и не превышает нескольких литров или килограммов.
При отборе проб (образцов) воды следует руководствоваться действующими нормативными документами на методы отбора проб воды.
Метод отбора проб выбирают в зависимости от цели испытаний и перечня определяемых показателей с таким расчетом, чтобы исключить (свести к минимуму) возможные изменения определяемого показателя в процессе отбора пробы. Методы отбора, подготовки к определению состава и свойств, транспортирования и хранения проб воды должны обеспечивать неизменность состава проб в интервале времени между отбором проб и их испытанием.
Пробы воды для проведения физико-химических исследований отбирают в емкости, изготовленные из химически стойкого стекла с притертыми пробками или из полимерных материалов, разрешенных для контакта с водой. Перед отбором пробы емкости для отбора проб не менее 2-х раз ополаскивают водой, подлежащей анализу, и заполняют ею емкость до верха. При отборе проб, подлежащих хранению, перед закрытием емкости пробкой верхний слой воды сливают так, чтобы под пробкой оставался слой воздуха и при транспортировании пробка не смачивалась.
2.4.5. Отбор пробы твердых веществ
При отборе генеральной, лабораторной и анализируемой пробы твердых веществ оптимальная масса проб обусловлена неоднородностью анализируемого объекта, размером частиц, с которых начинается неоднородность, и требованиями к точности анализа, обычно определяемой погрешностью в отборе пробы.
Способы отбора генеральной пробы твердого вещества различны для веществ, находящихся в виде целого (банки, пачки и др.) или сыпучего продукта. При пробоотборе от целого твердого объекта необходимо учитывать, что он может быть неоднороден, поэтому при отборе пробы его либо дробят, если вещества хрупкие, либо распиливают через равные промежутки, либо высверливают в разных местах образца.
При отборе пробы сыпучих продуктов массу исследуемого объекта перемешивают и пробу отбирают в разных местах емкости и на разной глубине, используя при этом специальные щупы-пробоотборники.
Генеральная (первичная, большая, грубая) проба отбирается непосредственно из анализируемого объекта в количестве от 1 до 60 кг. Из генеральной пробы путем ее сокращения отбирают лабораторную пробу (от 1 до 25 кг). Одну ее часть используют для предварительных исследований, другую – для арбитражных анализов, третью – непосредственно для анализа (анализируемая проба). В случае необходимости пробу измельчают и усредняют. После отбора генеральной (или лабораторной) пробы твердого вещества осуществляют процесс гомогенизации, включающий операции измельчения и просеивания. Пробы, содержащие крупные куски, разбивают в дробильных машинах и мельницах разного типа, меньшие частицы измельчают в шаровых мельницах и специальных ступках. Для тонкого измельчения используют фарфоровые, агатовые, яшмовые и кварцевые ступки с пестиками из такого же материала.
Для проведения анализа берут так называемую среднюю (представительную) пробу. Это небольшая часть анализируемого объекта, средний состав и свойства которой должны быть идентичны во всех отношениях среднему составу и свойствам исследуемого объекта. Различают генеральную, лабораторную и анализируемую пробы.
Для анализируемой пробы проводят несколько определений компонента: из отдельных навесок 10—1 000 мг (если анализируемый объект твердое вещество) или аликвот (если анализируемый объект – жидкость или газ). Анализируемая проба должна быть представительной, но не очень большой.
При отборе пробы необходимо учитывать следующее: агрегатное состояние анализируемого объекта (способы отбора различны для газов, жидкостей и твердых веществ); неоднородность анализируемого материала; размер частиц, с которых начинается неоднородность; требуемую точность оценки содержания компонента во всей массе анализируемого объекта в зависимости от задачи анализа и природы исследуемого объекта. Необходимо учитывать возможность изменения состава объекта и содержания определяемого компонента во времени (например, изменение концентрации компонентов в пищевых продуктах).
Во избежание потерь в процессе измельчения периодически отделяют крупные частицы от мелких частиц просеиванием и растирают их отдельно. Операции измельчения и просеивания чередуют до тех пор, пока не получат достаточно растертую однородную пробу.
Следующий этап отбора пробы – усреднение, включающее операции перемешивания и сокращения пробы. Перемешивание проводят механически в емкостях, перекатыванием из угла в угол на различных плоскостях. Сокращение пробы проводят способами квартования, шахматного отбора и механического делителя.
Способ квартования заключается в том, что проба, отобранная из различных ящиков, мест и т. п., смешивается, рассыпается ровным слоем, делится накрест на 4 части (квартуется), из них две противоположные удаляются, а две оставшиеся вновь перемешиваются и снова делятся на 4 части. Так поступают, пока количество материала не уменьшится до необходимого для анализа. Степень сокращения может быть определена заранее на основании расчета величины генеральной и анализируемой проб.
2.4.6. Потери и загрязнения при отборе и хранении пробы
В процессе отбора и хранения пробы возможны потери определяемого компонента, внесение загрязнений, изменение химического состава, что приводит к увеличению общей погрешности анализа. Потери в виде пыли можно в заметной степени уменьшить просеиванием пробы при измельчении. Другой возможный источник ошибок при отборе и хранении пробы – потеря летучих продуктов вследствие изменения температурного режима при хранении или разогрева при измельчении твердых образцов. Большие потери могут быть также вследствие адсорбции определяемого компонента на поверхностях емкостей для отбора и хранения пробы.
Состав анализируемого объекта может меняться за счет проходящих в нем химических реакций (разложения компонентов, окисления их при взаимодействии с атмосферным кислородом). Например, концентрация пестицидов в растениях, почве и пищевых продуктах со временем значительно понижается вследствие их химических превращений. Погрешности, обусловленные внешними загрязнениями, особенно велики при определении примесей компонентов, их следовых количеств. Поэтому при растирании образцов используют ступки из особо твердых материалов и хранят пробы в посуде из особых сортов стекла или полиэтилена. Например, пробы воды для определения кремния отбирают только в полиэтиленовые бутыли. При определении органических соединений предпочтительнее посуда из стекла.
В отдельных случаях для сохранения определяемого компонента его экстрагируют органическими растворителями или адсорбируют на различных твердых веществах. Пробы можно стабилизировать на несколько часов охлаждением до 0ºС и на несколько месяцев – резким охлаждением до минус 20ºС. Для консервирования определяемых компонентов добавляют разные консерванты (кислоты, образующие комплексные соединения вещества и др.). Хранят пробы в условиях, гарантирующих постоянство их состава в отношении тех компонентов, которые предполагается определять.
2.5. Подготовки пробы к анализу
2.5.1. Высушивание пробы
Подготовка пробы зависит от природы анализируемого объекта и от способа измерения аналитического сигнала.
При подготовке пробы к анализу можно выделить три основные стадии:
– высушивание;
– разложение (чаще с переведением пробы в раствор);
– устранение влияния мешающих компонентов.
Анализируемый образец содержит, как правило, переменное количество воды. Это может быть химически несвязанная вода, например, адсорбированная на поверхности пробы твердого вещества, сорбированная щелями и капиллярами аморфных веществ (крахмал, белок), окклюдированная полостями твёрдых веществ.
Анализируемый объект может также содержать химически связанную воду. Это может быть кристаллизационная вода (например, в соединениях BaCl2 2H2O, CaSO4·2H2O, Na2B4O7·10H2O) или конституционная вода, выделяющаяся в результате разложения вещества при нагревании. Часть химически связанной воды может теряться в процессе отбора и хранения пробы.
Для установления состава объекта и получения воспроизводимых результатов необходимо удалить влагу из образца, высушив его до постоянной массы. Чаще всего анализируемый образец высушивают на воздухе или в сушильных шкафах при температуре от +105ºС до +120ºС в течение 1—2 ч или в эксикаторах над влагопоглощающими веществами (прокаленный хлорид кальция, фосфорный ангидрид). Длительность и температуру высушивания образца, зависящих от его природы, устанавливают заранее методом термогравиметрии.
Содержание воды определяют гравиметрически косвенным или прямым методом. В косвенном методе о содержании воды судят по потере массы анализируемой пробы при ее высушивании или прокаливании. Прямой гравиметрический метод основан на поглощении выделившейся из образца воды подходящим поглотителем. О содержании воды судят по увеличению массы предварительно взвешенного поглотителя.
Для определения воды также применяют титриметрический метод, газожидкостную хроматографию и инфракрасную спектроскопию.
2.5.2. Разложение пробы
Процесс разложения (вскрытия) пробы заключается в переводе анализируемой пробы в удобное для анализа агрегатное состояние или соединение. Для перевода пробы в раствор в химических методах, ее непосредственно обрабатывают жидкими растворителями (водой, кислотами, щелочами) или переводят в соединения, способные растворяться, путём разрушения прокаливанием, сожжением, сплавлением с плавнями или другими способами. В физических методах перевод вещества в необходимое для анализа состояние (например, газообразное) обычно производится воздействием потока энергии (искры, индукционно-связанной плазмы, электрического тока и др.)
Способы разложения делят на сухие и мокрые. К сухим относят термическое разложение, сплавление и спекание с различными веществами (солями, оксидами, щелочами и их смесями), к мокрым – растворение анализируемой пробы в различных растворителях.
Растворитель в мокром способе должен растворять пробу быстро, в достаточно мягких условиях и не мешать на последующих стадиях анализа. Лучшим растворителем является вода. Для растворения органических соединений применяют органические растворители (спирты, хлорированные углеводороды, кетоны). В отдельных случаях используют смесь воды и смешивающегося с ней органического растворителя (например, смесь воды и этанола).
При мокром способе разложения пробы часто применяют различные кислоты высокой степени очистки и их смеси при нагревании с использованием сосудов из соответствующего (инертного к кислотам) материала. Лучшим растворителем для многих металлов является соляная кислота. Для ускорения разложения кислотами иногда используют катализаторы (например, ферменты). Для обеспечения разложения веществ, не взаимодействующих с реагентами при обычной температуре и давлении, растворение проб часто проводят в автоклавах.
Выбор сухого способа разложения (сплавление, спекание и термическое разложение) определяется задачей анализа, природой разлагаемого вещества, выбранным методом определения компонентов, наличием необходимой аппаратуры.
Сплавление как метод разложения пробы сухим способом чаще используют при анализе неорганических веществ.
При сплавлении тонко измельченный образец перемешивают с 8—10-кратным избытком реагента (плавня) и нагревают при температуре от +300°С до +1 000°С до получения прозрачного сплава. Сплавление считается законченным, когда масса в тигле становится совершенно однородной, прозрачной и легкоподвижной. После охлаждения застывшую массу растворяют в воде или кислотах. При сплавлении используют щелочные, кислые и окислительные плавни.
Спекание – это взаимодействие веществ при повышенной температуре в твердой фазе, основанное на высоком химическом сродстве компонентов пробы к введенным реагентам, на диффузии и реакциях обмена. В отдельных случаях спекание позволяет провести разложение пробы быстрее и проще, способствует уменьшению количества загрязнений, поскольку при этом часто используют
Таблица 2.5 Температура озоления некоторых материалов
(определение общей зольности)
меньший (двух- или четырехкратный) избыток реагентов и менее высокие температуры. Спекание проводят обычно со смесью карбонатов щелочных металлов и оксидов магния, кальция или цинка. Рекомендуется использовать спекание при разложении проб силикатов, сульфидов, оксидов металлов.
Сухое озоление (термическое разложение, сожжение) наиболее распространено при вскрытии проб органического происхождения в токсикологическом анализе следовых содержаний примесей металлов. Сухое сожжение органических веществ проводят под действием кислорода воздуха или кислорода из баллона. Большинство пищевых продуктов сгорает при температуре от +550°С до +600 °С (таблица 2.5).
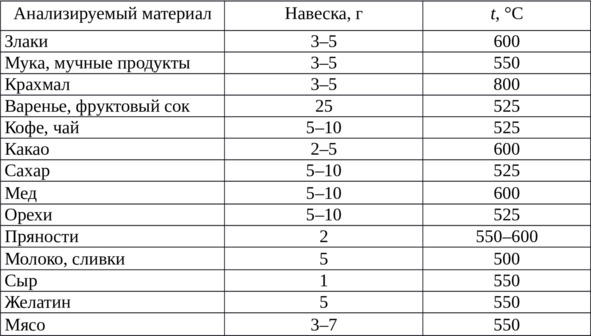
Преимуществом сухого озоления является простота аппаратуры (термопечи и тигли), минимум внимания оператора, отсутствие загрязнений от реактивов; недостатком – возможность потерь легколетучих элементов (Hg, As, Se, Те), взаимодействие с материалом тигля и длительность процесса. Широкое распространение получило сухое сожжение с озоляющими добавками (окислители, разбавители, плавни, вещества, препятствующие улетучиванию элементов).
Сухой способ используют тогда, когда мокрый способ не дает удовлетворительных результатов, поскольку возрастает вероятность и величина погрешностей, особенно при сплавлении.
Пиролиз – процесс термического разложения в отсутствие веществ, реагирующих с разлагаемым соединением. При пиролизе органических веществ характеристические фрагменты органических соединений появляются главным образом в интервале от +300°С до +700 °С. Неорганические вещества разлагаются, как правило, при температурах от +1 000°С до +1 500 °С.
Пиролиз желательно проводить в атмосфере инертного газа (азот, гелий) или в вакууме при большой скорости нагрева. Его проводят различными способами: прокаливают пробу в тигле или небольшой лодочке в печи, наносят образец на металлическую проволоку или спираль и нагревают их до нужной температуры, помещают вещество в вакуумированную или заполненную инертным газом стеклянную или кварцевую трубку и также нагревают ее до необходимой температуры. Кроме того, применяют облучение лазером, потоком электронов высокой энергии, нагревание смеси пробы с ферромагнитным материалом (например, с порошком железа) в высокочастотном электрическом поле и т. д.
Пиролиз чаще используют при анализе органических веществ, особенно полимеров. Газообразные продукты пиролиза определяют различными аналитическими методами (газовая хроматография, ультрафиолетовая (УФ-) и инфракрасная (ИК-) спектроскопия, масс-спектрометрия).
Высокоэффективным способом окислительной минерализации является разложение образцов с помощью низкотемпературной кислородной плазмы, предполагающее пропускание газообразного кислорода под давлением 133—665 Па через высокочастотное электрическое поле. Этот способ успешно используют для определения Zn, Cd, Pb и Cu методом дифференциальной инверсионной вольтамперометрии наряду с методом мокрого озоления в смеси хлорной и азотной кислот. Достоинствами метода являются отсутствие опасности загрязнения пробы материалом сосуда или реагентами, а также селективность (отделение органической части от неорганической), что важно при анализе почв, медико-биологических образцов, объектов животного и растительного происхождения.
При микроволновом разложении пробы источником тепла для мокрой минерализации веществ является энергия микроволнового (МВ) излучения (300—30 000 МГц), приводящая к быстрому разогреву всего объема образца, поглощающего МВ-энергию. В результате вместо 1—2 ч для полного разложения проб кислотой требуется 10—15 мин, а температура кипения достигается в течение 2 мин.
Современные способы измерения температуры и давления непо-средственно в МВ-печи позволили определить температуры разложения основных компонентов пищевых продуктов азотной кислотой под давлением (углеводы – 140°С, белки – 150°С, жиры – 160°С). Достаточно 10 мин для полного разложения азотной кислотой всех компонентов пищевых продуктов. Использование МВ-печей позволяет автоматизировать процесс подготовки пробы и значительно ускорить ход анализа. При разложении различных проб в микроволновом поле в большинстве случаев используют смесь (НNО3 +H2O2).
Использование ультразвука в подготовке пробы. При ультразвуковой (УЗ) обработке пробы происходит дробление частиц, увеличение поверхности перемешивания, образование эмульсий с большой поверхностью контакта. УЗ-обработка в подготовке проб пищевых продуктов и объектов окружающей среды применяется для перемешивания и измельчения материалов.
Фотохимическая подготовка пробы широко используется при определении органических веществ, углерода, азота и фосфора, присутствующих в воде. За последние годы увеличилось применение ультрафиолета в подготовке проб биологических объектов и пищевых продуктов. Особое место занимает УФ-минерализация органических веществ в катодной адсорбционной вольтамперометрии.
Электрохимический метод подготовки пробы основан на том, что в присутствии обычно хлорид-ионов ведется прямое анодное окисление органических веществ либо косвенное их окисление через реакции с частицами генерированных окислителей. Преимуществом этого метода является минимальное загрязнение проб из-за отсутствия окисляющих реактивов и возможность совмещения подготовки пробы с определением тяжелых металлов. Данный метод эффективен при обработке проб, содержащих органические вещества в малых количествах, например, в природных водах.
Экстракция. Для извлечения из проб пищевых продуктов органических веществ используется экстракция – процесс распределения вещества между двумя или более несмешивающимися фазами. С целью усиления экстракции в одну из фаз экстракционной системы вносят экстрагент. При анализе пищевых продуктов в качестве экстрагентов используют воду, спирты, бензол, ацетон, дихлорметан и др. Выбор экстрагента зависит от природы пищевых продуктов. Экстракционный способ имеет недостаток – необходимость отгонки значительных объемов растворителя, что может привести к потерям веществ, особенно летучих или образующих с растворителем азеотропные смеси.
Жидко-жидкостная экстракция (далее – ЖЖЭ) – классический способ извлечения пестицидов из водных образцов при использовании дихлорметана. В настоящее время появилась микроЖЖЭ – экстракция из большого объема воды (400 мл) очень малым объемом растворителя (500 мкл), которая применяется для подготовки пробы для анализа методом газовой хроматографии без стадии испарения, что важно для определения высоколетучих соединений. В сравнении с твердофазной экстракцией данный метод подготовки пробы является более быстрым и дешевым.
Твердофазная экстракция применяется при анализе природных вод, пестицидов и продуктов их распада. Ее преимущества – экономия времени и растворителей, исключение опасности образования эмульсий, возможность выделения следовых количеств аналита и автоматизации.
Сверхкритическая жидкостная экстракция является относительно новым методом, применяемым для извлечения веществ с помощью специальных экстрагентов – «сверхкритических» жидкостей (жидкие СО2, NH3, пропан, бутан и др.). Сверхкритическая жидкостная экстракция используется для анализа пестицидов в почвах, тканях растений и животных.
2.5.3. Устранение влияния мешающих компонентов
Большинство аналитических методов недостаточно селективны (избирательны), т. е. обнаружению и количественному определению данного вещества могут мешать другие вещества, присутствующие в анализируемом объекте. Для устранения этого мешающего влияния используют методы разделения анализируемой смеси или выделения из нее определяемого вещества. Разделение заключается в разъединении анализируемой смеси на группы веществ, одна из которых, кроме определяемого вещества, должна содержать только те компоненты смеси, которые не мешают анализу. Если это не помогает, то применяют выделение определяемого вещества. Оно основано на извлечении этого вещества из смеси в чистом виде или в виде соединения известного химического состава.
В случае, когда концентрация определяемого вещества меньше предела обнаружения данного метода или меньше нижней границы его рабочего диапазона, то применяют концентрирование определяемого вещества.
Концентрирование – это повышение отношения концентрации (или количества) определяемого микрокомпонента к концентрации (или количества) макрокомпонента. Различают абсолютное и относительное концентрирование. При абсолютном концентрировании определяемое вещество собирают в меньшем объеме или массе анализируемой смеси, а при относительном – выделяют из смеси так, чтобы отношение его концентрации к концентрации не отделившихся примесей увеличилось.
Для разделения, выделения и концентрирования используют химические, физические и физико-химические методы.
Из химических методов, в основном, применяют маскирование, осаждение и соосаждение.
Маскирование заключается в связывании мешающих ионов в малодиссоциированные, в основном, комплексные соединения, или перевод их в другую форму (например, изменением степени окисления) без удаления из анализируемого раствора, поскольку в таком состоянии они не мешают определению данного вещества. Для маскировки широко применяют добавление в анализируемый раствор таких комплексообразователей, как органические кислоты (лимонная, уксусная, винная, щавелевая и др.), комплексоны, а также неорганические соединения, например, фториды, цианиды и др.
Осаждение основано на выделении одного или нескольких ионов или веществ в виде малорастворимого соединения. Осаждение применяют для разделения элементов в химическом анализе и в химической технологии. Разделение осаждением основано на различной растворимости соединений, преимущественно в водных растворах.
Соосаждение – это захват посторонних веществ (примесей) осадком основного вещества (макрокомпонентом). При этом, примеси не образуют собственной твердой фазы, а лишь соосаждаются за счет выделения на поверхности осадка основного вещества (адсорбция) или распределения по объему осадка в процессе его образования (окклюзия), или образования совместной кристаллической решетки с макрокомпонентом (изоморфизм), или образования химического соединения с ним (хемосорбция). Осадок основного вещества называют носителем или коллектором.
Коллекторы – это органические или неорганические вещества, которые должны полностью захватывать нужные вещества и не захватывать мешающие микрокомпоненты и компоненты основного вещества.
В качестве неорганических коллекторов используют гидроксиды, сульфиды, фосфаты и др., т. е. преимущественно соединения, образующие аморфные (некристаллические) творожистые осадки с большой развитой поверхностью. Например, в качестве коллектора при анализе кадмия высокой чистоты используют оксид марганца (IV), позволяющий соосадить примеси As, Bi, Ga, In, Ni, Pb, Sb, Sn, Te, Ti.
Среди органических коллекторов различают в основном три вида:
– малорастворимые ассоциаты, состоящие из объемистого органического катиона и аниона (например, катион кристаллического фиолетового или метиленового синего, или тиоцианат-ион);
– хелаты (дитиокарбаминаты, дитизонаты, b-дикетоны и др.);
– органические индифферентные соединения, которые не содержат комплексообразующих групп.
В качестве физических методов используют методы испарения: отгонку, перегонку (дисцилляцию), возгонку (сублимацию) и др.
Отгонка (выпаривание) – это одноступенчатый процесс разделения и концентрирования. При выпаривании удаляются вещества, которые находятся в форме готовых летучих соединений, ими могут быть и основа, и примеси, причем последние отгоняют реже. Выпаривание проводят разными способами, например, нагреванием снизу (с помощью водяной бани) или сверху (под инфракрасной лампой). В первом случае потери могут достигать до 50— 70%, во втором – меньше. Распространена отгонка с предварительным химическим превращением, как основы, так и примесей, в легколетучие соединения в результате химических реакций.
Один из таких методов – сжигание органических и биологических проб (сухая и мокрая минерализация). Сухую минерализацию проводят путем сжигания вещества в трубчатых печах в атмосфере воздуха или кислорода. Образующиеся летучие соединения CO, CO2, N2, SO2, SO3, H2O и другие улавливают с помощью адсорбционных систем и определяют. Мокрую минерализацию проводят в растворах анализируемых веществ, получая легколетучие соединения добавлением концентрированных кислот, их смесей или сильных окислителей (H2O2, KClO3, KMnO4 и др.).
Перегонка (дистилляция) – разделение жидких смесей на фракции различных составов путем их частичного испарения с последующей конденсацией образовавшихся паров. Разделение основано на различии температур кипения жидкостей, составляющих данную смесь. Используют при анализе органических и неорганических смесей.
Возгонка (сублимация) – это перевод вещества из твердого в газообразное состояние, минуя жидкую фазу. К возгонке прибегают, когда разделяемые компоненты трудно плавятся или растворяются. Использование метода ограничено небольшим числом сублимирующихся веществ.
В качестве физико-химических методов применяют экстракцию, сорбцию, ионный обмен, хроматографию и различные электрохимические методы, например, электролиз, электрофорез, электродиализ и др.
Экстракция – это процесс извлечения одного или нескольких веществ из раствора путем добавления к нему другого растворителя, значительно лучше растворяющим извлекаемые вещества, но не смешивающимся с первым растворителем. Разделение основано на различной растворимости веществ в различных растворителях. Экстракцию широко используют для разделения смесей элементов.
Сорбция – это процесс поглощения газов, паров и растворенных веществ твердыми или жидкими поглотителями на твердом носителе (сорбентами). В качестве поглотителей используют различные высокопористые вещества: активные (активированные) угли, силикагель, диатомовую землю, желеобразные гели с различным размером пор между их частицами, а также различные органические поглотители (цеолиты). Сорбция веществ может происходить на поверхности сорбента (адсорбция), или всем его объемом (абсорбция), или путем образования химических соединений между материалом сорбента и разделяемыми веществами (хемосорбция).
Активированные угли получают при действии на уголь неактивных паров H2O или CO2 при 850—950 С0. При этом часть угля выгорает и получается активированный уголь, пронизанный порами с радиусом менее 1 нм. Активные угли используют в качестве эффективных сорбентов для извлечения Pb из атмосферного воздуха; Ca, Ba, Sr из концентрированных растворов солей, щелочей и других соединений; Cr, Mo, V из воды и др.
Силикагель – это высушенная кремниевая кислота:
Ионный обмен основан на разделении смеси ионов с помощью твердых веществ – ионитов, способных обменивать свои ионы на ионы раствора, который пропускают через слой ионита. Обмен ионами может происходить как в гомогенном растворе, так и в гетерогенной системе. Под ионным обменом понимают гетерогенный процесс, посредством которого осуществляется обмен между ионами, находящимися в растворе и в твердой фазе, называемой ионитом или ионообменником.
В зависимости от того, какие ионы подвижны, иониты делят на катиониты и аниониты. Катиониты содержат неподвижные анионы и обмениваются катионами, для них характерны кислотные свойства – подвижный ион водорода или металла. Например, катионит RSO3-H+ (здесь R – структурная основа с неподвижной функциональной группой SO3– и противоионом Н+). По виду содержащихся в катионите катионов его называют Н-катионитом, если все его подвижные катионы представлены только водородом, или Na-катионитом, Са-катионитом и т. п. Их обозначают RH, RNa, R2Ca, где R – каркас с неподвижной частью активной группы катионита. Широко используются катиониты с неподвижными функциональными группами —SO3-, —РО32-, —СОО-, —AsO32- и др.
Аниониты содержат неподвижные катионы и обмениваются анионами, для них характерны основные свойства – подвижный гидроксид-ион или ион кислотного остатка. Например, анионит RN (CH3) 3+OH-, с функциональной группой —N (CH3) 3+ и противоионом ОН-. Анионит может быть в разных формах, как и катионит: ОН-анионит или ROH, SO4-анионит или RSO4, где R – каркас с неподвижной частью активной группы анионита. Наиболее часто применяют аниониты с неподвижными группами – [N (CH3) 3] +, – [N (C5H5) 3] +, NH3+NH, + и др.
Хроматография – это совокупность методов разделения и анализа смесей с помощью подвижной и неподвижной фаз хроматографической системы, которые не смешиваются друг с другом. Разделение основано на различном сродстве компонентов смеси к этим фазам, а за счет этого – на различной скорости перемещения компонентов в потоке подвижной фазы относительно слоя неподвижной фазы.
Электролиз – это совокупность методов разделения и анализа растворов электролитов, основанная на протекании в нем окислительно-восстановительной реакции под действием пропускаемого через электролит электрического тока, с выделением продуктов электролиза на электродах. Разделение основано на различной способности веществ выделяться на электродах, в зависимости от величины тока или напряжения электролиза.
Электрофорезом называется движение заряженных диспергированных (раздробленных) частиц в жидкости под действием электрического поля. Разделение основано на различной подвижности частиц различных веществ в электрическом поле постоянного тока.
Электродиализ – это ускоренная форма диализа, основанного на разделении растворенных частиц, значительно различающихся между собой размерами и массой, с помощью полупроницаемой мембраны. При электродиализе скорость движения частиц через мембрану задается электрическим полем. Для его создания по обе стороны мембраны помещаются электроды, на которые подается внешнее напряжение. Например, с помощью электродиализа можно отделить примеси электролитов от чистого растворителя, используя мембрану проницаемую для ионов электролита.
В большинстве методик по испытанию пищевой продукции изложены методы отбора и подготовки проб.
2.6. Примеры применения разных способов подготовки пробы для проведения анализа качества пищевых продуктов
2.6.1. Способ сухой минерализации проб
ГОСТ 26929—94 устанавливает порядок проведение подготовки пробы разными способами минерализации для определения содержания токсичных элементов в сырье и пищевых продуктах.
Подготовка к минерализации
Способ сухой минерализации основан на полном разложении органических веществ путем сжигания пробы сырья или продуктов в электропечи при контролируемом температурном режиме и предназначен для всех видов сырья и продуктов, кроме животных, растительных жиров и масел.
Непосредственно перед использованием лабораторную посуду обрабатывают горячим раствором азотной кислоты (1:1), затем ополаскивают дистиллированной водой, обрабатывают горячим раствором соляной кислоты (1:1), ополаскивают 3—4 раза дистиллированной водой, затем 1—2 раза бидистиллированной или деионизированной водой и сушат. Обработку горячим раствором кислоты проводят следующим образом: посуду помещают в термостойкий химический стакан вместимостью 1000 см3, заливают раствором кислоты, нагревают до кипения и отключают подогрев. Выдерживают до полного охлаждения и промывают, как указано выше.
Вместо обработки посуды одним из растворов кислот допускается выдерживание чаш или тиглей с раствором уксусной кислоты на кипящей водяной бане в течение 1 ч.
Продукты, содержащие углекислый газ (пиво, шипучие и игристые вина, минеральные воды, газированные напитки и соки), освобождают от него.
При анализе пива колбу вместимостью 1000 см3 на треть заполняют пивом (температура продукта должна быть комнатной), закрывают пробкой с отверстием, в которое вставлена трубка, и встряхивают в течение 20—30 мин.
При анализе вина, минеральной воды, газированных соков и напитков в пробе продукта, помещенного в колбе с тубусом, создают вакуум при помощи водоструйного или масляного насоса в течение 2—3 мин до исчезновения пены и появления больших пузырей на поверхности жидкости.
В чашу (чашку, тигель) берут навеску продукта из подготовленной к испытаниям пробы. Необходимый объем жидкого продукта отмеряют пипеткой. Значения массы навески (или объема пробы) указаны в таблице 1 ГОСТ 26929—94.
Минерализация проб для определения содержания меди, свинца, кадмия, цинка, хрома, никеля, алюминия, а также железа методом атомно-абсорбционной спектрофотометрии
При содержании в продукте до 20% влаги чашу с навеской помещают на электроплитку и проводят осторожно обугливание, не допуская сильного дымления. После прекращения выделения дыма чашу помещают в электропечь, отрегулированную ранее на температуру около 250°С.
При содержании влаги в продукте от 20 до 80% чашу с навеской помещают на кипящую водяную баню или в сушильный шкаф (доводя его температуру до 150°С), или на электрическую плитку и удаляют влагу. Затем осторожно обугливают содержимое чаши на газовой горелке или электрической плитке до прекращения выделения дыма, не допуская сильного дымления, воспламенения и выбросов. Чашу помещают в электропечь, отрегулированную ранее на температуру около 250°С, а продукцию, содержащую более 20% сахаров, помещают в электропечь, отрегулированную ранее на температуру около 150°С.
При содержании в продукте влаги более 80% навеску в чаше обрабатывают следующим образом:
– винодельческие продукты упаривают досуха на водяной бане и помещают в электропечь;
– пиво, минеральную воду, безалкогольные напитки и плодоовощные соки и напитки на электроплитке упаривают досуха и проводят обугливание до прекращения выделения дыма, затем помещают в электропечь, отрегулированную на температуру около 150°С;
– в навеску жидких молочных продуктов (молока, кисломолочных продуктов и молочных консервов) добавляют раствор азотной кислоты из расчета 1 см3 на 50 г продукта, перемешивают, помещают на электроплитку и осторожно проводят обугливание до прекращения выделения дыма, затем чашу помещают в электропечь, отрегулированную ранее на температуру около 250°С.
Для интенсификации процесса обугливания рекомендуется:
а) одновременно обогревать чашу с навеской продукта инфракрасной лампой;
б) в чашу с навеской добавить этиловый спирт из расчета 5 см3 на 1 г сухого вещества, закрыть часовым стеклом и выдержать 24—48 ч, затем проводить обугливание;
в) для проб продуктов, содержащих более 20% сахаров (варенье, джем и др.), а также темноокрашенных соков и компотов добавить к навеске раствор серной кислоты (1:9) из расчета 5 см3 на 1 г сухого вещества, закрыть часовым стеклом и выдержать 48 ч, затем проводить обугливание;
г) для проб продуктов, содержащих 20—60% жира (сыр, масличные семена, жмых, шрот и белковые продукты), в навеску добавить раствор азотной кислоты (1:1) из расчета 1—1,5 см3 на каждые 10 г навески, выдержать 15 мин, затем проводить обугливание.
После окончания обугливания минерализацию проб проводят в электропечи, постепенно (на 50°С через каждые 30 мин) повышая температуру до 450°С. Продолжают минерализацию при этой температуре до получения серой золы. Допускается минерализация зерна и зернопродуктов при температуре 500°С.
Чашу с золой вынимают из электропечи через 10—15 ч озоления, охлаждают до комнатной температуры и смачивают содержимое по каплям минимальным количеством раствора азотной кислоты.
Выпаривают кислоту досуха на водяной бане с последующей выдержкой в сушильном шкафу при температуре до 140°С либо под инфракрасной лампой, либо на электроплитке со слабым нагревом. После охлаждения чашу с навеской снова помещают в охлажденную электропечь. Постепенно доводят температуру до 300°С и выдерживают в течение 0,5 ч. Указанный цикл повторяют несколько раз. Минерализацию считают законченной, когда зола станет белого или слегка окрашенного цвета, без обугленных частиц. При наличии обугленных частиц повторяют обработку золы раствором азотной кислоты или водой.
Параллельно в двух чашках проводят минерализацию добавляемых к навеске реактивов для контроля их чистоты.
Минерализация проб для колориметрического определения содержания железа
Минерализацию проб пищевых продуктов, кроме сыров, плодоовощного сырья и продуктов его переработки, проводят так, как было описано выше.
При минерализации сыров, плодоовощного сырья и продуктов его переработки пробу подвергают обработке азотной кислотой. Пробу плодоовощных продуктов перед обработкой высушивают в сушильном шкафу при температуре 105°С. Содержимое чаши смачивают азотной кислотой так, чтобы вся поверхность была покрыта кислотой (2—3 см3), и нагревают на водяной бане до прекращения выделения паров. Обработку азотной кислотой повторяют еще два раза. Затем обработанную навеску обугливают на электроплитке и проводят минерализацию так, как было описано выше.
Параллельно проводят минерализацию добавляемых к навеске реактивов для контроля их чистоты.
Минерализация проб для определения содержания мышьяка
В чашу с навеской продукта, содержащего менее 80% влаги, добавляют 10% массы навески в расчете на сухое вещество оксида магния и такое же количество спиртового раствора азотнокислого магния (в расчете на безводную соль). Полученную смесь тщательно перемешивают до образования однородной кашицы.
При анализе жидких продуктов, содержащих 80% влаги и более, вносят в чашу с навеской по 5% массы навески в расчете на сухое вещество оксида магния и раствора азотнокислого магния.
Допускается минерализацию зерна, продуктов его переработки и кондитерских продуктов проводить без добавления смеси оксида магния и азотнокислого магния.
Чашу с навеской помещают на водяную баню или в сушильный шкаф при температуре 80—100°С и выпаривают досуха, после чего переносят на электроплитку и обугливают при слабом нагреве до прекращения выделения дыма. Затем чашу помещают в электропечь, ранее отрегулированную на температуру 250°С, повышают температуру до 450°С постепенно на 50°С в час и продолжают минерализовать при этих условиях до получения серой золы. Далее проводят минерализацию, используя вместо раствора азотной кислоты воду. Параллельно в двух чашках проводят минерализацию добавляемых к навеске реактивов для проверки их чистоты.
2.6.2. Способ мокрой минерализации проб
Подготовка к минерализации
Способ основан на полном разрушении органических веществ пробы продукта при нагревании с серной и азотной концентрированными кислотами с добавлением хлорной кислоты или перекиси водорода, или при нагревании только с перекисью водорода и предназначен для всех видов сырья и продуктов, кроме сливочного масла и животных жиров.
Навеску жидких и пюреобразных продуктов массой, указанной в таблице 1 ГОСТ 26929—94, взвешивают в стакане, переносят в колбу Кьельдаля или в плоскодонную колбу, смывая стенки стакана 10—15 см3 дистиллированной воды. Допускается брать навеску непосредственно в плоскодонную колбу. Навеску твердых и пастообразных продуктов массой, указанной в таблице 1, берут на обеззоленный фильтр, заворачивают в него и стеклянной палочкой помещают на дно колбы Кьельдаля или плоскодонной колбы.
Из подготовленной пробы пива, минеральной воды, безалкогольного напитка отмеряют пипеткой объем, указанный в таблице 1 ГОСТ 26929—94, переносят в колбу Кьельдаля и упаривают на электроплитке до 10—15 см3.
Из подготовленной и отфильтрованной пробы винодельческих продуктов отмеривают пипеткой объем, указанный в таблице 1ГОСТ 26929—94, переносят в колбу Кьельдаля.
Навеску сухих продуктов (желатин, сухие яичные продукты) помещают в колбу Кьельдаля, добавляют 15 см3 воды, перемешивают. Желатин затем оставляют на 1 ч для набухания.
Кислотная минерализация проб сырья и пищевых продуктов, кроме винодельческих продуктов, растительных масел, маргарина, пищевых жиров, для определения содержания олова, меди, железа, алюминия
В колбу с пробой продукта, подготовленной к минерализации, вносят азотную кислоту из расчета 10 см3 на каждые 5 г продукта, на каждые 1—2,5 г консервированного молока или 20 см3 пива, минеральной воды или безалкогольного напитка и выдерживают не менее 15 мин. Можно оставить на ночь. Затем в колбу вносят 2—3 стеклянных шарика для равномерного кипения, закрывают грушевидной стеклянной пробкой и начинают нагревать на электроплитке слабо, затем сильнее, упаривая содержимое колбы до объема 3—5 см3. Колбы охлаждают, вносят 10 см3 азотной кислоты, содержимое упаривают до объема 5 см3, после чего охлаждают. Эту процедуру повторяют 2—4 раза.
В колбу вносят 10 см3 азотной кислоты, 5 см3 серной кислоты, 4 см3 хлорной кислоты (или вместо хлорной кислоты 4 см3 перекиси водорода) из расчета на каждые 5 г продукта или на 20 см3 пива, минеральной воды или безалкогольного напитка. Минерализацию молочных продуктов при определении меди и железа проводят без добавления серной кислоты. Не допускается изменять последовательность внесения кислот; хлорная кислота всегда добавляется последней. Содержимое колбы упаривают до объема около 5 см3, не допуская образования коричневой окраски жидкости. При появлении коричневой окраски нагревание прекращают.
Колбу охлаждают до комнатной температуры, добавляют 5 см3 азотной кислоты и 2 см3 хлорной кислоты (или вместо хлорной кислоты 2 см3 перекиси водорода) и снова нагревают до появления белых паров серного ангидрида. Если при этом раствор не обесцветился, эту процедуру повторяют. Минерализацию считают законченной, если раствор после охлаждения остается бесцветным или бледно-желтым.
Для удаления остатков кислот в охлажденную колбу добавляют 10 см3 воды и кипятят 10 мин с момента выделения белых паров, затем охлаждают. Добавление воды и нагревание повторяют еще два раза.
Если при этом образуется осадок, в колбу вносят 20 см3 воды, 2 см3 серной кислоты, 5 см3 соляной кислоты и кипятят до растворения осадка, постоянно дополняя испаряющуюся воду. Полученный минерализат после охлаждения используют для анализа, полностью или количественно переносят водой в мерную колбу, доводят до метки водой и перемешивают.
Параллельно проводят минерализацию добавляемых реактивов для контроля их чистоты.
Кислотная минерализация проб растительных масел, маргарина, пищевых жиров для определения содержания меди и железа
Пробу продукта в колбе Кьельдаля, подготовленную к минерализации, нагревают на электроплитке 7—8 ч до образования вязкой массы, охлаждают, добавляют 25 см3 азотной кислоты и вновь осторожно нагревают, избегая бурного вспенивания. После прекращения вспенивания колбу с содержимым охлаждают, добавляют еще 25 см3 азотной кислоты и 12 см3 хлорной кислоты и нагревают до получения бесцветной жидкости. Если во время сжигания жидкость темнеет, то к ней добавляют периодически по 5 см3 азотной кислоты и продолжают нагревание до завершения минерализации. Минерализацию считают законченной, если раствор после охлаждения остается бесцветным.
Параллельно проводят минерализацию добавляемых реактивов для контроля их чистоты.
Кислотная минерализация проб сырья и пищевых продуктов, кроме винодельческих продуктов, пива, растительных масел, маргарина, сыров для определения содержания мышьяка
В колбу Кьельдаля с навеской вносят азотную кислоту из расчета 2—3 см3 кислоты на 1 г сухих веществ (при этом азотная кислота должна полностью покрывать продукт) и выдерживают не менее 12 ч. После этого в колбу вносят 2—3 стеклянных шарика и медленно нагревают на электроплитке в течение 1,5—2 ч, избегая бурной реакции.
После охлаждения к содержимому колбы осторожно добавляют 10 см3 смеси равных объемов концентрированной серной и азотной кислот и нагревают в течение 1,5—2 ч. Прекращают нагревание, как только парообразование становится чрезмерным.
Если раствор в колбе до этого времени не обесцветился, то колбу охлаждают и добавляют в зависимости от интенсивности окраски азотную кислоту в количестве, равном первоначальному, или смешанный раствор азотной кислоты и перекиси водорода (2:1 по объему) и кипятят еще 0,5—2 ч до обесцвечивания жидкости. Если обесцвечивания не происходит, то вновь добавляют азотную кислоту и кипятят до прекращения выделения бурых паров окислов азота.
В колбе при кипячении всегда должно оставаться не менее 5 см3 жидкости.
Для удаления остатков кислот в колбу добавляют бидистиллированную воду в двойном количестве по отношению к первоначальному количеству азотной кислоты и кипятят до выделения белых паров. Затем в колбу добавляют 20 см3 воды, 0,1—0,2 г сернокислого гидразина и кипятят содержимое колбы в течение 1,5—2 ч. Готовый раствор должен быть бесцветным, допускается соломенно-желтая окраска.
Минерализация проб винодельческих продуктов с перекисью водорода для определения содержания меди
В колбу Кьельдаля с пробой продукта добавляют для вин и виноматериалов с массовой концентрацией сахара до 10 г/дм3, коньяков и коньячных спиртов 5 см3 перекиси водорода, для вин и виноматериалов с массовой концентрацией более 10 г/дм3 – 10 см3 перекиси водорода и нагревают на газовой горелке или электроплитке до кипения.
Вина и виноматериалы с массовой концентрацией сахара до 100 г/дм3 кипятят до объема 5—6 см3, затем колбу помешают в кипящую водяную баню и выпаривают содержимое до 2—3 см3.
Вина и виноматериалы с массовой концентрацией сахара от 100 г/дм3 и более кипятят до объема 7—10 см3, охлаждают, добавляют еще 5 см3 перекиси водорода, кипятят до объема 5—6 см3, затем выпаривают на водяной бане до объема 2—3 см3.
Если при выпаривании на водяной бане жидкость потемнеет, то после охлаждения добавляют еще 5 см3 перекиси водорода, кипятят до объема 5—6 см3 и вновь выпаривают на водяной бане до 2—3 см3.
После минерализации к содержимому колбы добавляют 1 см3 раствора соляной кислоты (1:36) и выпаривают на водяной бане до объема 2—3 см. Минерализат используют для анализа полностью, без разбавления.
Параллельно в двух колбах проводят минерализацию добавляемых к навеске реактивов для контроля их чистоты.
2.6.3. Метод минерализации при повышенном давлении
ГОСТ 31671—2012 (EN 13805:2002) определяет порядок подготовки проб пищевых продуктов методом минерализации при повышенном давлении для определения следовых элементов.
Кислотная минерализация при повышенном давлении является физико-химическим методом получения раствора следовых элементов пробы, используемым при подготовке пробы к определению этих элементов в соответствии со стандартизованными методиками, ссылающимися на данный метод и аттестованными в комбинации с ним.
Пробу гомогенизируют с помощью оборудования, гарантирующего незначительную степень контаминации определяемыми элементами, затем минерализуют при высокой температуре и давлении с использованием обычного или микроволнового способа нагрева в герметичном сосуде, помещенном в контейнер, выдерживающий высокое давление.
Следует иметь в виду, что при кислотной минерализации материалов с высоким содержанием углерода (например, углеводов, жиров и пр.) существует опасность взрыва.
Перед началом работы с аппаратом для минерализации под давлением следует внимательно ознакомиться с инструкциями по его эксплуатации и технике безопасности. Особое внимание следует обратить на риск отравления персонала лаборатории окислами азота. Детальное описание процедуры минерализации должно быть доступно в лаборатории в форме рабочей инструкции.
При подготовке пробы следует всеми возможными мерами предотвращать ее контаминацию определяемыми элементами. Например, при подготовке проб для определения хрома и никеля нельзя использовать ножи из нержавеющей стали.
Массу навески пробы подбирают, исходя из вместимости сосуда для минерализации, строго соблюдая инструкции производителя по обеспечению безопасности.
Например, в сосуд вместимостью 70 см3 в большинстве случаев можно поместить для минерализации до 400 мг сухой пробы или до 4 см3 жидкой пробы, эквивалентных 200 мг углерода. При меньшем содержании углерода допустимо использовать навеску пробы большей массы. Объем кислоты, необходимый для минерализации, зависит от природы материала пробы. Как правило, для минерализации пробы в указанных выше количествах достаточно 3 см3 концентрированной азотной кислоты. При минерализации чистых жиров может возникнуть необходимость использовать навеску пробы меньшей массы и порцию кислоты большего объема. Для предотвращения цементирования материала пробы на стенках сосуда и достижения полного смешивания пробы с кислотой добавляют от 0,5 до 1 см3 перекиси водорода.
При определении железа в сосуд с навеской пробы дополнительно вносят 0,5 см3 соляной кислоты для предотвращения потерь вследствие адсорбции на стенках сосуда.
Температуру, необходимую для достижения полной минерализации, определяют опытным путем, исходя из результатов анализов следовых элементов используемым методом. Например, применение более высокой температуры приводит к уменьшению остаточного содержания углерода в минерализате. Вследствие этого снижается фон при анализе методами электротермической атомно-абсорбционной спектрометрии и атомно-эмиссионной спектроскопии индуктивно-связанной плазмы, уменьшаются матричные эффекты при определении хрома с помощью масс-спектрометрии индуктивно-связанной плазмы и устраняются помехи при вольтамперных измерениях.
В начале минерализации рекомендуется плавное повышение температуры. Общей закономерностью является улучшение качества минерализации с повышением температуры. При определении мышьяка с помощью атомно-абсорбционной спектрометрии с генерацией гидридов минерализацию необходимо проводить при температуре 320°С, если имеется вероятность присутствия в пробе органических веществ, содержащих мышьяк.
Рекомендуемая продолжительность минерализации гомогенизированной пробы – около 3 ч. Продолжительность минерализации в микроволновых устройствах – от 15 до 30 мин. Продолжительность минерализации при высокой температуре можно сократить, если предварительно выдержать сосуд с навеской пробы и добавленной кислотой при комнатной температуре более длительное время, например, в течение ночи.
Для снижения давления внутри сосуда для минерализации его охлаждают в закрытом состоянии до температуры, близкой к комнатной.
Охлажденный сосуд с минерализованной пробой помещают в вытяжной шкаф, открывают и выдерживают до прекращения видимого выделения коричневого дыма. Настоятельно рекомендуется дегазировать минерализат с помощью ультразвуковой бани.
Минерализат должен быть прозрачным, а его объем должен быть примерно таким же, как до минерализации. При заметном уменьшении объема минерализата, свидетельствующем о разгерметизации контейнера, минерализацию следует повторить.
Минерализат разбавляют водой до нужного объема, полученный таким образом раствор пробы переносят в сосуд из кварцевого стекла (настоятельно рекомендуется при определении ртути), перфторэтиленпропилена или перфторалкоксиполимера.
Для контроля над контаминацией проводят всю процедуру минерализации с холостой пробой, состоящей из того же объема кислоты и воды объемом до 4 см3 (в зависимости от массы навески пробы продукта).
Для контроля качества результатов анализа при испытании каждой серии образцов проводят анализ контрольной пробы с известным содержанием определяемого элемента, включающий все стадии, начиная с минерализации.
2.6.4. Способ кислотной экстракции (неполной минерализации)
Подготовка к экстракции
Способ основан на экстракции токсичных элементов из пробы продукта кипячением с разбавленными соляной или азотной кислотами и предназначен для растительного и сливочного масел, маргарина, пищевых жиров и сыров. В термостойкую колбу с навеской продукта, массой, указанной в таблице, вносят цилиндром 40 см3 раствора соляной кислоты (1:1) по объему. Допускается вместо раствора соляной кислоты применять раствор азотной кислоты (1:2) для указанных продуктов, за исключением сыров, при колориметрическом определении содержания железа.
В колбу добавляют несколько стеклянных шариков, вставляют в нее холодильник, помещают на электроплитку, покрытую асбестом, и кипятят в течение 1,5 ч с момента закипания. Затем содержимое колбы медленно охлаждают до комнатной температуры, не вынимая из холодильника.
Колбу с экстракционной смесью сливочного масла или жиров, или маргарина с кислотой помещают в холодную водяную баню для затвердевания жира. Затвердевший жир прокалывают стеклянной палочкой, водный слой фильтруют через фильтр, смоченный раствором кислоты, используемой для экстракции, в сосуд, выбор которого определяется дальнейшим ходом анализа и зависит от определяемого элемента (реакционную колбу, колбу Кьельдаля, кварцевую или фарфоровую чашу). Оставшийся в колбе жир расплавляют на водяной бане, добавляют 10 см3 раствора используемой кислоты, встряхивают, охлаждают, после охлаждения жир прокалывают и промывную жидкость сливают в тот же сосуд через тот же фильтр, затем фильтр промывают 5—7 см3 воды.
Экстракционную смесь растительного масла с кислотой переносят в делительную воронку. Колбу ополаскивают 10 см3 раствора используемой кислоты, который сливают в ту же воронку. После разделения слоев нижний водный слой сливают через фильтр, смоченный раствором используемой кислоты, в сосуд, выбор которого определяется дальнейшим ходом анализа, затем фильтр промывают 5—7 дм3 воды.
Экстракционную смесь сыра с кислотой фильтруют через фильтр, смоченный раствором кислоты, в сосуд, выбор которого определяется дальнейшим ходом анализа. Колбу ополаскивают 10 см раствора кислоты, который фильтруют через тот же фильтр, затем фильтр промывают 5—7 см воды
Подготовка экстрактов к определению содержания мышьяка
При использовании для экстракции раствора соляной кислоты экстракционную смесь фильтруют сразу в реакционную колбу для отгонки мышьяковистого ангидрида.
При использовании для экстракции раствора азотной кислоты экстракционную смесь фильтруют в коническую колбу, вносят 0,2 г сернокислого гидразина и кипятят содержимое колбы в течение 1,5—2 ч. Затем раствор количественно переносят в реакционную колбу для отгонки мышьяковистого ангидрида, смывая колбу порциями воды.
Подготовка экстрактов к колориметрическому определению содержания меди и железа
Экстракционную смесь фильтруют в колбу Кьельдаля. При использовании для экстракции раствора азотной кислоты содержимое колбы упаривают на электроплитке до объема 5—7 см3, колбу охлаждают, добавляют 1 см3 хлорной кислоты и кипятят до получения бесцветного или слабоокрашенного раствора.
При использовании для экстракции раствора соляной кислоты в колбу вносят 5 см3 азотной кислоты, упаривают на электроплитке до объема 5—7 см3, колбу охлаждают, добавляют 4 см3 азотной кислоты и 1 см3 хлорной кислоты и кипятят до получения бесцветного или слабоокрашенного раствора.
При определении меди в растительных маслах и маргарине обработку экстрактов не проводят.
Для удаления остатков кислот в охлажденную колбу с экстракционной смесью добавляют 10 см воды и кипятят 10 мин, затем охлаждают. Добавление воды и нагревание повторяют еще два раза. Полученный раствор количественно переносят в мерную колбу. Объем раствора доводят до метки водой и перемешивают.
Подготовка экстрактов для полярографического и атомно-абсорбционного анализа
Экстракционную смесь фильтруют в кварцевую или фарфоровую чашу. Жидкость осторожно выпаривают, а затем обугливают на электроплитке. Затем чашу помещают в электропечь и далее продолжают минерализацию.
Параллельно в двух колбах проводят экстракцию и подготовку экстрактов к анализу реактивов для контроля их чистоты.
2.6.5. Подготовка проб с помощью измельчения, дробления, размола и растирания
Подготовка проб продуктов переработки фруктов и овощей, консервов мясных и мясорастительных для лабораторных анализов осуществляется по методам, установленным ГОСТ 26671—2014.
Подготовка лабораторных проб для твердых продуктов, в том числе мясных консервов, заключается в получении однородной массы продукта с помощью измельчения, дробления, размола и растирания в зависимости от вида продукта.
Лабораторные пробы жидких и пюреобразных продуктов однородной консистенции (соковую продукцию с мякотью, фруктовые и овощные пюре, овощную икру, томатную пасту, паштеты, фарш, повидло и т.д.) только перемешивают. Варенье и джем тщательно растирают в ступке до состояния однородной массы.
Измельчение лабораторных проб
Пробы продуктов в зависимости от консистенции измельчают с помощью дробилки, гомогенизатора, миксера или ступки до получения гомогенной массы. Перед измельчением пробы продукта:
– в продуктах из косточковых фруктов удаляют косточки, в консервах из домашней птицы и дичи – кости, в остальных продуктах – специи, веточки, чашелистики и посторонние примеси;
– продукты, содержащие животные жиры, нагревают на водяной бане до расплавления жира;
– замороженные продукты предварительно размораживают в закрытом сосуде, жидкую часть, образующуюся при размораживании, добавляют к продукту.
В продуктах, содержащих легко разделяемые жидкую и твердую части, измельчению подвергают только твердую часть, предварительно слив жидкость в стакан, а затем обе части объединяют, перемешивают и растирают по частям в ступке до состояния однородной массы.
Дробление лабораторных проб
Дробление проб до размеров 10 мм осуществляют на щековых дробилках, до 2 мм – на валковых. Измельчение до размеров менее 1 мм, если это необходимо, проводят с использованием истирателей различных типов (дисковых, вибрационных) или мельниц (шаровых, стержневых), а также в лабораторных ступках. Внутренняя часть дробилки (мельницы) должна быть очищена, чтобы избежать загрязнения пробы, для чего через агрегат пропускают материал, попадание которого в пробу не приведет к загрязнению нежелательными компонентами. В процессе дробления (истирания) не должно быть потерь материала пробы.
Размол
Размалывание должны проводить как можно быстрее с тем, чтобы лабораторная проба подвергалась воздействию атмосферы ограниченное время. Если необходимо, предварительно перед размалыванием проводят дробление или крошение кусочков до нужных размеров. Важно, чтобы лабораторная проба была тщательно перемешана перед каждой стадией.
Если проба проходит через сито с отверстиями 1 мм, ее тщательно перемешивают. Затем пробу разделяют последовательно, используя делитель или аппарат для квартования до тех пор, пока не будет получена проба нужного размера.
Если проба не проходит через сито с отверстиями 1 мм, но проходит через сито с отверстиями 2,80 мм, ее тщательно перемешивают и готовят пробу нужного размера путем проведения последовательных делений, как было сказано выше. Осторожно размалывают эту пробу на хорошо очищенной мельнице, до полного прохода через сито с отверстиями 1 мм.
Если лабораторная проба не проходит через сито с отверстиями 2,80 мм, ее осторожно размалывают на хорошо очищенной мельнице до полного прохода через сито с отверстиями 2,80 мм. Тщательно перемешивают.
Размолотую лабораторную пробу последовательно разделяют при помощи делительного аппарата до тех пор, пока не будет получена проба нужного размера, необходимая для всех видов анализа (испытаний). Эту пробу размалывают на хорошо очищенной мельнице до ее полного прохода через сито с отверстиями 1 мм.
2.6.6. Подготовка проб с помощью центрифугирования
Подготовка лабораторных проб соковой продукции для лабораторных анализов осуществляется по методу, установленному в ГОСТ 26671—2014.
Осветленные соки и сокосодержащие напитки с объемной долей мякоти до 10% включительно (соки и нектары из цитрусовых фруктов, ананаса, персика, абрикоса и др.) или содержащие нерастворимые в воде вещества фильтруют через обеззоленный фильтр или центрифугируют с фактором разделения не менее 990 g в течение 15 мин.
Соки и сокосодержащие напитки с объемной долей мякоти свыше 10% (из манго, томата, банана и др.) предварительно разбавляют водой в соотношении 1:5 (по объему) для осветления раствора и центрифугируют с фактором разделения не менее 990 g в течение 15 мин. В случае неполного осаждения нерастворимых в воде частиц пробу вновь фильтруют через обеззоленный фильтр или центрифугируют с фактором разделения не менее 990 g в течение 15 мин.
Концентрированные соки и пюре предварительно разбавляют водой в соотношении 1:5 весовым методом.
В том случае, если концентрированный сок представляет собой пюре или содержит нерастворимые в воде вещества, пробу дополнительно центрифугируют.
При проведении хроматографического анализа часть подготовленной пробы продукта отбирают в медицинский шприц с дисковым фильтром диаметром пор 0,45 мкм и отфильтровывают его в виалу.
2.6.7. Требования к подготовке лабораторных проб
В процессе подготовки лабораторных проб с целью сохранения их свойств следует принимать особые меры.
Для определения массовой доли тяжелых металлов в продукте измельчение проводят в оборудовании из материала, не загрязняющего продукт металлами. Для определения массовой доли витамина С в продукте не допускается контакт пробы продукта с металлическими поверхностями, его аэрация и нагрев.
Для определения массовой доли минеральных примесей в продукте методом флотации пробу продукта перемешивают и измельчают, не подвергая растиранию.
Подготовленную пробу продукта помещают в банку подходящего объема по ГОСТ 5717.2 с плотно закрывающейся крышкой и снабжают этикеткой с указанием наименования предприятия-изготовителя, наименования продукта, даты выработки.
От подготовленной пробы одним из указанных способов отбирают пробы для всех последующих анализов (испытаний), причем каждый раз перед взятием пробы всю массу тщательно перемешивают.
Для определения витаминов, каротиноидов и других нестабильных веществ анализы (испытания) проводят сразу после приготовления пробы, а для остальных анализов (испытаний) – берут по мере необходимости в течение суток. При этом пробу хранят при температуре от 0°С до 5°С.