4. «Запрещённая химия» А. Р. Оганова
С помощью методики, предложенной А. Р. Огановым, можно прогнозировать кристаллические структуры, существующие в условиях повышенного давления. Соединения, предсказанные алгоритмом А. Р. Оганова, бывают как слоистыми, так и носят пространственный характер. Вещества под давлением могут обладать сверхпроводимостью или являться хорошими изоляторами электрического тока. В разделе 10 мы вернёмся к более подробному описанию свойств исследуемых в данном параграфе кристаллических решёток. Рассматриваемую в этой книге методику можно применить для моделирования химических структур, существующих как под высоким давлением, так и в нормальных условиях.
А. Р. Оганов в программе «USPEX» разработал максимально результативный на сегодняшний день численный алгоритм, опираясь на который возможно предсказать ту или иную кристаллическую структуру. Время, которое необходимо затратить на прогнозирование кристаллов или молекул, в общем случае будет зависеть не только от числа частиц, участвующих в расчёте, но и от количества полученных квантовых систем с минимальным значением полной энергии.
Принципы, положенные в основу моделирования кристаллических структур и молекул:
а) В исследуемом химическом соединении не должно существовать пустых потенциальных ям, в которых могут располагаться электроны. Исключениями являются потенциальные ямы, соответствующие полностью свободным подуровням, входящим в состав орбитальной диаграммы атомов, зафиксированных в узлах рассматриваемой структуры. Вдобавок ко всему, необходимо взять в расчёт сумму тех треугольников, которые будут отвечать за дырочную проводимость, если таковая появится в веществе.
б) Между элементами кристаллической решётки должна существовать симметрия. Данное условие обеспечивает стабильность химической структуры.
в) Кристаллы характеризуются строгой пространственной периодичностью в расположении составляющих их материальных частиц (ионов или молекул). Под периодичностью понимают повторяемость элементов решётки в том или ином направлении. Данное требование не распространяется на квазикристаллы.
г) Модели кристаллов или молекул должны быть максимально компактными. Если исследуемая структура окажется менее компактной, чем прочие химические соединения, обладающие похожим составом атомов, тогда рассматриваемое вещество нельзя будет синтезировать в природе.
В случае, когда моделируемый кристалл или молекула будут удовлетворять требованиям, рассмотренным выше (см. пункты а – г), тогда полная энергия полученной на практике квантовой системы примет минимальное значение. Таким образом, атом водорода H, например, будет стремиться приблизиться к центру грани другого химического элемента, с которым происходит соединение.
Пример 4.1. Na2He
Рассмотрим слоистую структуру Na2He, существующую под высоким давлением. В дальнейшем наименования видимых ядер, входящих в состав исследуемых химических соединений, будем обозначать большим шрифтом, а невидимых – маленьким. Вычислим сумму треугольников, заключённых внутри каждого из атомов гелия и натрия, тогда:
He=0;
Na=48—11+10-30=17
где 48 – расчётное количество потенциальных ям, расположенных на оболочке куба (атома) уровня h=3 (см. таблицу 2.1 столбец 3);
11 – порядковый номер натрия Na, определяемый согласно таблице Менделеева;
10 – номер последнего химического элемента, расположенного на предыдущем уровне h=2. Подходящим элементом является неон Ne;
30 – трёхкратное количество электронов, зафиксированных на предыдущих оболочках куба (атома) уровней h=1 и h=2.
Определим количество крестиков, следовательно:
He=2; Na=48—17=31.
Структура Na2He продемонстрирована на изображениях 4.1 и 4.2.

Рисунок 4.1 Вид «спереди» для кристалла Na2He.
Символом «*» обозначаются потенциальные ямы, где треугольники совмещаются с крестиками.

Рисунок 4.2 Вид «сверху» для структуры Na2He.
Необходимо отметить, что в процессе формирования кристаллической решётки Na2He 3d10 подуровень, входящий в состав орбитальной диаграммы атома натрия Na, останется полностью свободным. Таким образом, общее число треугольников, определяемое для рассматриваемого химического элемента, составит 17—10+2=9, где 17 – сумма незанятых потенциальных ям, заключённый внутри иона натрия Na, а 10 – количество потенциальных ям, расположенных на незаполненном 3d10 подуровне. Если 3p6 подуровень, входящий в состав орбитальной диаграммы атома Na, останется полностью свободным, то в этом случае общее число треугольников примет следующее значение: Na=9-6-2=1. Итак, чтобы определить количество треугольников, находящихся в атоме Na, необходимо и достаточно взять в расчёт 2 неучтённые частицы, которые по факту перейдут на 4-й уровень.
В процессе трансформации пространства потенциальных ям внутренняя энергия u химического соединения начнёт изменяться. Вместе с тем атомы исследуемой структуры будут перемещаться относительно неподвижной точки пространства в сторону минимизации полной энергии Ep. В случае, когда полупериоды синусоидальной функции стабилизируются, тогда рассматриваемая квантовая система примет стационарное состояние.
Пример 4.2. CaF2He
Вычислим сумму треугольников для фтора, следовательно:
F=14-6-9+2=1
где 14 – расчётное количество потенциальных ям, существующих на оболочке куба (атома) уровня h=2 (см. таблицу 2.1 столбец 3);
6 – трёхкратное количество электронов, находящихся на уровне h=1;
9 – порядковый номер фтора F;
2 – номер последнего химического элемента, расположенного на предыдущем уровне h=1.
Определим общее число треугольников для кальция, тогда:
Ca=48-30-20+10=8
здесь 48 – расчётное количество потенциальных ям, локализованных на оболочке куба (атома) уровня h=3 (см. таблицу 2.1 столбец 3);
30 – трёхкратное количество электронов, находящихся на предыдущих оболочках куба (атома) уровней h=1 и h=2;
20 – порядковый номер кальция Ca, определяемый согласно таблице Менделеева;
10 – номер последнего химического элемента, расположенного на предыдущем уровне h=2.
Вычислим количество крестиков, следовательно:
Ca=48—8=40;
F=14—1=13.
Сумма треугольников для гелия He была определена в примере 4.1.
Кристаллическая структура CaF2He изображена на чертежах 4.3 и 4.4.

Рисунок 4.3 Вид «сверху» для кристалла CaF2He.

Рисунок 4.4 Вид «спереди» для структуры CaF2He.
Пример 4.3. MgF2He
Исходя из особенностей строения кристаллической решётки CaF2He, возможно смоделировать структуру MgF2He.
В синтезированном на практике химическом соединении взаимодействующие между собой атомы как правило могут располагаться различным образом относительно друг друга. Рассматриваемое вещество MgF2He не является исключением. В этом примере мы смоделируем лишь одну из модификаций исследуемой кристаллической структуры.
Определим количество треугольников для магния, следовательно:
Mg=48-30-12+10—10=6. Вместе с тем в рассматриваемом атоме 4s2 подуровень будет полностью заполнен электронами, тогда Mg=8;
где 48 – расчётное количество потенциальных ям, расположенных на оболочке куба (атома) уровня h=3 (см. таблицу 2.1 столбец 3);
30 – трёхкратное количество электронов, зафиксированных на предыдущих оболочках куба (атома) уровней h=1 и h=2;
12 – порядковый номер магния Mg, определяемый согласно таблице Менделеева;
10 – номер последнего химического элемента, находящегося на предыдущем уровне h=2;
– 10 – количество свободных потенциальных ям, расположенных на незаполненном 3d10 подуровне.
Вычислим сумму крестиков, входящих в состав иона магния Mg, тогда:
Mg=48-8-10=30.
Расчётные параметры для гелия He и фтора F были определены в примерах 4.1 и 4.2 соответственно.
Структура MgF2He продемонстрирована на иллюстрациях 4.5 и 4.6.

Рисунок 4.5 Вид «сверху» для структуры MgF2He.

Рисунок 4.6 Вид «спереди» для кристалла MgF2He.
Моделируемое в этом примере химическое соединение является проводником электрического тока, поскольку в процессе поиска наиболее компактной структуры MgF2He произошло заполнение 4s2 подуровня, входящего в состав орбитальной диаграммы атома Mg.
Пример 4.4. H3S
Определим сумму треугольников для водорода H и серы S, тогда:
H=1;
S=48-30-16+10—10=2
где 48 – расчётное количество потенциальных ям, расположенных на оболочке куба (атома) уровня h=3 (см. таблицу 2.1 столбец 3);
30 – трёхкратное количество электронов, зафиксированных на предыдущих оболочках куба (атома) уровней h=1 и h=2;
16 – порядковый номер серы S, определяемый согласно таблице Менделеева;
10 – номер последнего химического элемента, находящегося на предыдущем уровне h=2;
– 10 – количество свободных потенциальных ям, расположенных на незаполненном 3d10 подуровне.
Вычислим общее число крестиков, следовательно:
S=48-2-10=36;
H=1.
По своим свойствам химическое соединение H3S является высокотемпературным сверхпроводником.
Рассматриваемое в этом примере вещество возможно синтезировать в природе из сульфида водорода H2S, если повысить давление до 1,5 млн. атмосфер и понизить температуру до —70° C. При данных термодинамических параметрах кристаллическая решётка H3S будет иметь нулевое электрическое сопротивление, что приведёт к появлению сверхпроводимости внутри исследуемого опытного образца.
Структура H3S продемонстрирована на чертежах 4.7 и 4.8.

Рисунок 4.7 Вид «спереди» для кристалла H3S.
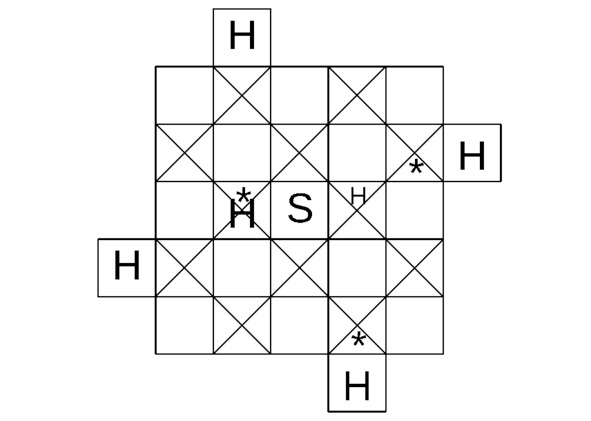
Рисунок 4.8 Вид «сверху» для кристалла H3S.
Пример 4.5. Пентазолат натрия
В современных научных исследованиях часто поднимается вопрос о хранении тех или иных материалов, которые в нормальных условиях окружающей среды не образуют чистых стабильных соединений. Пентазол HN5 является таковым материалом, а вещество, которое способно удерживать атомы рассматриваемой молекулы в стабильном состоянии, носит название пентазолата натрия.
Пентазол имеет следующую химическую структуру:

Рисунок 4.9 Структурная формула пентазола HN5.
Прежде чем приступить к доказательству того, что молекула пентазола не может быть получена в чистом виде на практике, необходимо определить количество свободных потенциальных ям, участвующих в химическом взаимодействии атомов.
Вычислим сумму треугольников для азота, следовательно:
N=14-7-6+2=3
где 14 – расчётное количество потенциальных ям, расположенных на оболочке куба (атома) уровня h=2 (см. таблицу 2.1 столбец 3);
7 – порядковый номер азота N, определяемый согласно таблице Менделеева;
6 – трёхкратное количество электронов, зафиксированных на предыдущей оболочке куба (атома) уровня h=1;
2 – номер последнего химического элемента, находящегося на первом квантовом уровне h=1.
Количество треугольников для водорода H и натрия Na было определено в примерах 4.4 и 4.1 соответственно.
Вычислим сумму крестиков, тогда: