Глава 2 Знакомьтесь: рибосома
Стоит упомянуть ДНК, как почти все понимающе закивают в ответ. Все мы знаем – или думаем, что знаем, – что такое ДНК. Эта молекула определяет нашу сущность: кто мы такие и что от нас унаследуют дети. Она превратилась в метафору, описывающую фундаментальные свойства почти чего угодно. «Это у них в ДНК» – говорим мы, даже рассуждая о какой-нибудь корпорации.
Однако, заговорив о рибосоме, вы рискуете наткнуться на непонимание даже у некоторых ученых. Несколько лет назад в радиоэфире передачи «Материальный мир» на ВВС Квентин Купер сказал мне, что гость с прошлой передачи просто возмутился, что на обсуждение глаза было выделено всего полвыпуска, а какой-то обычной молекуле (рибосоме) посвятили целый выпуск. Важно не только то, что большинство компонентов глаза формируется благодаря рибосомам – практически любая молекула в любой клетке любого организма собирается либо благодаря рибосомам, либо под действием ферментов, которые на них синтезируются. На самом деле, пока вы это читаете, рибосомы в каждой из триллионов клеток вашего тела успевают сделать тысячи белков. Миллионы существ обходятся без глаз, в то время как рибосомы нужны любому организму. Открытие рибосомы и ее роли в синтезе белков – это кульминация одного из величайших триумфов в истории современной биологии.
Прибыв в Калифорнию для изучения биологии, я, как и большинство физиков, понятия не имел о рибосоме и весьма приблизительно представлял, что такое ген. Знал, что в генах заключены признаки, наследуемые от предков и передаваемые потомкам. Оказалось, что все гораздо интереснее. Это информационные единицы, обеспечивающие развитие полноценного организма из единственной клетки, например из оплодотворенного яйца. Хотя практически во всех клетках содержится полный набор генов, в разных тканях активируются разные совокупности генов, поэтому нервная клетка отличается по свойствам от эпителиальной. Но что же такое гены?
В широком смысле ген – это участок ДНК, содержащий информацию о том, как и когда синтезировать белок. Белки выполняют тысячи биологических функций. Например, обеспечивают мышечные сокращения, позволяют воспринимать свет и тепло, осязать, бороться с болезнями, даже мыслить и запоминать. Многие белки, называемые ферментами, катализируют химические реакции, при которых в клетке синтезируются тысячи других молекул. Итак, белки отвечают не только за структуру и форму клетки, но и за ее функционирование.
Открытие того факта, что информационная единица из ДНК служит для синтеза белка, стало вершиной творческого десятилетия, которое началось с публикации классической статьи Джеймса Уотсона и Френсиса Крика о двойной спирали ДНК в 1953 году. Эта структура позволяет сделать вывод, как молекула работает, передает информацию и самовоспроизводится, но долго оставалось тайной, как клеточная информация дублируется при делении клетки и как потомки наследуют эту информацию при репродуктивном цикле.

Рис. 2.1. Структура ДНК
Когда Уотсон экспериментировал с картонными шаблонами азотистых оснований, его осенила блестящая идея: он осознал, что аденин (A) из одной спирали может образовывать химическую связь (пару) только с тимином (T) из другой спирали, тогда как гуанин (G) из одной спирали аналогичным образом соединяется с цитозином (C) из другой. Контуры любой пары оснований, будь то АТ или GC, примерно одинаковы, причем форма одной спирали задает форму другой, а порядок оснований в одной спирали зависит от порядка оснований в другой. При делении клетки двойная спираль расплетается, и каждая половина содержит достаточную информацию, чтобы послужить шаблоном для новой спирали. В результате из одной молекулы ДНК получаются две, то есть гены самовоспроизводятся, передавая наследственные признаки из поколения в поколение.
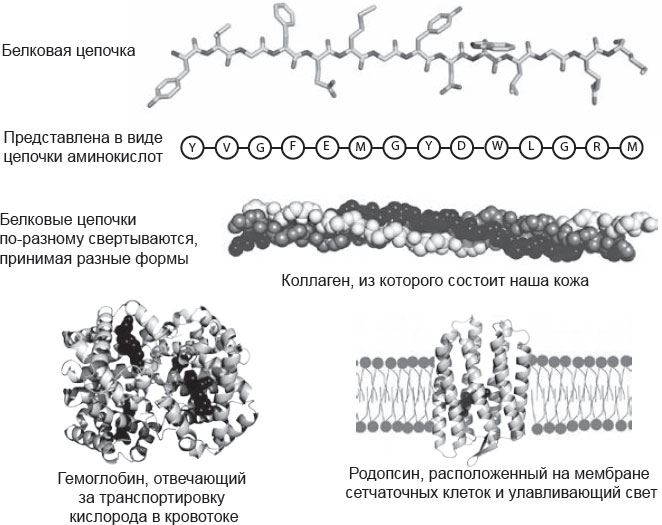
Рис. 2.2. Белки
Структура ДНК подсказала, как гены должны копироваться и передаваться, но не продемонстрировала их участия в синтезе белков. Дело в том, что каждая молекула ДНК – это длинная цепочка «первоэлементов», в состав которых входят четыре типа азотистых оснований. Но белки – это совершенно иные цепочки, состоящие из аминокислот, и химические связи в них тоже абсолютно другие. Исключительное разнообразие белков обусловлено тем, что двадцать аминокислот, входящих в их состав, сильно отличаются друг от друга по химическом свойствам. Их длина и порядок в каждой белковой цепочке уникальны, и, что удивительно, белок содержит информацию, необходимую для правильного свертывания цепочки, чтобы та приобретала нужную форму и правильно функционировала. Крик догадался, что порядок оснований в ДНК кодирует порядок аминокислот в белке, но оставался вопрос: каким образом?

Рис. 2.3. Транскрипция: копирование гена из ДНК на матричную РНК
Ученые бились над этой проблемой более десяти лет. Оказалось, что участок ДНК, содержащий ген, копируется на схожую молекулу, именуемую матричной РНК (мРНК), которая доставляет генетическое «сообщение» туда, где оно требуется. РНК (рибонуклеиновая кислота) отличается от ДНК (дезоксирибонуклеиновой кислоты) тем, что имеет дополнительную гидроксильную группу в сахарном «кольце»[6]. В РНК тоже четыре азотистых основания, но вместо Т находится очень похожее основание урацил (U), которое образует пару с А.
Как сделать двадцать типов аминокислот, имея четыре типа оснований? Все равно что прочесть длинную последовательность инструкций, записанных незнакомыми буквами. Оказалось, что основания считываются группами (кодонами) по три за раз. Способ их считывания, предсказанный Криком, связан с еще одной молекулой РНК, именуемой транспортной РНК (тРНК). С одного конца к ней прикрепляется нужная аминокислота, а с другого – группа из трех оснований (антикодон). Антикодон и кодон образуют пары оснований, такие же, как возникающие между двумя спиралями ДНК. Следующий кодон распознается другой тРНК, которая подносит его вместе с соответствующей аминокислотой, и т. д.
Следующее крупное открытие заключалось в том, что все это происходит не само собой. Клеточные биологи открыли органеллы, где считываются мРНК и синтезируются белки. В каждой клетке (и у бактерии, и у человека) есть тысячи таких крошечных частиц. Но по молекулярным меркам они огромны. В каждой из них находится примерно пятьдесят белков и три больших участка собственной РНК (это уже РНК третьего типа, существующая наряду с мРНК и тРНК). Сначала ученые называли эти органеллы рибонуклепротеиновыми частицами микросомального порядка, поскольку они состоят одновременно из РНК и белков и при этом отграничены от клеточных органелл, именуемых микросомами. Но такое название получалось слишком пространным, поэтому на одной конференции в конце пятидесятых Говард Динцис назвал их рибосомами – с тех пор это название и закрепилось. Именно Динцис первым определил, в каком направлении происходит синтез белковой цепочки. Диву даюсь, но, проработав тридцать лет в сфере биологии, я ничего не слышал о Динцисе и его работах. Когда в 2009 году мы с ним в конце концов повстречались в Университете Джона Хопкинса, куда меня пригласили прочитать названную в его честь лекцию, Динцис все еще по праву гордился, что сам придумал это слово.

Рис. 2.4. Транспортная РНК: молекулы-адаптеры, подносящие аминокислоты и считывающие код матричной РНК
Целая рибосома состоит из половины миллиона атомов. Связывая наши гены и кодируемые ими белки, она находится на перекрестке жизни. Хотя все знали это, никто не представлял, как выглядит рибосома, кроме того, что она глобулярная и состоит из двух частей. Но, не зная, как выглядит рибосома, разве мы могли понять, как она связывается с мРНК и сшивает белок из аминокислот, поднесенных тРНК.

Рис. 2.5. Состав рибосомы
Представьте, что вы – марсианин, смотрите на Землю издалека. Видите на поверхности крошечные объекты, движущиеся преимущественно по прямым линиям и иногда поворачивающие в перпендикулярном направлении. Приблизившись, вы замечаете, что эти объекты движутся, только когда в них попадают более мелкие тельца, и останавливаются, когда эти тельца их покидают. Обратившись к приборам, вы обнаруживаете, что эти объекты поглощают углеводороды и кислород, а в окружающую среду выбрасывают углекислый газ, водяной пар и избыток тепла, а также некоторое количество загрязнителей. Но чтобы выяснить, каким образом происходят эти процессы, вам необходима более серьезная детализация.
Когда мы узнали детали строения ДНК, это произвело революцию в представлениях о том, как именно в ней хранится, передается и воспроизводится генетическая информация. Но рибосома, в отличие от ДНК, колоссальная и сложная, поэтому казалась непостижимой.
Многие великие ученые, в частности Крик, сыгравшие ключевые роли в выяснении того, как кодируется информация в ДНК, попросту не решились подступиться к рибосоме и занялись другими исследованиями. Сидни Бреннер, не менее именитый коллега Крика и один из первооткрывателей мРНК, еще в шестидесятых сказал, что разгадка структуры рибосомы – тривиальная проблема, над которой не нужно работать в Кембридже, поскольку ее решат американцы. Мне это напоминает фразу сенатора Джорджа Эйкена, выразившегося о неподъемной вьетнамской войне так: «США должны объявить о победе и отправить войска домой». Одним из первых ученых, неотступно занимавшихся рибосомами, были молекулярный биолог Джеймс Уотсон и биохимик из Женевы Альфред Тиссьер. Почти сорок лет спустя в лаборатории Колд-Спринг-Харбор в 2001 году Уотсон вспоминал те давно минувшие дни, когда, по его словам, он осознал, сколь сложна рибосома, и смирился, что никогда не узнает ее структуру.

Рис. 2.6. Альфред Тиссьер и Джеймс Уотсон, одни из первых исследователей рибосом (фото предоставлено лабораторией Колд-Спринг-Харбор)
Я был еще очень далек от размышлений о рибосомах, когда обосновался в лаборатории Маурисио Монталя, но, проработав там всего несколько месяцев, наткнулся на статью о рибосомах в журнале Scientific American, которая изменила мою жизнь. В ней было описано, как найти в рибосоме множество разных белков методом рассеяния нейтронов – такая практика широко известна в физике, но едва ли используется в биологии. Авторами этой статьи были Дон Энглман и Питер Мур. Я вспомнил, что Дон один из тех, кто был готов дать мне работу, когда я пытался перейти из физики в биологию, и написал ему, что подготовился к работе постдока. Мне казалось, что я уже достаточно изучил биологию, чтобы приступить к исследованиям в этой дисциплине, и получать кандидатскую степень по биологии мне незачем.
Основные научные интересы Дона, как и у Маурисио, были связаны с мембранами и мембранными белками, и я сказал, что хотел бы работать у него в лаборатории. Он мне ответил, что у него вакансий нет, зато они есть у Питера Мура, и если бы я отправился туда работать над рибосомами, то в свободное время мог бы позаниматься исследованием мембран. В ту пору я уже понимал фундаментальную важность рибосом, поэтому ответил, что меня предложение устраивает. Оказалось, что свободного времени у меня не будет.
Вскоре Питер написал мне, что собирается в Сан-Диего на конференцию и будет рад увидеться со мной. Он предстал передо мной в своем фирменном консервативном наряде: коричневый вельветовый пиджак, очки в толстой оправе. А его манеры завершали образ классического университетского интеллектуала из Лиги Плюща. Уже в ранней юности он стал быстро продвигаться в науке, и я подозревал, что он не представляет, как живут другие люди. Его отец был одним из родоначальников трансплантологии, работал в Гарварде, а сам Питер учился в частной школе, потом в Йеле, а затем отправился в аспирантуру в Гарвард, где вместе с Уотсоном исследовал рибосомы. После этого он продолжил работу в Женеве вместе с Тиссьером, который к тому времени стал ведущим ученым в исследовании рибосом. Там он приступил к постепенной очистке различных белков в составе рибосомы.

Рис. 2.7. Так Питер Мур выглядел около 1980 г., когда автор работал в его лаборатории в Йеле
Питер Мур осознал, что ключ к пониманию рибосомы спрятан в ее структуре и нужно освоить структурный анализ. Он покинул Женеву и прибыл в Лабораторию молекулярной биологии Совета медицинских исследований (MRC) Кембриджа. Там в свое время Уотсон и Крик работали над ДНК, и лаборатория стала Меккой для тех, кто занимался изучением структур всевозможных биомолекул. Британцы называли ее MRC–LMB или просто LMB – под таким наименованием она известна сегодня.
Затем Питер вернулся в альма-матер, Йельский университет, и стал там преподавателем. Всесторонне эрудированный и остроумный, он терял свою привычную сдержанность, когда речь заходила о науке. Его лекции были выразительны, изобиловали шутками, и целые поколения йельских студентов и преподавателей испытали на себе его ярость, когда пытались предъявить ему небрежные доводы.
На конференции в Сан-Диего, где мы впервые встретились, он стоял особняком и дожидался меня. После краткого приветствия мы обсудили мой научный багаж и его проект. Я не был уверен, что это неформальное собеседование прошло успешно, но вскоре он пригласил меня в Йель. Там, несмотря на мою очевидную неподкованность, Питер официально предложил мне работу. Остаток академического года я провел в лаборатории Маурисио, завершая начатое исследование. В конце лета отправился в Нью-Хейвен, по дороге подобрав в Огайо семью, с которой не виделся несколько недель.
Осенью 1978 года я прибыл в лабораторию Питера, испытывая некоторый трепет. Несмотря на два года аспирантуры по биологии, я обладал весьма ограниченным опытом. Через пару дней после моего приезда мы с Питером шли навстречу друг другу по длинной галерее в Химической лаборатории имени Стерлинга, выстроенной в неоготическом стиле. Как только мы приблизились, он вдруг отвел глаза. Я переживал, что он уже успел пожалеть о том, что принял меня. Потом Бетти Ренни, рассмеявшись, объяснила мне, что это просто его манера. Питер оставался крайне приветлив со мной, и год спустя он, должно быть, чувствовал, что я был достаточно компетентным, чтобы остаться без его руководства на целый год – пока он будет находиться в творческом отпуске в Оксфорде. За время его отсутствия я отпустил бороду, которую носил почти двадцать пять лет.
К тому моменту, как я стал работать у Питера, уже были установлены некоторые базовые факты о рибосомах. Каждая рибосома состоит из двух частей: большой и малой субъединиц. Малая субъединица связывается с мРНК, содержащей генетическую информацию, а большая сшивает аминокислоты, подносимые тРНК, и делает из них белок. В рибосоме есть пазы для трех тРНК, одна из которых подносит новую аминокислоту, другая – удерживает растущую белковую цепочку, а третья – выступает в качестве своеобразной перевалочной базы, куда белки попадают перед выходом из рибосомы. И тРНК движутся по рибосоме от одного паза к следующему. В сущности, они протаскивают мРНК вслед за собой, и сама рибосома фактически движется вдоль мРНК, помогая тРНК считывать кодон за кодоном при синтезе белка. Прохождение каждого этапа требует энергии, поэтому рибосому часто называют молекулярной машиной, или наномашиной.
Рибосомы были интересны не только из-за фундаментальной роли очага жизни, но и с практической точки зрения. За годы работы многие ученые замечали, что действие антибиотиков заключается в блокировании функций рибосомы на разных этапах. Человеческие рибосомы существенно отличаются от бактериальных, причем некоторые из этих антибиотиков связываются преимущественно с бактериальными рибосомами и поэтому лечат инфекционные заболевания. Однако бактерии стремительно развивают резистентность к лекарствам, поэтому, точно зная, как именно антибиотик связывается с рибосомой, можно проектировать и создавать более качественные препараты.
Эти основополагающие факты уже присутствовали в учебниках, поэтому, когда я рассказывал кому-нибудь, что исследую рибосомы, меня часто спрашивали: «А что, разве о них еще не все известно?» Иногда меня при этом удостаивали снисходительным взглядом, как какого-то беднягу, который дорисовывает последние штрихи к проблеме, которая никого уже не интересует. Но пусть мы и представляли в общих чертах, как работает рибосома, мы еще не знали, как в ней реализуется хотя бы один из сложных процессов на пути к синтезу белка.
Как и во многих иных областях, в науке есть модные темы. Зачастую это сравнительно новые области, где исследователи быстро приходят к открытиям. Самые креативные открывают новые дисциплины, но другие просто переключаются с одной модной области на другую. Если бы так поступали все, то представление о феноменах было бы весьма поверхностным. Но, к счастью, бывают и другие ученые, которые не отступаются от проблемы, независимо от того, насколько она стара и сложна, чтобы докопаться до ее сути.
Хотя изучение рибосомы и продолжалось уже пару десятилетий, никто даже не представлял, где в ней располагаются эти пять десятков белков, не говоря уже о том, как они работают. Питер корпел над этой проблемой вместе с Доном Энглманом. Можно сказать, что не бывает двух настолько разных людей. Дон, в отличие от сдержанного Питера, был высокий общительный калифорниец с аккуратно подстриженной бородой и громовым баритоном, благодаря чему выглядел авторитетно в любых ситуациях. Он окончил Рид-Колледж в Портленде, затем защитил кандидатскую в Йеле и отправился в постдокторантуру к Морису Уилкинсу – третьему ученому, причастному к открытию ДНК. У Уилкинса он исследовал структуру мембран клеточной оболочки. В отличие от Питера, всю жизнь занимавшегося изучением тех или иных аспектов рибосомы, Дон имел более разнообразные интересы.
Они прослушали в Брукхейвенской национальной лаборатории лекцию Бенно Шенборна о том, как можно использовать нейтроны для изучения биологических структур. Понадобился бы ядерный реактор, чтобы получить достаточное количество нейтронов для эксперимента, однако в них заложено интересное биологическое свойство: обычный водород и его тяжелый изотоп дейтерий взаимодействуют с нейтронами очень по-разному, а на водород приходится более половины атомов, из которых состоят все биомолекулы, в частности белки и РНК.
Эта лекция натолкнула Дона и Питера на мысль, что можно попытаться выяснить расположение рибосомных белков. Они поняли, что если бы удалось каким-то образом синтезировать рибосому, в которой всего в двух белках вместо водорода содержался бы дейтерий, то от этих белков нейтроны рассеивались бы совсем иначе.
Можно получить дейтерированные белки, выращивая бактерии в тяжелой воде – оксиде дейтерия. Затем пересобрать рибосому, в которой было бы два дейтерированных белка на ваш выбор. (Масаясу Номура из Висконсина биохимическими способами выделил белки из малой рибосом-ной субъединицы, а потом очистил из смеси каждый из двадцати белков методом хроматографии.) Затем можно смешать все компоненты в растворе и, при соблюдении нужных условий, пересобрать из очищенных белков и РНК рабочую малую субъединицу, в которой два белка заменены на дейтерированные аналоги. Затем субъединицы можно поместить в ядерный реактор Брукхейвенской национальной лаборатории в Лонг-Айленде и подставить под пучок нейтронов, чтобы узнать расстояния между разными парами белков и определить, как они упорядочены и какова их трехмерная структура. Примерно так первопроходцы в старину картировали неизвестную территорию методом триангуляции. Такой эксперимент состоял из повторения однотипных измерений.
Я поступил в лабораторию, когда таким способом были идентифицированы лишь несколько первых белков, и принял эстафетную палочку от моего предшественника, постдока Дэна Шиндлера. С удивлением я узнал, что нейтронные пучки от ядерного реактора на порядки слабее рентгеновских лучей, поэтому могло уйти несколько дней на то, чтобы измерить слабый сигнал от дейтерированных белков, тонувший в фоновом рассеивании от всей остальной рибосомы. Летом такую работу было делать сподручнее; пока шел сбор данных, я иногда мог отправиться на пляж Файр-Айленда в нескольких километрах на юг. В другие периоды заточение в Брукхейвене отнюдь не казалось захватывающим, поскольку лаборатория находилась на территории старой военной части в глуши за Япханком. Ученые, работавшие там, жили в городках за многие километры от лаборатории, и эти территории представляли собой череду пасторальных деревушек и разросшихся пригородов. В отличие от университетского города с яркой культурной жизнью и ночными развлечениями, лаборатория пустовала вечерами и выходными. Эта ситуация напомнила мне знаменитую карикатуру на Лонг-Айлендскую автомагистраль; картинка гласила: «Съезд 66 – на Япханк. Если вы уже бывали в Япханке, пожалуйста, игнорируйте этот съезд».
Примерно через три года удалось идентифицировать около половины белков малой субъединицы, и мы написали пару статей об их расположении. Я задумывался, сколько времени мне понадобится на проработку остальных, но, когда срок моей стипендии подходил к концу, Дон обратился ко мне и сказал, что сейчас в моих интересах переходить к следующему этапу карьеры и что образование, нужное на этапе постдокторантуры, я уже получил. В конце концов этот проект завершил сменивший меня Малкольм Кейпел. В итоговой статье, описывавшей положение всех белков, они были изображены в виде бильярдных шаров, наложенных на контур малой субъединицы, и я любил пошутить, что примерно треть из этих шариков – мои.
Вняв совету Дона, я отправил резюме почти на пятьдесят преподавательских вакансий, но тогда было не лучшее время искать работу. В стране только что началась рейгановская эпоха, и научные исследования финансировались скупо, а биотехнологии только начали появляться.