Глава 1 ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ГЕСТОЗА
Современными исследователями установлено, что поток гормонов, поступающих в организм беременной женщины из плаценты, а также мощная импульсация с нервного рецептивного поля матки создают новую доминанту в центральной нервной системе (ЦНС) и соответствующее перераспределение энергозатрат. Гормоны беременности оказывают также и разностороннее непосредственное воздействие на многие органы и ткани. Как указывают Н. Л. Гармашева и Н. Н. Константинова (1985), происходящие при этом в организме изменения отнюдь не хаотичны; комплекс явлений, меняющих состояние во время беременности, называют «адаптацией к беременности», что хорошо отражает его физиологическую направленность.
Адаптивные реакции являются значительной дополнительной нагрузкой для беременной женщины, ивтожевремя они необходимы для плода. Это видно из следующих примеров.
1. Во время беременности масса тела возрастает значительно больше, чем весит матка с ее содержимым. Средней прибавкой массы называют цифру 10,5 кг, а нормальными границами, т. е. пределами, обычно не сопровождающимися осложнениями со стороны матери и плода, считают 6 – 16 кг.
2. Масса тела увеличивается отчасти за счет накопления жира (в ранние сроки беременности) и главным образом за счет воды. Общее количество воды к концу нормальной беременности возрастает на 7,5 л, что не сопровождается отеком. Установлена прямая корреляция между увеличением массы тела во время беременности и массой новорожденного ребенка.
3. Абсолютное число эритроцитов в крови во время беременности возрастает, но в меньшей степени, чем количество плазмы. Осмолярность крови уменьшается в среднем на 10 мосмоль. Снижается и вязкость крови. По-видимому, ее новые реологические свойства способствуют интенсивному маточноплацентарному кровотоку и обмену веществ между матерью и плодом.
4. Для благополучной адаптации к беременности нужна соответствующая перестройка почечной функции. Почки претерпевают большую дополнительную нагрузку во время беременности и нередко участвуют в дезадаптации организма к ней. Поэтому наиболее существенными изменениями при беременности, требующими внимания медицинского персонала, считают увеличение объема крови, минутного объема сердца, почечного кровотока, гипервентиляции легких, увеличение гидратации тканей, уменьшение PCO2 и осмолярности крови. Эти явления могут способствовать отеку, варикозному расширению вен на ногах и в прямой кишке, одышке, ортостатическому головокружению, гипотензивному синдрому в положении на спине.
5. Следует учитывать перестройку кровообращения в связи с появлением нового мощного сосудистого русла – материнской части плаценты. Сосудистое сопротивление этого русла очень низкое, и поток крови через него сравнивают с потоком через артериовенозную фистулу. Развивается дополнительная мощная сеть не только артериальных, но и венозных сосудов.
6. В процессе адаптации к беременности большую роль играют стероидные гормоны, которые влияют на материнский организм. Содержание прогестерона в крови во время беременности возрастает в 100 – 1000 раз, в моче беременных женщин обнаруживается 26 различных эстрогенов, продуцируемых плацентой.
7. Во время беременности происходит изменение обмена веществ так, что беременная больше, чем до беременности, может использовать энергию из жиров и тем самым сберегать углеводы и аминокислоты для плода.
Нарушения адаптации к беременности могут быть весьма разнообразными. Чаще всего встречается гестоз. Создавались различные теории патогенеза гестозов. Почти каждая из них вносила свой вклад в понимание этого процесса, а следовательно, и в современное представление о нем. Мы не будем останавливаться на всестороннем рассмотрении этой проблемы. Приведем лишь относительно новые данные и нашу концепцию возникновения гестоза.
Большого внимания заслуживает патогенез нарушений водно-солевого обмена при этом осложнении беременности, что привело к изменению клинического подхода к нему. Во время беременности задержка воды в организме сочетается с увеличением содержания натрия, и таким образом сохраняется новый, характерный для беременности, уровень осмотического давления. Одновременно, наряду с общими, наблюдаются и внутриорганные изменения гемодинамики, весьма значительные в почках. При этом во время беременности стимулируется как механизм, увеличивающий выделение натрия, так и механизм, консервирующий натрий. Изменение натриевого обмена при беременности тесно связано с гипервентиляцией, а увеличение уровня прогестерона приводит к нарушению газообмена за счет различной функциональной чувствительности нервных центров, ответственных за газообмен, что приводит к очень важному изменению его при беременности, а именно при всех сроках беременности вентиляция превышает уровень, необходимый для удовлетворения повышенной потребности беременной женщины в кислороде. При гестозе сокращаются почечный кровоток и гломерулярная фильтрация и задерживаются вода и натрий.
Показано, что патологический отек характеризуется увеличением внутриклеточной жидкости более, чем внеклеточной, что и наблюдается при гестозе. При нормальной же беременности большая часть воды находится вне клеток. Имеется много и других факторов, влияющих на водно-солевой обмен при беременности. Исходя из этого, ранее широко рекомендовалось ограничение солей, белков, а при развившемся токсикозе – применение мочегонных средств. Современные исследования показывают, что ограничение соли в диете и применение мочегонных средств являются грубым вмешательством в сложные механизмы установления и охраны нового уровня водно-солевого гомеостаза в организме беременной женщины. Более того, некоторые клинические исследования показывают, что ограничение солей и белков в диете женщин не только не препятствует, но даже способствует развитию гестозов беременных, а при ограничении количества жидкости может быть уменьшена прибавка содержания плазмы в крови, что далеко не безразлично для плода. Кроме того, при приеме беременными мочегонных препаратов существенно может нарушиться баланс калия в организме плода. Эти препараты, проникая легко через плаценту, оказывают влияние на функцию почек плода: например, применение фуросемида во время беременности вызывает у плода значительное увеличение диуреза. Поэтому в настоящее время общепризнано, что при беременности следует значительно ограничивать применение диуретиков. Многие авторы даже считают, что беременность является противопоказанием к их применению и исключением являются лишь декомпенсированные пороки сердца.
Общепризнано, что основное патогенное влияние на плод при гестозе оказывает уменьшение маточно-плацентарного кровообращения, особенно при гипертензивных формах гестоза. Изучен патогенез изменений системной гемодинамики при гестозе с увеличением ангиотензина и уменьшением реактивности к нему сосудистого русла, которое наблюдается при нормальной беременности, а при гестозе нет уменьшения реактивности сосудов по отношению к ангиотензину, возрастает периферическое сосудистое сопротивление, уменьшается объем крови за счет сокращения сосудов. Таким образом содержание крови, уменьшенное при преэклампсии в среднем на 10 %, соответствует новому уменьшенному объему сосудистого русла. Поэтому некоторые ученые считают нецелесообразным корригировать гиповолемию, перегружая сосудистое русло. Они также считают ошибочным мнение о том, что это может улучшить плацентарное кровообращение, так как здоровое сердце легко компенсирует уменьшение наполнения желудочков учащением сердечного ритма.
Наряду с указанными изменениями гемодинамики при гестозе наблюдаются значительные изменения функции плаценты. Возникает синдромы плацентарной недостаточности и отставания в развитии плода, который может неблагоприятно отразиться на развитии организма после рождения или привести к ранней неонатальной смертности.
КОНЦЕПЦИЯ ПАТОГЕНЕЗА ГИПЕРТЕНЗИВНЫХ ФОРМ ГЕСТОЗА
Артериальная гипертензия возникает вследствие повышения выше нормы содержания Са2+ в мышечных клетках сосудов. Артериальная гипертония беременных вызывается недостатком Са2+, что ведет к уменьшению содержания кальция в межклеточной жидкости. Это ведет к кальциевой перегрузке митохондрий как следствие нарушенной мембранной регуляции цитоплазматического свободного кальция, что в свою очередь создает предпосылки для отклонений в утилизации продуктов обмена, обеспечивающих выработку энергии в митохондриальном аппарате клеток. Последнее может проявиться в дальнейшем гипергликемией, дислипидемией, абдоминальным типом ожирения (рис. 1).
Мембранная концепция патогенеза первичной гипертензии исходит из признания того, что основа гипертензии – нарушение структуры и ионотранспортной функции клеточных мембран, проявляющееся снижением их способности (недостаточности) поддерживать в цитоплазме клеток нормальные величины градиента концентрации важнейших ионов (К+, Са2+, Na+) по отношению к внеклеточной среде.

Рис. 1. Первичная гипертензия. Вариант предполагаемой связи нарушений мембранной регуляции внутриклеточного Ca2+ энергообразовательной функции митохондрий (2) и метаболических нарушений (3), лежащих в основе проявлений метаболического синдрома [Постнов Ю. В., 2000]
Ключевым по значимости и более всего изученным следствием мембранного дефекта является смещение пределов регуляции концентрации свободного кальция цитоплазмы в сторону более высоких, чем в норме, значений с последующим развитием клеточного ресетинг-функциональной адаптации клетки к кальциевой перегрузке.
Благодаря уникальной роли кальция в клеточной физиологии повышенные концентрации свободных ионов кальция в цитоплазме существенно изменяют характеристики Ca2+-зависимых внутриклеточных механизмов, в связи с чем изменяются соотношения клетки с гормонами и нейромедиаторами, т. е. с системой нейрогормональной интеграции.
Появление избытка свободного кальция в цитоплазме клетки изменяет ответ кальцийзависимых внутриклеточных механизмов, в частности систем проведения сигнала от рецепторов к ее исполнительным механизмам. Этим изменяется взаимодействие клетки с симпатической нервной системой, эндокринной и другими системами интеграции. Для сохранения нормальной величины физиологического ответа воздействие гормона или медиатора на клетку должно быть соответственно изменено (обычно оно усилено).
Таким образом, по мнению Ю. В. Постнова (2000), сохраняя функцию в условиях нарушенной мембранной регуляции, клетка работает в новом режиме клеточно-гормональных отношений, названном «перенастройкой», или ресетингом, клетки. Вследствие этого вся совокупность клеток, составляющих ткани, будучи измененной, воздействует на системы нейрогормональной интеграции как бы изнутри – со стороны клеточной мишени, изменяя активность этих систем. Так повышается эфферентная активность симпатической нервной системы, гипоталамо-гипофизонадпочечниковой системы, изменяется функция инсулярного аппарата. Схема дополняется тем, что развитие хронической гипертензии всегда происходит при участии почки, играющей в кровообращении роль баростата. Возросшая активность нейрогормональных систем (прежде всего эфферентного звена симпатической нервной системы), отражая изменения кальциевого гомеостаза на клеточном уровне, позволяет почкам вопреки повышенному системному АД сохранить нормальный объем экскреции солей и воды.
Стабилизация АД на стационарно повышенном уровне, отвечающем особенностям ионотранспортной функции клеточных мембран и соответствующих им метаболических отклонений, реализуется через «перенастройку» (ресетинг) многокомпонентной системы контроля АД и сосудистого тонуса от системы эндотелин-NО-ренин-ангиотензиновой системы до барорецепторного аппарата в кровообращении.
В течение I половины беременности плохое, несбалансированное питание и стрессы вызывают истощение адреналосекреторной деятельности коры надпочечников, а избыток циклического аденозинмонофосфата (цАМФ) ведет к: 1) гиперхолистеринемии, дегенерации ворсинок хориона; 2) избытку альдостерона, вызывающему задержку натрия и воды; 3) увеличению в крови ангиотензина, повышающего АД, что вызывает рост внутриклеточного Са2+ и спазм гладкомышечных клеток сосудов; 4) вазопрессиноподобному действию на почечные канальцы, что ведет к задержке воды в организме беременной женщины.
Дегенерация ворсинок ведет к недостатку прогестерона. Прогестерон заменяется кортизолом, вызывая еще большее истощение коры надпочечников и, в тяжелых случаях, некроз. Во II половине беременности увеличивающийся недостаток Са и гипокальциемия в межклеточном пространстве ведут к проникновению избыточного Са2+ в гладкомышечные клетки сосудов, вызывая спазм сосудов, и преганглионарные симпатические нейроны с высвобождением избыточных количеств ацетилхолина. В постганглионарных адренергических нейронах избыток ацетилхолина ведет к дополнительной секреции α-адренергических катехоламинов с высвобождением большего количества Са2+ в гладкомышечных клетках сосудов, что приводит к усилению спазма сосудов и артериальной гипертонии. Повышение содержания Са2+ в поперечно-полосатых мышцах вызывает судороги мышц.
Такова общая конструкция патогенеза первичной гипертензии беременных, составляющая основу мембранной концепции. Она показывает, что артериальная гипертензия – это естественное и непременное качество конкретного организма, обусловленное особенностями клеточного метаболизма, и делает понятным, почему действие известных лекарственных гипотензивных средств всегда транзиторно, а высокое давление неминуемо возвращается к прежнему уровню после их отмены.
Гестоз (отеки, нефропатия, преэклампсия, эклампсия, протеинурия, гипертонический синдром) рассматривается как единое явление. Беременная женщина является превосходной клинической моделью для изучения гипертонии, которая может развиваться в острой молниеносной форме в течение нескольких недель и затем исчезать через несколько недель после окончания беременности.
Предполагается, что недостаток кальция может служить причиной развития гестоза. Эпидемиологические исследования показали, что у беременных женщин, потреблявших кальцийсодержащие продукты в большом количестве, реже бывает гестоз, даже у беременных с низким социальным уровнем и при отсутствии пренатального наблюдения. Экспериментальные исследования этих авторов на лабораторных животных также показали, что артериальная гипертензия развивается при недостаточном потреблении кальция и исчезает при нормализации его потребления вместе с пищей.
Согласно современным воззрениям отечественных авторов, показана роль митохондриальных нарушений в механизме энергетического дефицита. Как известно, в митохондриях осуществляется сопряжение процессов окисления и фосфорилирования с образованием аденозинтрифосфорной кислоты (АТФ). В то же время сведения о митохондриях клеток при первичной гипертензии очень немногочисленны.
Митохондрии, как буферная система поддержания оптимально низкой (10– 7 м) концентрации свободного кальция в цитозоле в силу хронической кальциевой перегрузки клеток, обусловленной недостаточностью ионотранспортной функции мембран при гипертензии, настроены на регулирование в цитозоле клеток более высоких концентраций кальция (Са2+), имея соответственно и более высокую, чем в норме, концентрацию этого иона в митохондриальном матриксе (Са2+).
Постоянно повышенный уровень аккумуляции Са2+ митохондриями при гипертензии вызывает в них ряд нарушений, важнейшим следствием которых является снижение синтеза АТФ и развитие структурных изменений митохондрий, прослеженных на экспериментальной модели первичной гипертензии.
Интенсивная аккумуляция митохондриями избытка цитозольного Са2+ при гипертензии, сопровождающаяся затратой энергии на выкачивание протонов в цитоплазме и соответствующим снижением продукции АТФ, носит постоянный характер. Происходящее при этом «сжигание» АТФ для обеспечения механизма аккумуляции Са2+ сопровождается повышенным образованием побочных токсических продуктов работы дыхательной цепи, в частности супероксида свободных гидроксильных радикалов, способных повреждать молекулы белка, липидов и нуклеиновых кислот. Это составляет основу механизмов повреждения митохондриального аппарата при первичной гипертензии.
Одновременно нарушение клеточной энергетики составляет звено, объединяющее мембранные нарушения и метаболический синдром.
Патофизиологические изменения при гестозе могут быть подразделены на две фазы: в 1-й фазе, примерно в I половине беременности, проявляющейся действием избыточного цАМФ, происходит гиперплазия коры надпочечников, их гиперфункция и истощение; во 2-й фазе, характеризующейся действием избыточного клеточного Са2+, которое наступает ко II половине беременности после геморрагии и некроза коры надпочечников.
Основным нарушением функции клеток, ведущим к гипертензии, является длительный спазм гладкомышечных клеток — артериол.
Механизм возникновения этой дисфункции во время беременности в результате действия различных гормонов и Са2+ является предметом развиваемой нами концепции гестоза.
Оптимальная суточная потребность кальция составляет для беременных и кормящих 1200 мг.
Концентрация кальция во вне- и внутриклеточной жидкости поддерживается в очень узких пределах, что жизненно важно для нормального функционирования физиологических систем. Этот элемент находится преимущественно вне клетки.
Его внутриклеточная концентрация составляет около 1/10000 от концентрации вне клетки. Нервное проведение, сокращение мышцы и свертывание крови зависят от нормального содержания кальция.
Кальций находится в крови в ионизированном состоянии (Ca2+), а также в связанной с белками форме и образует комплексы с различными отрицательно заряженными соединениями. Около 50 % общей концентрации представлено свободной или ионизированной формой кальция. Ионизированный кальций биологически активен и играет ключевую роль в осуществлении нервно-мышечной передачи и свертывании крови. Внеклеточный ионизированный кальций находится в равновесном состоянии с резервной формой кальция, депонированной в костях. Концентрации кальция и фосфата во внеклеточной жидкости взаимосвязаны: приблизительно сохраняется величина произведения растворимостей этих двух ионов.
Механизмы, участвующие в поддержании нормальной концентрации ионизированного внеклеточного кальция, регулируют его абсорбцию в желудочно-кишечном тракте, экскрецию почками и процессы обмена в костях. Организм защищает себя от гипокальциемии, увеличивая его абсорбцию в желудочно-кишечном тракте, уменьшая почечную экскрецию и повышая скорость разрушения костей и деминерализации. Высокие концентрации кальция во внеклеточном пространстве приводят к снижению его абсорбции в желудочно-кишечном тракте, увеличению экскреции почками и усилению минерализации костей.
В процессе эволюции появилась клеточная мембрана для защиты клетки от окружающей среды и для поддержания ионного баланса межклеточной жидкости в состоянии, подобном тому, при котором развивалась жизнь на Земле.
В высокой концентрации Са2+ является токсином для клетки, и при резком повышении концентрации Са2+ клетка немедленно умирает. Практически при всех энзиматических взаимодействиях используется Са2+, но в очень малых количествах. Имеется специальный клеточный механизм, поддерживающий гомеостаз Са2+. В мембране есть каналы, благодаря которым Са2+ может проникать через мембрану. При этом кальциевые каналы являют большое разнообразие по сравнению с натриевыми каналами. С точки зрения филогенеза считается, что Са-каналы гораздо древнее, чем натриевые каналы, и в процессе развития они появляются всегда раньше.
В плане механизма действия Са2+ важно учитывать, что, во-первых, мембрана в покое очень слабо проницаема для Са2+, поэтому не требуется больших затрат энергии для поддержания оптимального уровня Са2+, во-вторых, имеется Са-насос, или Са2+-Mg2+-АTФaзa, который выкачивает Са2+ из клетки в межклеточное пространство.
Повышение содержания Ca2+ внутри клетки приводит в действие мембранный Са-насос, контролируемый Са-кальмодулином. Тогда в норме концентрация Са2+ внутри клетки понижается, клетка таким образом защищается от токсического воздействия высокой концентрации Са2+.
Митохондрии и эндоплазматический ретикулум в гладких мышцах играют главную роль в клеточном Са-гомеостазе.
Перенос Са2+ из цитоплазмы в пространство матрикса митохондрий требует затраты энергии и может совершаться в больших количествах, в то время как перемещение из матрикса лимитировано и совершается пассивно. Если концентрация Са2+ в цитоплазме повышается, например вследствие продолжительного воздействия мессенджера (агента), тогда Са2+ в большом количестве поступает в митохондрии и большая его часть остается здесь в ионизированном состоянии. Наконец, достигается какой-то постоянный уровень, при котором обмен Са2+ между митохондриями и цитоплазмой происходит таким образом, что содержание Са2+ в цитоплазме сохраняется лишь на несколько более высоком уровне, чем в клетке в состоянии покоя. Если все же концентрация Са2+ продолжает оставаться повышенной, Са2+ начинает поступать в митохондрии или в эндоплазматический ретикулум быстрее, чем выводится из них, и происходит насыщение митохондрий. Когда способность митохондрий поглощать Са2+ истощается, избыточное содержание Са2+ приводит к дисфункции клетки и, наконец, к ее гибели.
КАЛЬЦИЙ, ГЛАДКОМЫШЕЧНАЯ МУСКУЛАТУРА СОСУДОВ, ГИПЕРТЕНЗИЯ
Ангиотензин и α-адренергические катехоламины, воздействуя на гладкомышечные клетки сосудов, вызывают их сокращение. При повышенной концентрации какого-нибудь из катехоламинов они вступают в соединение с соответствующими специфическими рецепторами на поверхности мембраны мышечной клетки сосуда и вызывают поступление Ca2+ в цитоплазму из пула плазменной мембраны и эндоплазматического ретикулума, а также происходит поступление Са2+ из межклеточного пространства через каналы с рецепторной или электрической регуляцией.
Содержание Са2+ в цитоплазме также повышается при уменьшении способности эндоплазматического ретикулума абсорбировать его и понижается при повышении содержания цитоплазматического Na+ и повышении вследствие этого Na+-Са2+-обмена. Оба эти вида обмена регулируются цАМФ таким образом, что повышенное содержание цАМФ может привести к повышению содержания Са2+ в цитоплазме.
Состояние сокращения гладкомышечных клеток сосудов зависит от степени фосфорилирования миозиновой короткой легкой цепи, которое контролируется Са-зависимой протеинкиназой, киназой миозиновой легкой цепи. Таким образом, если содержание Са2+ в цитоплазме повышается, процесс фосфорилирования миозиновой легкой цепи усиливается и АД повышается. Любые процессы, вызывающие длительное повышение содержания Са2+ в цитоплазме гладкомышечных клеток сосудов выше нормы, ведут к артериальной гипертензии.
ПАТОФИЗИОЛОГИЯ ГЕСТОЗА
Необходимо подчеркнуть, что в I половине беременности могут возникать условия, ведущие к дисфункции эндокринной системы (рис. 2), что в дальнейшем может привести к спастическим васкулитам и артериальной гипертензии во II половине беременности.
Аргументом для пересмотра сложившихся представлений явилось открытие характерных для этой патологии генерализованных нарушений ионотранспортной функции и ряда других свойств клеточных мембран различных тканей организма, а также выявление «метаболического синдрома», объединившего гипертензию с целым спектром сопутствующих обменных нарушений, к которым относят сахарный диабет тип 2, гиперинсулинемию, дислипидемию, абдоминальное ожирение. Полагают, что основу метаболического синдрома составляет необычно высокая резистентность тканей к инсулину, характерная для этой формы гипертензии.
Вначале адренокортикотропный гормон (АКТГ), воздействуя на кору надпочечников, вызывает ее гиперстимуляцию, что ведет к повышению продукции цАМФ в коре надпочечников в несколько тысяч раз выше нормы. При таком сверхфизиологическом количестве цАМФ наблюдается не только избыточный синтез холестерола, кортизола и альдостерона в коре надпочечников, но и поступление больших количеств цАМФ в кровь и далее в различные органы, где он вызывает неспецифическую задержку воды, приводящую также к различным патологическим состояниям и реакциям. Имеется клиническое подтверждение, что если у беременных в I половине беременности повышается уровень цАМФ в крови, моче и в амниотической жидкости, то во II половине беременности развивается гестоз.

Рис. 2. Патофизиология гестоза в I половине беременности
ЭТИОЛОГИЧЕСКИЕ ФАКТОРЫ
Следующие этиологические факторы ведут к гиперстимуляции коры надпочечников и к продукции больших количеств цАМФ.
• Плохое общее питание.
Для нормального клеточного метаболизма необходимо определенное количество витаминов, энзимов, коэнзимов, ионов H+ и других метаболитов, так же как и углеводов, жирных кислот, аминокислот и белков, минеральных веществ и О2.
Дефицит каких-либо компонентов энзимных систем может привести к блокированию нормальных биохимических реакций.
Недостаток одного или нескольких витаминов всегда ведет к гиперплазии, гипертрофии коры надпочечников, которая может доходить в крайних случаях до удвоения массы. Витамины выступают в качестве катализаторов в энзимных системах. Тропные гормоны, действующие извне на рецепторы мембран, контролируют энзимные системы. Если биохимическая реакция энзимной системы заблокирована по той или иной причине, система обратной связи вызывает большую продукцию гормона, контролирующего энзимную систему. Гормоны коры надпочечников участвуют в большинстве физиологических функций. Если вырабатывается недостаточно гормонов коры надпочечников (кортикальных), механизм обратной связи, воздействуя на систему гипоталамус – гипофиз – кора надпочечников, вызывает усиленное образование адренокортикотропного гормона (АКТГ), что приводит к кортикальной гиперплазии и гипертрофии и в крайних случаях к истощению и дегенерации коры надпочечников. В отсутствие Са+2 активность большинства гормонов подавляется, в то время как продукция цАМФ в надпочечниках на отсутствие Са+2 почти не влияет.
Продукция цАМФ в коре надпочечников при максимальном стероидогенезе мала по сравнению с продукцией цАМФ в ответ на максимальную концентрацию АКТГ, когда она может быть в несколько тысяч раз выше нормы. Для уменьшения избытка цАМФ необходимо действие фосфодиэстеразы и Са-кальмодулина; таким образом при недостатке Са+2 избыток цАМФ сохраняется. АКТГ взаимодействует с мембранным рецептором клеток коры надпочечников и активирует аденилатциклазу. Аденилатциклаза в присутствии Са-кальмодулина образует цАМФ из АТФ. Действуя посредством протеиновых киназ, цАМФ образует холестерол (холестерин Са27Н45ОH) из липидных капель.
Образование специфического протеина в клетках коры надпочечников также вызывает цАМФ. При взаимодействии этого протеина со свободным холестеролом образуется прегненолон, который внутри митохондрий превращается в прогестерон. В ходе дальнейшего синтеза в цитоплазме прогестерон превращается в кортизол и альдостерон, которые секретируются кортикальными клетками в кровь.
• Предшествующие заболевания.
Такие предшествующие заболевания, как сахарный диабет и гипофункция щитовидной железы, могут вызывать стрессоподобные состояния и давать такой же эффект, как и недостаточное (несбалансированное) питание. При недостатке вторичных гормонов биохимические реакции в энзимных системах могут блокироваться и холестерол будет накапливаться. Организм матери может абсорбировать инсулин или тироксин плода, что приведет к относительному диабету или гипотиреозу плода, сопровождаемым гиперхолистеринемией.
• Синдром истощения.
Общий метаболизм увеличивается с начала беременности и к III триместру повышается на 33 % по сравнению с уровнем его до беременности. Питание может быть адекватным до беременности, но с наступлением беременности может стать неадекватным. Работа сердца в покое возрастает в начале беременности и достигает пика – примерно на 40 % больше, чем до беременности – к 20-й нед. беременности. Наибольшее гемодинамическое напряжение достигается к 32-й нед. беременности. Гемодинамические изменения еще больше возрастают при физической нагрузке, и расход О2 повышен у беременных по сравнению с небеременными женщинами. При интенсивной и (или) длительной физической нагрузке может возникать дефицит O2, при котором некоторые ткани могут оказаться в состоянии кислородного голодания.
Недостаток О2 может привести к блокированию биохимических реакций в энзимных системах как у матери, такиуплода и к накоплению у них цАМФ и холестерола.
Синдром истощения сейчас играет бóльшую роль в возникновении гестоза, чем раньше. В современном обществе женщины часто работают полный рабочий день в дополнение к их обычным обязанностям домашней хозяйки, жены и матери. Очень часто они работают по 16 ч в день, что ведет к хроническому истощению и стрессу.
Многие биохимические реакции могут быть заблокированы вследствие относительного недостатка питательных веществ и гормонов. Синтез прогестерона может нарушаться в плаценте и в коре надпочечников, где прогестерон является предшественником кортизола. Кортизол составляет 80 % кортикальных гормонов и является необходимым для многих биологических функций, особенно связанных с продукцией энергии.
• Эмоциональный стресс.
Селье (1950) показал, что любой стресс вызывает в основном одинаковые изменения физиологических процессов и биохимических реакций на уровне клеточного метаболизма. Эмоциональный стресс, действуя на систему кора головного мозга – гипоталамус – гипофиз – кора надпочечников, вызывает длительную АКТГ-стимуляцию, истощение коры надпочечников и избыток цАМФ. Хотя беременная женщина может противостоять значительному количеству стрессов небольшой интенсивности и продолжительности, не заболев при этом, и родить здорового ребенка, но, если она подвергается сильному стрессовому воздействию в течение долгого времени, это может привести к истощению коры надпочечников и избытку цАМФ, что также может явиться этиологическим фактором возникновения гестоза.
• Недостаток кальция.
Недостаток кальция в I половине беременности может привести к блокаде энзимных реакций в клетках многих органов. Сюда относятся не только метаболизм костей, свертывание крови, но и те процессы, где Са2+ активирует внутриклеточные протеины, такие как кальмодулин и такие, где Са2+ служит вторичным мессенджером. Механизм обратной связи ведет к избытку цАМФ, что может также привести к развитию гестоза.
ДЕЙСТВИЕ ИЗБЫТКА цАМФ В КОРЕ НАДПОЧЕЧНИКОВ
• Возникновение избытка холестерола.
При нарушении синтеза стероидных гормонов в коре надпочечников возникающий там избыток цАМФ может продолжать вызывать синтез свободного холестерола. Этот избыточный холестерол может затем поступать в кровь, что ведет к гиперхолистеринемии, которая часто встречается у беременных и более выражена при развитии гестоза. Недостаточные состояния матери сказываются на состоянии плода, что ведет к нарушению остального стероидогенеза. Холестерин накапливается в крови плода. Гиперхолестеринемия ведет к холестериновым эндартериитам у матери, плода и в плацентарных сосудах.
• Возникновение избытка альдостерона и кортизола.
Избыток цАМФ также ведет к избыточному синтезу кортизола и альдостерона, выделяющихся в кровь. Альдостерон слабо связывается с протеинами плазмы крови и быстро выходит из крови в клеточную и межклеточную жидкость. В месте нахождения он вызывает внутри-, экстрацеллюлярную и васкулярную задержку Na+ и воды. Также он вызывает задержку Na+ и воды в почках, действуя на клетки дистальных канальцев и коллекторного протока.
ДЕЙСТВИЕ ИЗБЫТКА КОРТИКАЛЬНОГО цАМФ ВНЕ КОРЫ НАДПОЧЕЧНИКОВ
• Возникновение избытка ренина.
Обычно цАМФ действует в той клетке, где он синтезирован. Внутриклеточная концентрация цАМФ равна примерно 10– 7 М, в то время как в плазме крови – 10– 9 М. Гормоны в нормальных условиях могут повышать содержание цАМФ в плазме крови в 40 раз, тем не менее введенный извне цАМФ неэффективен в этой концентрации из-за слабой абсорбции клетками. Некоторые аналоги цАМФ легче проникают в клетку и используются в эксперименте для получения цАМФ-подобного эффекта.
В эксперименте с использованием суспензии клеток почки было показано, что добавление цАМФ вызывает статистически значимое повышение продукции ренина. Если цАМФ производится в количествах, превышающих физиологические, и наступает истощение коры надпочечников, тогда большие количества цАМФ могут поступать в кровь и достигать околоклубочковых клеток почек (юкстагломерулярные клетки), что может привести к синтезу избыточного ренина, который превратится в ангиотензин II (АII), являющийся наиболее сильным из известных сосудосуживающих веществ. Вдобавок ангиотензин действует на периферические адренергические нейроны и на мозговую часть надпочечников, вызывая синтез и выделение катехоламинов, что также действует на мозговые центры, вызывая повышение симпатической активности, и все это вместе приводит к повышению артериального давления.
• Избыток цАМФ вызывает вазопрессиноподобный эффект в клетках почечных канальцев.
Вазопрессин, или антидиуретический гормон, секретируется нейронами супраоптического и паравентрикулярного ядер гипоталамуса и накапливается в заднем отделе гипофиза. Его секреция и выделение контролируются осморецепторами, находящимися в гипоталамусе, которые чувствительны к изменениям осмотического давления в плазме крови. В этих клетках почечных канальцев цАМФ вызывает резкое повышение проницаемости клеточных мембран, обращенных в просвет канальца с луминальной стороны к воде, мочевине и другим растворимым веществам, что ведет к задержке воды. Количество мочи уменьшается, и она становится концентрированной. Избыточное действие вазопрессина может привести к периферическим отекам. При истощении коры надпочечников и продукции сверхфизиологических количеств цАМФ его уровень в плазме крови становится настолько высок, что абсорбируется в значительных количествах как юкстагломерулярными клетками, так и клетками почечных канальцев. Тогда действие избытка цАМФ на клетки почечных канальцев приводит к возникновению отека.
ДЕГЕНЕРАТИВНЫЕ ИЗМЕНЕНИЯ В ПЛАЦЕНТЕ
Если кортикальный стероидогенез у матери и плода нарушается вследствие какой-либо причины, это ведет к избыточному синтезу цАМФ, холестерина, альдостерона и к задержке Na+, как это описано выше. Гиперхолестеринемия вызывает холестериновые эндартерииты у матери, у плода и в плацентарных сосудах. В то же время избыток цАМФ ведет к гиперсинтезу ренин-ангиотензина, что вызывает спастические васкулиты в сосудах плаценты. Все это вместе может привести к окклюзии сосудов плаценты. Если в процесс вовлечены мелкие сосуды ворсинок, ворсинка может подвергнуться дегенерации и абсорбции или же рядом с дегенерирующей ворсинкой может происходить фибринообразование. Если затронуты крупные сосуды, может произойти инфаркт и дегенерация плаценты, на месте инфаркта может сформироваться рубец или киста. При обширной дегенерации ворсинок плацента теряет способность продуцировать прогестерон, необходимый для поддержания беременности, и также нарушается синтез кортикальных стероидов.
РАННИЕ ФАЗЫ ГЕСТОЗА
• Отек беременных.
Предпосылки для развития гестоза в конце I половины или в начале II половины беременности. Истощение коры надпочечников у матери и плода, вызываемое в I половине беременности плохим питанием и различными стрессами, во II половине беременности – замещением прогестерона кортизолом, сопровождается продукцией сверхфизиологических количеств цАМФ у матери и плода. В коре надпочечников избыток цАМФ вызывает избыточный синтез холестерола (холестерина) и альдостерона. Вне коры надпочечников избыток цАМФ вызывает вазопрессиноподобный эффект в почечных канальцах и задержку воды, что усиливается действием альдостерона и ведет к отекам и задержке натрия в различных тканях и органах, включая стенки артерий.
• Начало гипертонии.
Избыток цАМФ вызывает избыточный синтез ренин-ангиотензина в юкстагломерулярных (околоклубочковых) клетках. Ангиотензин стимулирует дальнейший синтез альдостерона. Наибольшие дозы ангиотензина в эксперименте у животных вначале не вызывают изменений артериального давления, но, безусловно, вызывают повышение секреции альдостерона. Позже, когда альдостерон уже привел к накоплению натрия в стенках сосудов, эти же самые малые дозы ангиотензина вызовут повышение артериального давления.
Ангиотензин приводит к повышению содержания Са2+ в цитоплазме гладкомышечных клеток сосудов, вызывая поступление Са2+ через рецепторно-управляемые каналы клеточной мембраны и высвобождение Са2+ из мембранного пула (резервуаров) из эндоплазматического ретикулума.
Повышение содержания натрия в клетке и воздействие цАМФ могут вызвать уменьшение Na-Са-обмена и привести к еще большему увеличению содержания Са2+ в цитоплазме. Повышенное количество Са2+ в цитоплазме приводит в свою очередь к повышению активности киназы легкой цепи миозина, к усилению фосфорилирования легкой короткой миозиновой цепи и тонического сокращения (тонуса) гладкомышечных клеток в стенках артерий, что ведет к повышению артериального давления.
В I половине беременности артериолы ворсинок оказываются весьма чувствительными к гиперхолистеринемии и сосудосуживающему действию ангиотензина. Плацентарные артерии тех пациенток, у которых развивается гестоз, поражены обширными эндартериитами, склерозированием и тромбозами и развитием дегенерации ворсинок.
У беременных крольчих, у которых удаление в конце I триместра беременности щитовидной железы вызывает гиперхолистеринемию у плода, также наблюдаются сильно выраженные холестериновые эндартерииты плацентарных сосудов.
Таким образом, рассматривая клеточные механизмы артериальной гипертензии, вызванной беременностью, следует заключить, что гипертония возникает вследствие увеличения выше нормы содержания Са2+ в гладкомышечных клетках сосудов. Гипертония (гестоз), обусловленная беременностью, вызывается недостатком Са, что ведет к уменьшению содержания Са в межклеточной жидкости, это деполяризирует клеточные мембраны и повышает потенциал нейронов в гладкомышечных клетках, что влечет за собой вход избыточного Ca2+.
В течение I половины беременности плохое (несбалансированное, недостаточное) питание и стрессы вызывают истощение адреносекреторной деятельности коры надпочечников и избыток цАМФ, что в свою очередь ведет к:
1) гиперхолистеринемии, эндартериитам и дегенерации ворсинок хориона;
2) избытку альдостерона, вызывающему задержку натрия и воды;
3) повышению в крови содержания ангиотензина, повышающего артериальное давление, что вызывает увеличение содержания внутриклеточного Са2+ и спазм гладкомышечных клеток сосудов;
4) вазопрессиноподобному действию на почечные канальцы, что ведет к задержке воды.
Дегенеративные изменения ворсинок хориона ведут к недостатку прогестерона. Прогестерон заменяется кортизолом, вызывая еще большее истощение коры надпочечников и, в тяжелых случаях, его некроз. Во II половине беременности возрастающий недостаток Са2+ и гипокальциемия межклеточной жидкости ведут к проникновению избыточного Са2+ в гладкомышечные клетки сосудов, а преганглионарные симпатические нейроны приводят к высвобождению избыточного ацетилхолина. В постганглионарных адренергических нейронах избыток ацетилхолина ведет к дополнительной секреции α-адренергических катехоламинов с высвобождением большого количества Са2+ в гладкомышечных клетках сосудов с усилением их спазма и появлением артериальной гипертонии. Повышение содержания Ca2+ в поперечно-полосатых мышцах вызывает судорожные сокращения мышц.
Такова общая конструкция патогенеза первичной гипертензии беременных, составляющая основу мембранной концепции. 1. Замещение недостатка прогестерона кортизолом у матери и плода.
Известно, что кортизол и прогестерон могут замещать друг друга в метаболических процессах, если имеется недостаток одного из них. Удаление коры надпочечников у экспериментальных животных обычно заканчивается смертельным исходом в течение 5 – 7 дней. Но этого, например, не происходит у 13-ringer бурундука, у которого полное удаление коры надпочечников имеет незначительные последствия, так как ее функции берут на себя яичники.
В яичниках развивается ткань, подобная ткани коры надпочечников. Прогестерон продлевает продолжительность жизни у животных с удаленной корой надпочечников, и некоторые из них могут сохранять удовлетворительное состояние неограниченно долгое время. Эстрогены и тестостерон не оказывают подобного эффекта. Экспериментальные животные после удаления коры надпочечников остаются в удовлетворительном состоянии, если имеется беременность или функционирует желтое тело, вплоть до окончания беременности или удаления желтого тела.
В случае недостатка прогестерона, что наблюдается при дегенерации плаценты, восстановительные механизмы вызывают увеличение выработки гормонов, которые стимулируют синтез прогестерона в тех железах, на которые они воздействуют. Кора надпочечников начинает синтезировать больше прогестерона. Взамен синтезируется больше кортизола и альдостерона из прогестерона, которые обладают способностью секретироваться. В более поздние сроки беременности, при продолжающейся плацентарной дегенерации, недостаток прогестерона еще более усиливается. Кора надпочечников продолжает подвергаться стимуляции вплоть до ее истощения, и может наступить ее некроз. Общий вес коры надпочечников матери и плода составляет примерно 20 г, а вес плаценты 400 – 800 г; ясно, что способность коры надпочечников продуцировать прогестерон мала по сравнению с плацентой. Удельная продукция кортизола (по отношению к весу и размерам тела) у плода соответствует таковой у взрослого. Относительное количество свободного кортизола по сравнению со связанными протеинами плазмы крови гораздо больше у плода (36 %), чем у матери (12 %). Поэтому существует градиент свободного кортизола от плода к матери. Вследствие наличия этого градиента и в результате замещения прогестерона кортизолом в случае дегенеративных изменений в плаценте регуляторные механизмы, воздействуя на гипофиз плода, вызывают усиление секреции АКТГ. За этим вскоре следует гиперплазия коры надпочечников плода, и это оказывается причиной «фетальной зоны», которую часто (но не всегда) находят при рождении у человека и у некоторых видов млекопитающих.
2. Некроз коры надпочечников.
Обнаруживаются некрозы и геморрагические инфаркты в участках коры надпочечников, взятых на биопсию при гестозе [Attia et al., 1970], а также в коре надпочечников в случае летального исхода. Продукция больших количеств цАМФ в коре надпочечников, когда они истощаются, должна прекратиться при наступлении некроза. Клиническая картина убедительно это доказывает. При нормальной беременности содержание цАМФ в моче, крови и амниотической жидкости повышается в III триместре беременности, а при гестозе оно достигает примерно лишь половины значений при нормальной беременности и приближается к средним значениям у небеременных. Когда эти значения определяются выше нормальных на сроках 16 – 24 нед. беременности, тогда развивается гестоз. Низкое содержание ренин-ангиотензина и альдостерона в тяжелых случаях гестоза можно объяснить низким уровнем цАМФ после некроза коры надпочечников.
3. Прогрессирующий недостаток Са.
По мере развития беременности потребность в Са возрастает. Во II половине беременности объем общего метаболизма повышается примерно на 1/3 и требуется больше Са, который участвует во многих метаболических процессах. Большие количества Са необходимы для быстро растущего организма (скелета) плода. Многие беременные женщины получают менее 1000 мг Са в день, в то время как исследования показывают, что они нуждаются в бо́льшем количестве. Duggin et al. (1974) установили, что если беременная получает 2000 мг Са в день, то ею абсорбируется и удерживается кальция больше, чем у тех, кто получает 1000 мг. В обеих группах выделяется одинаковое количество Са в моче. У тех беременных, которые получают 1000 мг Са, его позитивный баланс составляет 142 мг в день, а у тех, кто получает 2000 мг, позитивный баланс – 305 мг.
Недостаток поступления Са с пищей может привести к гипокальциемии в межклеточной жидкости. В этом случае регуляторные механизмы приводят к увеличению выработки паратиреоидного гормона, способствующего высвобождению Са из костей. Этот механизм может поддерживать содержание Са в межклеточной жидкости на уровне, близком к норме, если недостаток Са невелик и непродолжителен. Некоторое количество Са костей существует в мобильной форме, которая может быстро абсорбироваться в случае недостатка поступления Са извне. Тем не менее большая часть Са костей находится в форме устойчивых соединений и весьма медленно подвергается реабсорбции в случае недостатка поступления Са. Этот процесс оказывается неспособным поддерживать нормальный уровень Са в межклеточной жидкости, если во время беременности, когда потребности в Са остаются высокими в течение длительного времени, поступление Са извне недостаточно.
• Гипокальциемия в межклеточной жидкости ведет к повышенному содержанию ацетилхолина и α-адренергических катехоламинов, спазму гладкомышечных клеток сосудов и гипертензии. Гипокальциемия в межклеточной жидкости деполяризует клеточные мембраны преганглионарных симпатических нервов, относящихся к гладкомышечным клеткам сосудов, и повышает активный потенциал. Са проходит в клетку через канал, управляемый потенциалом. Активный потенциал проходит вдоль нейронного аксона к двигательному окончанию и вызывает высвобождение ацетилхолина посредством экзоцитоза, причем количество высвобождаемого ацетилхолина определяется количеством поступившего Са. Затем в постганглионарных адренергических нейронах ацетилхолин запускает высвобождение катехоламинов, которые посредством α-рецепторов приводят к повышению содержания Са в клетках гладкой мускулатуры сосудов, вызывая сокращение и спазм.
Если это воздействие продолжительно, то развивается гипертензия. Свидетельством в пользу данного механизма развития гестоза является то, что содержание адреналина и норадреналина в моче и в крови гораздо выше у тех, у кого развился гестоз, чем в контрольной группе. Кроме того, у больных с гестозом повышено содержание норадреналина и дофамина в мышечной ткани матки. При стимуляции мышечных клеток Ca2+ поступает в цитоплазму клетки из резервуаров Са в мембране и эндоплазматической сети, а в гладкой мускулатуре дополнительный Cа2+ поступает в цитоплазму из межклеточной жидкости для того, чтобы начать сокращение.
В гладкомышечных клетках нервные импульсы не начинают сокращение, а только регулируют его. Высокое содержание Cа2+ повышает активность киназы легких цепей миозина в клетках гладкой мускулатуры, от чего зависит объем фосфорилирования легких цепей миозина. Состояние длительного сокращения гладкой мускулатуры сосудов находится в прямой зависимости от степени фосфорилирования легкой цепи миозина таким образом, что избыток Са в цитоплазме клеток гладкой мускулатуры приводит к длительному (хроническому) сокращению и спазму. Продолжающийся спазм артериальной мускулатуры приводит к разрастанию фиброзной и мышечной ткани в интиме и средней оболочке сосуда, к фибринозной дегенерации стенки сосуда, к тяжелому артериосклерозу и гипертонии.
При фибринозной дегенерации в сочетании с холестериновым эндартериитом просвет сосуда может уменьшиться более чем вдвое, и затем может наступить закупорка тромбом. При гестозе отмечается такое же поражение спиралевидных артерий матки и плацентарных артерий. Если в какой-нибудь из них образуется тромб, то инфаркт плаценты неминуем. Если гестоз заканчивается летальным исходом, то при аутопсии выявляется генерализованное поражение артерий, особенно артерий гипофиза, коры надпочечников, печени, околоклубочкового аппарата.
• Гипокальциемия в межклеточной жидкости ведет к спастическим сокращениям поперечно-полосатой мускулатуры и к экламптическим судорогам. Пониженное содержание Са в межклеточной жидкости деполяризует мембраны клеток скелетной мускулатуры и вызывает повышение активного потенциала, что ведет к избыточному поступлению Cа2+ в цитоплазму. Процесс может затрагивать также и нервы, относящиеся к этим мышцам. Это ведет к патологическому сокращению скелетных мышц, проявляющемуся в виде подергиваний, тонических и клонических конвульсивных сокращений. Артериолы головного мозга также вовлекаются в процесс, наступает их спазм, что ведет к гипоксии головного мозга и еще большему усилению судорог (рис. 3).
Проведенные в последнее время исследования показывают, что причиной повышения артериального давления является увеличение нормы содержания Са в цитоплазме гладкомышечных клеток сосудов.

Рис. 3. Схема патофизиологии гестоза во II половине беременности
Парадокс заключается в том, что согласно исследованиям:
• высокая частота развития гипертонии наблюдается в тех группах населения, где потребление Са понижено;
• у экспериментальных животных, получающих мало Са, развивается гипертензия, которая проходит при получении животными большего количества Са;
• у беременных женщин, потребляющих много Са, редко развивается гестоз, несмотря на плохие материальные условия и отсутствие пренатального наблюдения и ухода.
Что касается патофизиологии гестоза, то можно выделить две различные, но взаимосвязанные фазы: к 1 – й ф а з е относятся изменения, возникающие в I половине беременности и происходящие в результате истощения коры надпочечников; 2 – я ф а з а – это изменения, происходящие главным образом вследствие прогрессирующей недостаточности Са во II половине беременности.
Первичным нарушением в I половине беременности является в буквальном смысле слова наводнение большими количествами цАМФ, продуцируемыми в коре надпочечников после наступившего их истощения.
Вначале причинами истощения коры надпочечников служат: 1) плохое питание; 2) предшествующее заболевание; 3) синдром истощения; 4) эмоциональный стресс.
Избыток цАМФ ведет к: 1) синтезу избыточных количеств холестерола (холестерина) в коре надпочечников и холестеринемии и эндартериитам в сосудах матери, плода и плаценты; 2) избытку альдостерона, вызывающему общую задержку натрия и воды (отеки) во всех тканях, включая стенки сосудов; 3) избытку ренин-ангиотензина и спазмам сосудов ворсинок, что в соединении с холестериновыми эндартериитами ведет к дегенерации ворсинок; 4) вазопрессиноподобному эффекту в клетках почечных канальцев, что ведет к задержке воды и отекам.
Возникающий вследствие дегенеративных изменений плаценты недостаток прогестерона замещается кортизолом у матери и плода. Это усугубляет истощение коры надпочечников, что в конце концов ведет к геморрагиям, некрозу надпочечников и к прекращению продуцирования цАМФ.
Первичным нарушением во II половине беременности является спазм гладкой мускулатуры сосудов, вызываемый избыточным количеством ионов Са+ в клетках.
Недостаточность Са, которая в I половине беременности, наряду с другими факторами, приводит к истощению коры надпочечников, усугубляется во II половине беременности вследствие повышенной потребности в Са со стороны растущего скелета плода и вследствие повышения объема на 1/3 материнского метаболизма.
Недостаток Са ведет в организме к пониженному содержанию его в межклеточной жидкости, к деполяризации мембран нервных и мышечных клеток и к появлению их активного потенциала. Во время действия активного потенциала Са из межклеточной жидкости поступает в цитоплазму мышечных клеток сосудов, вызывая сокращение, а также поступает в постганглионарные симпатические нейроны, вызывая высвобождение избыточных количеств ацетилхолина. Поступление избыточных количеств ацетилхолина в постганглионарные адренергические нейроны вызывает гиперсекрецию α-адренергических катехоламинов, что ведет к еще большему поступлению Са в клетки, усугубляя спазм и гипертензию.
Поступающий в большом количестве Са2+ в клетки поперечно-полосатых мышц во время действия активного потенциала вызывает экламптические судороги.
КОНЦЕПЦИЯ АНТИОКСИДАНТНОЙ НЕДОСТАТОЧНОСТИ В ПАТОГЕНЕЗЕ ГЕСТОЗА
Абрамченко В. В., Баскаковым В. П., Соколовским В. В., Костюшовым Е. В. (1982, 1984, 1987, 1988) разработана новая концепция роли антиоксидантной недостаточности в патогенезе гестоза. Исследования, посвященные изучению клинических и теоретических аспектов патогенеза гестоза, имеют большое научное, практическое, а также социальное значение. Однако, как справедливо отмечалось проф. В. И. Бодяжиной (1987), направленность проводимых исследований ограничивается до сих пор накоплением фактических данных без углубленного их обобщения, что не позволяет создать своевременную концепцию патогенеза данной патологии и, следовательно, разработать перспективные пути ранней диагностики, своевременной профилактики и лечения.
В настоящее время мнение о существовании многих факторов, которые могут принимать участие в формировании гестоза, не утратило своего значения. Одни авторы отводят в генезе заболевания первостепенную роль экзогенным факторам: физическим, химическим, алиментарным, гелиобиологическим; другие – эндогенным: иммунологическим, гормональным, генетическим, гипоксическим и др. Вместе с тем трудно представить, что перечисленные факторы риска действуют на организм беременной каждый в отдельности, независимо друг от друга. По-видимому, состояние женщины в тот или иной период беременности определяется совместным влиянием большинства перечисленных факторов в различных комбинациях, и гестоз было бы логично рассматривать как своеобразное осложнение течения беременности, имеющее многофакторный генез.
Организм беременной через нейроэндокринные регуляторные механизмы отвечает на воздействие внешних и внутренних раздражителей общими неспецифическими реакциями. Биологический смысл этих реакций состоит в мобилизации функциональных резервов организма беременной для поддержания гомеостаза. Совокупность процессов, направленных на сохранение постоянства критических параметров внутренней среды организма во время беременности при действии разнообразных агентов, составляет механизм а д аптации, или неспецифической резистентности организма. Конечный результат мобилизации адаптационных механизмов (приспособление организма беременной к новым условиям среды или несостоятельность систем неспецифической защиты, имеющая следствием развитие болезни) зависит от ряда условий: силы и продолжительности действия раздражителя, индивидуальных генетических, возрастных особенностей организма и др.
Адаптационные неспецифические реакции, развивающиеся в ответ на действие экстремальных факторов, характеризуются наличием стадий (или фаз), имеют широкий диапазон изменений и затрагивают разные уровни структурной организации: субмолекулярный, молекулярный, надмолекулярный, субклеточный, клеточный, органо-тканевой и организменный.
От функциональной полноценности механизмов неспецифической резистентности (как в целом, так и отдельных звеньев) зависит состояние адаптационных процессов.
В связи с этим возникает принципиально важный для понимания патогенеза гестоза вопрос: за счет какого конкретного механизма адаптированный организм беременной при действии факторов риска превращается в неадаптированный?
Для получения ответа на вопрос целесообразно использовать при изучении патогенеза гестоза концепции современной биохимии. Подобный подход позволяет надеяться на успешное решение таких важных в практическом отношении задач, как оценка индивидуальной защитной «мощности» систем адаптации или разработка способов искусственного повышения неспецифической резистентности организма беременной с помощью немедикаментозных и медикаментозных средств для профилактики и лечения гестоза.
Одной из концепций, которая, по нашему мнению, может приблизить специалистов к пониманию сущности нарушений механизмов гомеостаза при гестозе, является концепция, рассматривающая антиоксидантную недостаточность организма беременной как пусковой механизм заболевания.
В соответствии с новой концепцией развития гестоза предполагается, что в ответ на действие экзогенных и эндогенных факторов риска в материнском организме возрастает интенсивность адаптивных биохимических реакций, результатом побочного действия которых является увеличение количества первичных свободных радикалов. Последние инициируют образование перекисных соединений. Эти соединения в силу высокой электрофильности способны вызывать окислительную модификацию различных биосубстратов и оказывать повреждающее действие на клетку. Проявлению патогенного действия перекисных соединений препятствует многокомпонентная антиоксидантная система организма (АОС), имеющая непосредственное отношение к молекулярным механизмам неспецифического гомеостаза.
В частности, АОС обеспечивает связывание свободных радикалов, предупреждает образование перекисей или вызывает их разрушение [Glaving, 1963]. По современным представлениям, АОС состоит из неферментативного звена – водорастворимых диализуемых (низкомолекулярные тиолы, аскорбиновая кислота – АК) и жирорастворимых (токоферол, витамины A, K, P, убихинон и др.) веществ и ферментативного звена, включающего оксидоредуктазные (глутатионредуктаза – ГР) и антиперекисные (глутатионпероксидаза, супероксиддисмутаза – СОД, каталаза и др.) ферменты. Важно подчеркнуть, что функционирование неферментативного и ферментативного звеньев АОС зависит от фонда доноров водорода. Последний поставляется за счет каталитического дегидрирования субстратов биологического окисления, осуществляемого в первой фазе пентозофосфатного цикла (ПФЦ), в процессе гликолиза, в цикле Кребса и β-окисления высших жирных кислот. Этим объясняется тесная взаимосвязь между уровнем биоантиоксиданта в тканях и активностью дегидрогеназ.
Предполагается, что экстремальные факторы риска, воздействуя на организм матери, могут провоцировать неадекватное напряжение, а затем и истощение АОС, что в конечном итоге может привести к срыву ее функционирования. Как считают авторы, патогенное воздействие факторов риска на АОС организма беременной осуществляется за счет модификации ряда биохимических и иммунохимических реакций, и, в частности, тех, которые имеют прямое или косвенное отношение к функционированию АОС. Это прежде всего окислительно-восстановительные реакции в тиол-дисульфидной и аскорбатной системах, процессы перекисного окисления липидов (ПОЛ), влияющие на уровень антиоксидантов липидной природы, активность антиперекисных ферментов и оксиредуктаз.
Правомерность высказанных суждений подтверждается результатами проведенных нами исследований.
Комплексное клиническое обследование с использованием современных клинико-физиологических и биохимических методов было проведено у 320 женщин с различными формами гестоза – отеками беременных, нефропатией I – III ст. тяжести, преэклампсией, эклампсией. Для сравнения было обследовано 46 здоровых небеременных женщин и 56 женщин с физиологически протекающей беременностью при сроке 28 – 40 нед.
Как показал анализ полученных данных, у женщин с физиологически протекающей беременностью по сравнению со здоровыми небеременными женщинами была повышена активность как неферментативного, так и ферментативного звена АОС. В частности, отмечалось увеличение содержания в крови восстановленных эквивалентов небелковой тиол-дисульфидной и аскорбатной окислительно-восстановительных систем (SH-групп и АК) и незначительное накопление их окисленных производных (SS-групп, дегидроаскорбиновой – ДАК и дикетогулоновой кислот – ДКГК). Следствием этого явилось увеличение коэффициентов SH/SS и АК/ОФ. Наряду с этим имело место повышение уровня α-токоферола на фоне умеренно выраженной активации ПОЛ, о чем свидетельствует нарастание в крови малонового диальдегида (МДА).
Активация функции ферментативного звена АОС выражалась в тенденции к увеличению содержания в крови СОД, каталазы и особенно ГР.
Как считают авторы, повышение концентрации восстановленных эквивалентов небелковой тиол-дисульфидной (представленной в системе крови в основном глутатионом) и аскорбатной окислительно-восстановительных систем связано с увеличением активности ГР, которая поддерживает восстановительный потенциал глутатиона. В свою очередь, глутатион путем восстановления ДАК способствует регенерации АК. Вместе с тем ГР катализирует восстановление окисленного глутатиона, используя для этого никотинамидадениндинуклеотидфосфат – НАДФ ⋅ H2. Образование НАДФ ⋅ H2 зависит от активности дегидрогеназ-глюкозо-6-фосфатдегидрогеназы (Г-6-ФДГ), лактатдегидрогеназы (ЛДГ), сукцинатдегидрогеназы (СДГ) – важнейших метаболических циклов, в частности ПФЦ, гликолиза, цикла Кребса, β-окисления высших жирных кислот. Образующийся при этом НАДФ ⋅ H2 может быть использован как источник атомов водорода, необходимых для нормального функционирования АОС. В свете сказанного есть все основания полагать, что повышение уровня восстановленных эквивалентов может быть обусловлено активацией дегидрогеназ.
Высказанное предположение согласуется с результатами исследований ряда авторов, выявивших активацию Г-6-ФДГ, ЛДГ, СДГ в поздние сроки физиологически протекающей беременности [Машаева Л. Л. и др., 1985; Чиладзе З. А. и др., 1981].
Говоря о причинах изменения уровня субстратов липидной природы, можно предположить, что повышение концентрации α-токоферола в крови связано с мобилизацией синтетических процессов.
Повышение в крови содержания МДА наряду с активацией антиперекисных ферментов (СОД, каталазы) свидетельствует о возрастании интенсивности реакций свободнорадикального окисления (СРО). Именно умеренная интенсивность этих реакций является условием активации АОС клеток и тканей материнского организма, играя важную роль в механизмах его адаптации к новым условиям среды и предотвращая возможность развития функциональных расстройств или патологических изменений в жизненно важных органах и системах организма беременной.
Иной характер изменений компонентов АОС был обнаружен при обследовании беременных, страдающих гестозом. Так, при всех клинических формах этой патологии были обнаружены дефицит α-токоферола и нарушения окислительновосстановительного гомеостаза в небелковой тиол-дисульфидной и аскорбатной системах. В частности, отмечалось уменьшение содержания восстановленных (SH-групп и АК) и увеличение концентрации окисленных (SS-групп, ДАК, ДКГК) эквивалентов указанных систем. Следствием этого явилось уменьшение коэффициентов SH/SS и АК/ОФ. Выявленные нарушения являются следствием окислительной модификации субстратов, о чем свидетельствует сдвиг окислительно-восстановительного равновесия в сторону окисленных форм в небелковой тиол-дисульфидной и аскорбатной системах и накопление значительных концентраций МДА в крови больных. Указанные нарушения коррелировали с тяжестью течения токсикоза. Вместе с тем можно предположить, что снижение уровня восстановленных эквивалентов обусловлено инактивацией дегидрогеназ. Естественно, это предположение нуждается в подтверждении специальными исследованиями.
Наряду с вышеизложенным в состоянии ферментативного звена АОС выявлена д вухфазность изменений активности оксидоредуктазных и антиперекисных соединений (ферментов) в зависимости от тяжести течения гестоза. При отеках беременных обнаружена активация ГР, СОД, каталазы, тогда как при нефропатии I – III ст., преэклампсии и эклампсии имело место снижение активности энзимов. По-видимому, эта двухфазность в значительной мере обусловлена разным уровнем интенсивности реакций СРО при начальной и тяжелых формах гестоза.
Результаты проведенных исследований свидетельствуют о снижении буферной емкости АОС организма беременной на фоне многократного усиления реакций АОС при всех клинических формах гестоза.
Согласно полученным данным, можно предположить, что в условиях несостоятельности антиоксидантной системы организма беременной «мишенью» для биологического действия патогенных агентов (дисульфидов, ДАК, перекисных соединений, синглетного кислорода и др.) являются белки, нуклеиновые кислоты, субстраты липидной природы, окисление которых приводит к их модификационным изменениям и, как следствие этого, к нарушениям биологической активности, синтеза, транспорта ферментов, гормонов, витаминов, медиаторов, изменениям рецепции, мембранной проницаемости, а также к энергетическому дефициту и нарушениям транспорта гемоглобином кислорода и утилизации его тканями.
Указанные нарушения приводят к радикальным изменениям режимов жизнедеятельности организма и в конечном итоге к дезинтеграции гуморальных и клеточных механизмов защиты, что и может явиться основой нарушений деятельности ЦНС и ВНС, угнетения процессов тканевого дыхания, увеличения сосудистой проницаемости и внутрисосудистых расстройств. В свою очередь, результатом указанных нарушений являются изменения циркуляторного гомеостаза и системы гемостаза, сосудистой реактивности и микроциркуляции, сердечной деятельности, а также расстройств легочного газообмена, что и приводит к развитию гипоксии тканей и органов.
В дальнейшем гемоциркуляторные нарушения в сочетании с тканевой и клеточной гипоксией приводят к функциональным и морфологическим изменениям в органах и системах жизнеобеспечения – мозге, печени, почках, фетоплацентарной системе и др.
Вследствие неспособности органов и систем, регулирующих гомеостаз, к устранению промежуточных и конечных продуктов обмена возникают метаболические расстройства, характеризующиеся избыточным накоплением в организме недоокисленных продуктов обмена, свободных радикалов, перекисных соединений, что приводит к метаболическому ацидозу. Последний способствует прогрессированию обменных нарушений, в частности истощению компонентов АОС организма беременной.
Так создается порочный круг, усугубляющий изменения гомеостаза при гестозе (рис. 4).
Таким образом, все сказанное выше позволяет предположить, что патофизиологические механизмы гестоза обусловлены антиоксидантной недостаточностью. Первостепенное значение при этом имеют нарушения, касающиеся центральных и периферических нервных механизмов, сердечной деятельности, сосудистого и внутрисосудистого русла, процессов тканевого дыхания в организме матери, которыми определяется последовательность патологических сдвигов, приводящих к отеку, гиповолемии, диспротеинемии и дисэлектролитемии, нарушениям микроциркуляции, олигурии, гипертензии, нарушению маточно-плацентарного кровообращения, гипотрофии и риску внутриутробной гибели плода, выявленных при изучении данной патологии.
Выраженность клинических проявлений заболевания зависит как от силы и длительности действия патогенных факторов риска, так и от степени истощения компонентов АОС, роль которых сводится к защите биосубстратов организма беременной от патогенного действия этих факторов.
В пользу этого предположения говорит терапевтический эффект, достигнутый при комплексном применении триады препаратов, обладающих антиоксидантными свойствами, – унитиола, АК и токоферола.
Не вызывает сомнений необходимость продолжения исследований, направленных на всестороннее и глубокое изучение молекулярных механизмов антиоксидантной защиты при гестозе. Эти работы могут позволить пересмотреть некоторые традиционные представления о патогенезе заболевания и соответственно его фармакотерапию.

Рис. 4. Схема патогенетических механизмов развития гестоза
СПОСОБЫ ЛАБОРАТОРНОЙ ДИАГНОСТИКИ КЛИНИЧЕСКИХ ФОРМ И СТЕПЕНИ ТЯЖЕСТИ ГЕСТОЗА
• Определение соотношения концентраций восстановленных и окисленных форм тиолов и аскорбиновой кислоты SH/SS и АК/ОФ в крови – способ лабораторной диагностики клинических форм и степени тяжести гестоза [Соколовский В. В., Баскаков В. П., Абрамченко В. В. и др., 1982].
В литературе последних лет уже неоднократно высказывалось мнение о том, что редуцированные формы (SH-группы и АК) являются малоинформативными и не всегда объективными показателями истинного состояния окислительно-восстановительного равновесия в тиол-дисульфидной и аскорбатной системах. Достоверное представление о состоянии равновесия в указанных системах возможно лишь на основании оценки соотношения концентраций восстановленных и окисленных форм тиолов и аскорбиновой кислоты SH/SS и АК/ОФ [Соколовский В. В. и др., 1974]. В связи с этим у больных, страдающих гестозом отечно-нефротического ряда, определялись не только редуцированные формы (АК и SH-групп), но и их окисленные производные (ОФ и SS-группы). Критериями, характеризующими состояние и степень выраженности нарушений в исследуемых системах, явились восстановительноокислительные коэффициенты SH/SS и АК/ОФ.
Выявленные нарушения характеризовались увеличением содержания окисленных форм аскорбиновой кислоты и белковых SS-групп, уменьшением редуцированных форм АК и белковых SH-групп, а также уменьшением восстановительноокислительных коэффициентов SH/SS и АК/ОФ. Указанные изменения коррелировались с тяжестью течения патологии. Вместе с тем необходимо отметить, что на фоне количественного увеличения окисленных форм аскорбиновой кислоты и белковых SS-групп в ряде случаев в крови больных одновременно определялось относительно высокое содержание редуцированных форм АК и SH-групп. В этих случаях нарушения в белковой тиол-дисульфидной и аскорбатной системах только лишь по количественному содержанию восстановленных форм АК и белковых SH-групп, как это предлагают Р. Л. Шуб (1961), К. В. Воронин и соавт. (1978), Д. З. Григорян (1981), без учета показателей их окисленных форм (ОФ и SS-групп), указывают на незначительные сдвиги окислительно-восстановительного равновесия в исследуемых системах. Показатели АК и SH-групп свидетельствовали о легком течении патологии. В то же время на основании клинической картины заболевания у больных было диагностировано тяжелое течение гестоза.
Таким образом, редуцированные формы АК и белковых SH-групп являются малоинформативными и не всегда объективными показателями истинного состояния окислительновосстановительного равновесия в белковой и аскорбатной системах крови. Использование их в акушерской практике в качестве критериев, характеризующих состояние и степень выраженности нарушений в тиол-дисульфидной и аскорбатной системах крови больных, а также тестов лабораторной диагностики клинических форм гестозов может привести к ошибочному заключению о состоянии равновесия в указанных окислительно-восстановительных системах и, следовательно, о тяжести клинического течения патологии.
Предлагаемые восстановительно-окислительные коэффициенты и АК/ОФ исключают возможность подобной ошибки, являются объективными и информативными показателями, характеризующими истинное состояние окислительно-восстановительного равновесия в тиол-дисульфидной и аскорбатной системах крови больных, что позволяет рекомендовать их в качестве достоверных ранних прогностических и диагностических тестов.
• Способ лабораторной диагностики клинических форм и степени тяжести гестозов путем определения показателей стабильности липопротеиновых комплексов в сыворотке крови.
Нарушению синтеза и стабильности липопротеиновых комплексов (ЛПК) придается большое значение в патогенетических механизмах увеличения мембранной проницаемости и развитии гипоксии при различных заболеваниях. Имея в виду важность этой информации для понимания патогенеза гестоза, определялась стабильность ЛПК в сыворотке крови больных, изучалась их роль в биохимических механизмах, лежащих в основе сосудистых нарушений и развитии гипоксии при данной патологии. Для определения прочности связи липид – белок в ЛПК использован метод Л. Л. Делямуро (1968).
Результаты исследования показали, что если в поздние сроки нормально протекающей беременности имеется лишь тенденция к изменению стабильности ЛПК, то при беременности, осложненной гестозом, дестабилизация ЛПК явно выражена, при этом она тем значительнее, чем тяжелее течение заболевания. Особенно ценным является то, что изменения показателей стабильности ЛПК определялись раньше выраженных клинических симптомов патологии. Иными словами, опережали клиническую картину заболевания.
Кроме того, отмечалась нормализация показателей стабильности ЛПК при клиническом выздоровлении больных.
Учитывая значение обнаруженных нарушений в патогенетических механизмах развития патологии, пришли к выводу о целесообразности определения показателей стабильности ЛПК сыворотки крови с целью использования их в акушерской практике в качестве ранних прогностических и диагностических тестов оценки развития гестозов, контроля эффективности лечения и определения сроков госпитализации больных с данным заболеванием [Соколовский В. В., Баскаков В. П., Абрамченко В. В., Варфоломеев Д. И., Костюшов Е. В., 1982].
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ АНТИОКСИДАНТОВ В АКУШЕРСКОЙ ПРАКТИКЕ
Выраженность клинических проявлений гестоза предположительно зависит от силы и длительности действия патогенных факторов и от степени истощения компонентов биоантиоксидантной системы (небелковой и тиол-дисульфидной и аскорбатной окислительно-восстановительных систем).
Исходя из этого, с целью коррекции выявленных нарушений в тиол-дисульфидной и аскорбатной окислительно-восстановительных системах в общепринятую схему лечения гестоза были дополнительно включены лекарственные средства, обладающие антиоксидантными свойствами, – 5 % раствор унитиола и 5 % раствор натриевой соли аскорбиновой кислоты.
Комплексная интенсивная терапия проведена 93 больным гестозом: 43 (контрольная группа) получали лечение по общепринятой схеме; 50 (основная группа) проводилась терапия, при которой в общепринятую схему лечения была включена комбинация указанных препаратов. Показатели состояния тиол-дисульфидной и аскорбатной систем с вычислением коэффициентов SH/SS и АК/ОФ определялись до начала и на 6-е сутки лечения.
Первая серия исследований.43больных контрольной группы (отеки беременных, нефропатия I – III ст.) получали лечение по общепринятой схеме – диетотерапию, гипотензивные препараты, магнезиальную терапию, транквилизаторы, спазмолитики, мочегонные, антигистаминные препараты и др. Кроме того, проводилась инфузионная терапия – гемодез, реополиглюкин, комплексы аминокислот и альбуминов.
Препараты назначались по показаниям в зависимости от формы и степени тяжести патологии. Несмотря на клиническое улучшение течения заболевания, показатели величин коэффициентов SH/SS, АК/ОФ, используемых в качестве объективных критериев, характеризующих истинное состояние окислительно-восстановительного равновесия в тиол-дисульфидной и аскорбатной системах, и устойчивости ЛПК крови по сравнению с показателями до лечения существенно не изменились, что рассматривается как свидетельство продолжающегося патологического процесса.
Вторая серия исследований. 50 больным основной группы (отеки беременных, нефропатия I – III ст.) кроме препаратов, предусмотренных общепринятой схемой лечения, вводили 5 % раствор унитиола (из расчета 1 мл на 10 кг массы тела на введение) в сочетании с 5 % раствором натриевой соли аскорбиновой кислоты (из расчета 2 мл на введение) – 3 инъекции в сутки.
Терапевтический эффект выражался в нормализации исследуемых показателей (коэффициентов SH/SS, АК/ОФ и устойчивости ЛПК крови) у больных с отеками и нефропатией I ст. и значительном их улучшении у больных с нефропатией II и III ст. по сравнению с показателями до лечения. Наряду с этим отмечалось клиническое улучшение течения заболевания.
Проводилось сравнение терапевтического эффекта у 50 больных основной группы с результатами лечения 43 больных контрольной группы. Анализ полученных данных показал, что при включении унитиола с аскорбиновой кислотой в комплекс общепринятых терапевтических средств у больных основной группы повышалась эффективность лечения и значительно снижались сроки лечения по сравнению с больными контрольной группы. В частности, стойкое клиническое улучшение состояния отмечено у 33 (76,74 %) больных контрольной группы на 8,24 ± 0,58-й день лечения, в то время как у 48 (96 %) больных основной группы стойкое улучшение наступало на 5,12 ± 0,48-й день (p < 0,001). У этих больных быстрее нормализовалось артериальное давление, уменьшались отеки, улучшались клинические и биохимические показатели крови.
Изучение особенностей течения родов у обследованных больных показало, что при применении комплексной терапии унитиола с аскорбиновой кислотой снизилось в 3 раза число преждевременных и запоздалых родов, уменьшилось в 3 раза число патологических кровопотерь и в 2,5 раза – число оперативных вмешательств. Средняя продолжительность родов (в часах) сократилась с 16,4 ± 3,8 в контрольной группе (лечение по общепринятой схеме) до 9,6 ± 2,3.
• Положительный терапевтический эффект, полученный при применении унитиола с аскорбиновой кислотой, подтверждает патогенетическую роль тиол-дисульфидной и аскорбатной окислительно-восстановительных систем в развитии гестоза беременных и позволяет рекомендовать их применение в комплексном лечении данной патологии.
• Вторым показанием к сочетанному применению унитиола с аскорбиновой кислотой является гипоксия плода. Данные объективного изучения состояния плода методом кардиотокографии показали: при однократном применении указанных средств у 36 рожениц, страдающих гестозом, состояние сердечной деятельности плода после внутримышечного (22 роженицы) и внутривенного (14 рожениц) введения унитиола с аскорбиновой кислотой в I периоде родов характеризовалось статистически достоверным увеличением внутриминутных колебаний частоты сердцебиения плода – с 4,05 ± 0,28 до 6,04 ± 0,28 уд./мин. (p < 0,001) после внутримышечного и с 4,22 ± 0,35 до 6,66 ± 0,34 уд./мин. (p < 0,001) после внутривенного введения препаратов, а также повышением миокардиального рефлекса с 16 ± 1,34 до 20,05 ± 1,12 (p < 0,05) после внутримышечного и с 13,11 ± 2,61 до 18,72 ± 1,14 (p < 0,05) после внутривенного введения препаратов, что указывает на улучшение состояния плода.
• Третьим показанием к применению комбинации унитиола с аскорбиновой кислотой является лечение слабости родовой деятельноси (СРД), которое проведено у 46 рожениц в I периоде родов. Данные клиники и наружной многоканальной гистерографии, которая проводилась на протяжении всего I периода родов, показали статистически достоверное повышение маточной активности, выражающееся в увеличении амплитуды с 8,76 ± 0,44 до 11,39 ± 0,61 мм (p < 0,001) после внутримышечного (32 роженицы) и с 9,53 ± 0,9 до 14,37 ± 1,15 мм (p < 0,05) после внутривенного введения (14 рожениц) препаратов и возрастанием частоты сокращений матки за 10 мин. с 3,13 ± 0,34 до 4,22 ± 0,31 (p < 0,05) после внутримышечного и с 3,18 ± 0,16 до 4,37 ± 0,35 (p < 0,001) после внутривенного введения.
Это дает основание считать, что применение унитиола и аскорбиновой кислоты в родах способствует улучшению обменных процессов в миометрии, следствием чего является повышение маточной активности.
Полученные данные свидетельствуют о необходимости применения смеси указанных антиоксидантов в акушерской практике в комплексной терапии гестоза с целью интра- и антенатальной защиты плода, а также в качестве средств, усиливающих родовую деятельность.
КОНЦЕПЦИЯ ГЕНЕЗА ГИПОКАЛЬЦИЕМИИ ПРИ ГЕСТОЗЕ
Общеизвестно, что поддержание кальциевого гомеостаза является одним из важнейших условий нормального функционирования жизненно важных органов и систем.
С этой точки зрения трудно переоценить значение гипокальциемии в возникновении целого каскада нефизиологических реакций в системе мать – плацента – плод во время беременности, осложненной гестозом. Вместе с тем вопрос о молекулярных механизмах, лежащих в основе дефицита кальция при рассматриваемой патологии, до сих пор остается открытым.
Так, в исследовании Roelofsen et al. (1988) изучен метаболизм Ca и Mg в моче и крови при нормальной беременности и при беременности, осложненной гипертензией, или при задержке роста плода. У всех обследуемых уровень Ca в течение беременности снижался. При этом содержание ионизированного Ca не менялось. Концентрация Mg в крови снижалась в начале беременности и оставалась на одном уровне в III триместре. Отмечено, что концентрация Mg в крови повышена при задержке роста плода. Экскреция Ca и Mg с мочой возрастает при беременности и не зависит от осложнений. Таким образом, метаболизм Ca и Mg слабо меняется при патологии беременности.
В противоположность этим данным в работе Taufield et al. (1987) была поставлена задача: может ли гипокальциурия являться прогностическим критерием развития токсикоза. С этой целью авторы выделение Ca с мочой определяли у 40 беременных с гипертензиейиу10женщин с неосложненным течением беременности. Содержание ионизированного Ca и P в сыворотке крови в обеих группах было одинаковым, экскреция Ca с мочой у здоровых беременных составляла 313 ± 140, при транзиторной гипертензии – 248 ± 138, при гипертонической болезни – 233 ± 41, при токсикозе – 42 ± 29, при сочетанной его форме – 78 ± 49 мг/сут. Фракционная экскреция Ca с мочой была ниже при гестозе, чем в других группах.
Экскреция Na с мочой оказалась одинаковой. Снижение экскреции Ca с мочой может служить четким лабораторным критерием гестоза. Лечение Mg и Ca приводит к увеличению выделения Ca с мочой. Гипокальциурия служит для дифференцирования гестоза от других заболеваний беременных, сопровождающихся гипертензией. Остается неясным, может ли гипокальциурия являться прогностическим критерием развития гестоза.
В этой связи значительный интерес представляют экспериментальные данные о зависимости кальциевого обмена от состояния окислительно-восстановительного гомеостаза и прежде всего тиол-дисульфидной и аскорбатной систем организма [Мусил Я., 1985; Bruyn et al., 1977; Gambardella, Richardson, 1977].
Отсутствие в литературе сведений о роли тиол-дисульфидной и аскорбатной окислительно-восстановительных систем в молекулярных механизмах генеза гипокальциемии при гестозе послужило основанием для настоящей работы.
С этой целью комплексному клиническому обследованию с использованием современных клинико-физиологических и биохимических методов подверглись 228 женщин в возрасте от 18 до 40 лет, которых распределили следующим образом.
В 1-ю группу вошли женщины с физиологически протекающей беременностью при сроке 38 – 40 нед., в том числе и в начале нормальных родов (всего 38 человек). Указанная группа была взята в качестве контроля (табл. 1).
Таблица 1
Биохимические показатели плазмы крови больных гестозом


* Показатель статистически достоверно отличается от своего значения в контрольной группе (p < 0,05).
Последующие четыре группы (190) составили женщины с беременностью 32 – 40 нед., осложненной гестозом беременных, распределенные на основании клинических признаков заболевания по формам и степени тяжести согласно принятой классификации: 2-я группа – отеки беременных (80), 3-я – нефропатия I ст. (66), 4-я – нефропатия II ст. (26), 5-я – нефропатия III ст. (18).
У всех обследуемых определялось содержание оксалатов в моче, проводилось биохимическое исследование крови с целью изучения состояния тиол-дисульфидной системы, аскорбатной окислительно-восстановительной системы и кальциевого гомеостаза.
В работе использованы методы прямого и обратного амперометрического титрования сульфгидрильных (SH) и дисульфидных (SS) групп, раздельного определения редуцированной формы аскорбиновой кислоты (АК) и ее окисленных форм – дегидроаскорбиновой (ДАК) и дикетогулоновой (ДКГК) кислот [Соколовский В. В. и др., 1974, 1977]. Концентрация кальция в плазме крови определялась методом плазменной фотометрии. О наличии оксалатов судили на основании данных микроскопического осадка мочи. Получены также данные содержания стероидных гормонов в сыворотке крови в контрольной группе с использованием радиоиммунологического метода с применением стандартных наборов KIT фирмы «CEA – IRE – SORIN». Результаты исследований были подвергнуты математической обработке методами вариационной статистики [Беленький М. Л., 1963] (табл. 2).
Таблица 2
Выраженность оксалатурии в моче больных гестозом

Анализ полученных данных показал (см. табл. 1 и 2), что развитие гестоза сопровождается глубокими нарушениями состояния окислительно-восстановительного равновесия в тиолдисульфидной и аскорбатной системах плазмы крови больных по сравнению с контролем. Эти нарушения характеризуются уменьшением содержания редуцированных форм (SH-групп и АК) указанных систем и увеличением концентрации их окисленных производных (SS-групп и ДАК + ДКГК), что наиболее наглядно проявляется в уменьшении величин коэффициентов SH/SS и АК/ОФ. Наряду с этим обнаружен дефицит кальция в плазме крови и увеличение оксалатов в моче больных. Причем в ходе проведенных исследований установлена прямая зависимость тяжести клинического течения патологии и степени выраженности указанных нарушений. Особо необходимо акцентировать внимание на то, что интенсивность сдвигов окислительно-восстановительного равновесия в тиол-дисульфидной и аскорбатной системах, в свою очередь, коррелировала с выраженностью гипокальциемии и оксалатурии в плазме крови больных (рис. 5).
Необходимо отметить, что в контрольной группе не удалось выявить статистически достоверных изменений со стороны содержания стероидных гормонов и концентрации ионов кальция при сравнении показателей при 38 – 40 нед. беременности и во время начала родов. Так, эстриол соответственно составлял 264,7 ± 35,7 и 205,1 ± 28,3 мкг/мл, эстрадиол 26,93 ± 3,16 и 18,16 ± 2,8 мкг/мл, содержание прогестерона незначительно уменьшалось с 179,83 ± 18,25 до 102,63 ± 7,53 мкг/мл (p < 0,05), концентрация ионов кальция оставалась стабильной – 2,46 ± 0,08 и 2,26 ± 0,04 ммоль/л.
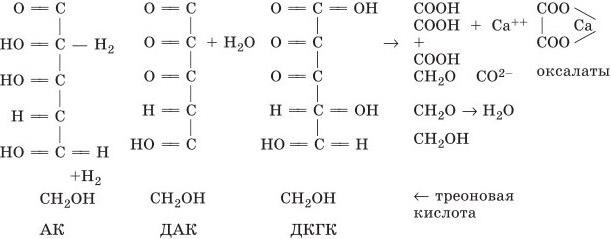
Рис. 5. Механизм образования оксалатов в плазме крови больных гестазом
В свете этих данных возможные причины гипокальциемии при гестозе беременных могут состоять в следующем.
Во-первых, окисление редуцированной формы АК приводит к накоплению ее окисленных производных – ДАК и ДКГК кислот. Последняя (ДКГК), как известно, являясь необратимо окисленной формой АК, в свою очередь, расщепляется на щавелевую и треоновую кислоты. Появление высоких концентраций щавелевой кислоты в различных средах организма при усилении процессов окисления АК обнаружили ряд исследователей [Мусил Я., 1985; Wapnick et al., 1968; и др.]. Исходя из этого, представляется, что биологический эффект ДКГК обусловлен появлением в организме больных одного из продуктов ее расщепления – щавелевой кислоты в значительном количестве, которая, взаимодействуя с ионами кальция плазмы крови, образует оксалаты, частично выводящиеся с мочой, вследствие чего происходит потеря кальция организмом. В пользу этого заключения свидетельствуют данные нашей работы. В частности, в результате проведенных исследований была обнаружена корреляционная зависимость между увеличением содержания ДКГК в плазме крови больных, с одной стороны, и уменьшением уровня кальция в плазме крови и увеличением концентрации оксалатов в моче больных – с другой. Правомерность высказанного предположения подтверждается результатами исследований ряда авторов, выявивших увеличение концентрации оксалатов в моче при введении в организм АК в больших количествах на фоне повышенной оксидазной активности [Мусил Я., 1985; и др.].
Во-вторых, известно, что появление оксалатов в организме может быть непосредственно связано с нарушениями процессов их оксалирования (распада). В то же время механизмы нарушения оксалирования обусловлены снижением активности ряда тиоловых ферментов: оксалатдекарбоксилазы (4.1.1.2), оксалат-оксидазы (1.2.3.4), оксалат-КоА-лигазы (6.2.1.8), оксалат-КоА-трансферазы (2.8.3.2)1. Активность тиоферментов, как известно, определяется состоянием тиол-дисульфидной системы организма, сдвиг которой в сторону окисления приводит к их инактивации. Поэтому есть все основания полагать, что нарушениями окислительно-восстановительного равновесия в тиол-дисульфидной и аскорбатной системах, обнаруженными при гестозе, может быть обусловлено снижение активности тиоловых ферментов, принимающих участие в процессах оксалирования. В этих условиях возможность образования и присутствия оксалатов в организме больных становится еще более вероятной.
Естественно, предлагаемая концепция не исчерпывает всей сложности возможного механизма гипокальциемии при гестозе. Тем не менее развивающиеся при данной патологии нарушения окислительно-восстановительного равновесия играют важную роль в генезе гипокальциемических состояний.
Таким образом, при гестозе закономерно возникают нарушения окислительно-восстановительного гомеостаза с уменьшением редуцированных и увеличением окисленных форм компонентов тиол-дисульфидной и аскорбатной систем. Эти нарушения в количественном выражении прямо пропорциональны степени выраженности клинических проявлений гестоза; одним из наиболее вероятных механизмов гипокальциемии является увеличение щавелевой кислоты как следствие описанного сдвига окислительно-восстановительного гомеостаза на фоне резкого снижения активности тиоловых ферментов и угнетения естественного механизма оксалирования.
РОЛЬ ФИКСИРОВАННЫХ В ПЛАЦЕНТЕ ИММУННЫХ КОМПЛЕКСОВ В ПАТОГЕНЕЗЕ ГЕСТОЗА
Гестоз является одним из наиболее тяжелых видов акушерской патологии и встречается у 12 – 20 % беременных. Несмотря на многочисленные исследования патогенетических механизмов развития заболевания и появление новых методов лечения гестоза, он продолжает занимать ведущее место среди причин материнской и перинатальной заболеваемости и смертности. Гестоз является причиной материнской смертности в 9,6 – 20 % случаев, а перинатальная смертность в 3 – 4 раза превышает этот показатель у женщин без гестоза [Айламазян Э. К., 1993; Репина М. А., 1988; Савельева Г. М. 1996]. При гестозе хроническая гипоксия плода и асфиксия новорожденных отмечается в 17 – 58,3 % случаев, гипотрофия плода и новорожденного – в 14,6 – 20,8 %. В неонатальном периоде у детей от матерей с гестозом часто наблюдаются такие осложнения, как нарушение мозгового кровообращения, постгипоксическая энцефалопатия, синдром дыхательных расстройств, нарушение процесса адаптации к внеутробной жизни [Озерец Н. А. и др., 1996]. Высокая частота гестоза и характер его осложнений для матери и плода диктуют необходимость дальнейшего изучения патогенеза этого заболевания в поисках новых методов профилактики и лечения.
В патогенезе гестоза значительную роль играют нарушения в системе иммунитета [Аничкова С. И. и др., 1992; Сидорова И. С., 1996; Vinatier D. et al., 1995]. Изучению особенностей иммунной системы матери при гестозе посвящены многие исследования, результаты которых свидетельствуют о значительном отличии иммунологического статуса беременных с гестозом от его характеристики при физиологической беременности. Ряд авторов [Старостина Т. А. и др., 1992; Калашникова Е. П., 1989; Redman C. W. G., 1991; Faulk W. P. et al., 1983] отмечают повышение содержания циркулирующих в крови и фиксированных в плаценте иммунных комплексов у беременных с гестозом по сравнению со здоровыми женщинами. Однако роль иммунных комплексов в развитии этой патологии, частота выявления при различных степенях тяжести гестоза, их влияние на клинические проявления заболевания не изучены.