Часть I
Введение к Части I
В более чем двухвековой истории систематизации химических элементов наибольших успехов в XIX веке достигли британец Джон Александр Ньюлендс, германец Юлиус Лотар Мейер и россиянин Дмитрий Иванович Менделеев. В последней прижизненной Таблице Менделеева было IX групп:

Рис. 1. Последняя прижизненная Периодическая Таблица Д.И. Менделеева
Как видно на рис. 1, у Менделеева была нулевая группа элементов, которая содержала доводородные элементы под номером, очевидно, 0 – Ньютоний (эфир), а под номером 1 – Короний. Водород, по-видимому, имел номер 2, Гелий – номер 3…., и т. д. Дмитрий Иванович почему-то не ставил номера элементам, видимо, полагая это очевидным по порядку расположения элементов в его Периодической Таблице: слева направо в рядах (писал и говорил именно о рядах, а не о периодах) и сверху вниз самих рядов (периодов). В восьмой (девятой от нулевой) группе были только триады: Fe, Со, Ni; Ru, Rh, Pd; Os, Ir, Pt.
Музыкальная октавная гармония, воплощённая в «Законе октав» Ньюлендса в его систематизации химических элементов, имела столь завораживающее воздействие на людей, что 120 лет после открытия Менделеевым Периодического Закона в Мире пользовались Периодической Таблицей химических элементов из VIII гомологических групп элементов-аналогов. В постменделеевский период вплоть до 1989 г. наиболее популярной и повсеместно используемой была Периодическая Таблица вида:

Рис. 2. Наиболее распространённая форма Периодической Таблицы химических элементов до 1989 г.
По сравнению с последней прижизненной Периодической Таблицей Менделеева нулевой группы вместе с нулевым элементом, Коронием и инертными элементами нет, первый номер у Водорода, Гелий и инертные газы из бывшей нулевой группы перенесены в группу VIII, где размещены и триады благородных металлов. Гелий поднялся на один ряд выше и стоит номером 2 в одном ряду с Водородом через 6 групп в крайней правой главной подгруппе VIII группы.
Размещение Гелия над Неоном и другими инертными газами было вполне понятно и оправдано во времена Менделеева, когда не знали о строении атомов, и не было квантовой механики. В самом деле, газ Гелий более инертен, чем все другие благородные газы и имеет наименьшую атомную массу среди них. Поэтому логично было ставить Гелий на первое место типозадающего элемента в гомологической группе инертных атомарных элементов-аналогов.
Но, когда открыли строение атомов, и было установлено, что в явлении периодичности свойств химических элементов лежит квантово-механическая основа формирования электронных оболочек, становится непонятным положение Гелия на рис. 2. Это в таблицах из VIII групп. Но, такая же картина сохраняется и в современных, после 1989 г., типах Периодических Таблиц с 18-ю группами.

Рис. З.Периодическая Таблица химических элементов с 18-тью группами, рекомендуемая IUPAC с 1989 г.
Уже с беглого взгляда на рис. 2 и рис. З отчётливо видно, будто Гелий вырван из естественного положения рядом с Водородом и перекинут на самую правую и верхнюю позицию над Неоном. При этом на обоих рис. 2 и 3 видно, что ячейка с Гелием, по цвету такая же, как у двух групп s-элементов. Как s-элемент Гелий может быть типозадающим в группе p-элементов? Авторы этих Таблиц, по-видимому, таким вопросом не задавались. Если же задавались, то предпочли не выходить за рамки сложившихся в XIX веке традиций. А, ведь, Таблицы на рис. 2 и рис. 3 создавались в середине XX века, когда строение атомов и формирование электронных оболочек на квантово-механической основе были повсеместно признаны и приняты.
Между тем, существует Периодическая Таблица химических элементов по версии Жанета с четырьмя s-элементами в начале (на самом верху, справа, над всеми остальными s-элементами) Таблицы, которую он разработал ещё в конце 20-х годов XX века.

Рис. 4. Периодическая Таблица химических элементов по версии Жанета
Прямоугольные блоки s-, р-, d-, f-элементов компактны и непрерывно последовательны справа налево. Расцветка блоков несколько отличается от привычных для нас красного, желто-оранжевого, синего и зелёного цветов. Но расцветка условна и может отличаться в зависимости от предпочтений и традиций разных народов.
Инертный Гелий возглавляет группу химически очень активных щелочноземельных металлов. Это для подавляющего большинства образованных (со средних школ, лицеев и гимназий) людей совершенно непривычно, более того, не приемлемо. Но если исходить из строения электронных оболочек атомов, то такое расположение Гелия научно оправдано.
Гелий является s-элементом, как щелочноземельные металлы, тогда как все благородные газы, над которыми его традиционно ставят в роли типозадающего в гомологической группе инертных элементов-аналогов, являются р-элементами.
Видно, что проблемы с общепринятыми Периодическими Таблицами химических элементов довольно глубокие. Они связаны с тем, что до сих пор у Периодического Закона химических элементов нет логического обоснования. Для фундаментальных Законов Природы, каковым, безусловно, является Периодический Закон химических элементов, логическим обоснованием может и должно быть математическое обоснование на математических принципах.
В истории систематизации химических элементов было множество попыток охватить все элементы математической формулой. Были попытки и с тригонометрическими, и с экспоненциальными, и со степенными функциями. Но все они потерпели неудачу. По-видимому, по причине того, что фундаментальные законы природы на самом деле просты, и выражаться должны простыми уравнениями. Как Закон всемирного тяготения, Закон электрического взаимодействия, Закон интенсивности света. И в самом деле, выжил и господствовал на протяжении 120 лет простейший математический закон октав из музыкальной гармонии, заложенный Ньюлендсом. Но и здесь были изначально и нарастали со временем проблемы, которые через сто с лишним лет привели к отказу от октавной простоты. В самом деле, Закону октав подчиняются только элементы s и р блоков, от Лития до Оганесона. Химические элементы с номерами 119 и 120 ещё не обнаружены и не синтезированы. Элементы s-, p-блоков отцвечены соответственно бардово-красным и жёлтым цветами на рис. 3. Полных рядов из октавы (восьми) «красных и жёлтых» химических элементов только 6, а элементов соответственно 48 из 118 известных на сегодня химических элементов. Это примерно 40,7 % всех химических элементов. Для истинного, математически выраженного Закона Природы, правомерно ожидать 100 %-го охвата элементов.
Индуктивный (от частного к общему) подход к систематизации химических элементов по мере открытия всё новых элементов оправдан с исторической точки зрения. Но к сегодняшнему дню открытия и синтез новых химических элементов подошли к верхнему пределу множества химических элементов. Настало время для дедуктивной (от общего к частному) систематизации множества химических элементов. Это не означает пренебрежения индуктивным методом, в особенности результатами, полученными к сегодняшнему дню. Напротив, результаты дедуктивного выявления общих математических закономерностей в распределении химических элементов (номеров) должны сопоставляться с известным ныне порядком (нумерацией) распределения химических элементов, полученным индуктивно в течение более двухсот лет.
Наука и просвещение/образование
Обучение, учёба – освоение познанного. Познание – продвижение к непознанному, от освоенного. Наиболее динамичные продвижения в познании за последние 2–3 века сделаны в математике, физике, химии. Тон задавала математика. Что такое теорема? Она формулируется в начале математического исследования, т. е. задаётся сформулированная цель. Остальное – доказательство теоремы, т. е. продвижение к сформулированному в теореме утверждению (истине). Хоть и не столь чётко как в математике, но и в теоретической физике, и в теоретической химии процесс познания идёт по такой же схеме, по такому же алгоритму. Физика и химия – наиболее математизированные естественные науки.
И мы изначально поставим цель – решить Менделеевскую Проблему отсутствия математической формулы у фундаментального естественного Закона Природы – Периодического Закона химических элементов Д.И. Менделеева. Решение будем искать в виде числовой (номерной) систематизации химических элементов.
Всякое научное достижение без его истории, истоков выглядит оторванным, изолированным от общего процесса и потока познания. Поэтому обратимся к числовым истокам и идеям систематизации химических элементов.
1. Двумерное представление множества химических элементов
Изначально, ещё с конца XVIII века химические элементы выстраивали по порядку возрастания атомных весов (масс). Всё множество химических элементов, а их уже в первой четверти XIX века насчитывалось более десятка, выстраивали в ряд. К 60-ым годам XIX века число химических элементов превысило уже 60. Ряд химических элементов стал слишком длинным. Скорее всего, это было главной причиной отступления от прямолинейного отображения множества химических элементов. Первым в этом направлении следует признать Александра де Шанкуртуа, который в 1862 году представил цилиндрическую форму отображения множества химических элементов.
В 1864 году Александр Ньюлендс предложил «закон октав» в двумерном размещении множества химических элементов. Годом позже Лотар Мейер предложил две таблицы по 28 и 22 элемента. Через 5 лет, в 1869 году представил свою Периодическую Таблицу химических элементов Дмитрий Иванович Менделеев. Именно он впервые сформулировал Периодический Закон распределения в системе химических элементов. До 1989 года в мире пользовались короткопериодной Периодической Таблицей химических элементов Д.И. Менделеева с некоторыми изменениями. Примечательно, что в короткопериодной Периодической Таблице химических элементов придерживались «закона октав» Ньюлендса. Таким образом, именно в 60-х годах XIX века произошёл переход от одномерного множества химических элементов к их двумерному множеству. Периодический Закон химических элементов, говорят, «приснился» Д. И. Менделееву именно на двумерном табличном представлении множества известных ему химических элементов.
Как бы то ни было на самом деле, но то, что Периодический Закон распределения химических элементов был выявлен на двумерном табличном представлении химических элементов – исторический факт.
Имеет смысл рассмотреть некоторые конкретные формы таблиц, в клеточках которых будем размещать химические элементы в последовательности 118 номеров, полученной к настоящему времени.
2. Двумерная числовая таблица 10 × 12
Возьмём множество первых 120 чисел натурального ряда, которыми пронумеруем клеточки-квадратики в таблице 10 × 12. Это наиболее простая таблица для чисел привычной всем десятеричной системы счисления. На рисунке ниже представлена такая таблица.

Рис. 5. Таблица 10 × 12 первых 120 чисел натурального ряда
Видна периодичность во всей таблице всех чисел первого разряда в 1-12 строках. Вся таблица периодична. В десятеричной системе счисления так и должно быть. Разряд из 1-10 задаёт (определяет) периодичность любых таблиц из строк в 10 чисел.
Посмотрим, как будет выглядеть таблица 10 × 12 с 118-ю известными на сегодня химическими элементами.

Рис. 6. Номера химических элементов в таблице 10 × 12
Все химические элементы делятся на 4 вида (блока). Они называются блоками s-, р-, d-, f-элементов или s-, р-, d-, f-блоками. Это из квантовой химии, довольно сложной науки. Но для нас важно сейчас только то, что любой химический элемент обязательно является членом одного из 4-х блоков. Нет химических элементов вне этих блоков. Все s-элементы у нас (в СНГ, со времён СССР) традиционно окрашивают в красный цвет, р-элементы – в жёлто-оранжевый, d-элементы – в синий и f-элементы – в зелёный.
Периодичность химических элементов означает, что какие-то ряды полностью повторяются в своих расцветках хотя бы один раз. На рис. 6 таких рядов только 4 из 12, т. е. только ЪЪ,Ъ%. Из этого можно сделать вывод: 12-ти рядная таблица из 10 химических элементов в рядах не пригодна для числового шифрования Периодического Закона.
3. Двумерная числовая таблица 8 × 15
Здесь также 120 чисел. Но 8-ми разрядный «октавный Закон» Ньюлендса был математическим законом Периодической Таблицы химических элементов до 1989 года. Поэтому и мы будем ожидать высокой периодичности во множестве химических элементов в таблице 8 × 15. На рисунке ниже представлена таблица 8 × 15 химических элементов.

Рис. 7. Таблица 8 × 15 химических элементов
Повторяющихся строк 9 из 15 или 72 химических элемента из 118. Это составляет 61 %. Действительно большой процент периодизуемости. Но до 100 % далеко.
Если первые 1–4 химических элемента вынести за пределы таблицы, то получим:

Рис. 8. Таблица 8 × 15 с вынесенными за пределы таблицы первыми 1–4 химическими элементами
Здесь мы имеем 11 периодизирующихся рядов, т. е. 88 из 118 химических элементов. Это составляет около 74,6 %, что выше предыдущего случая на 13,6 %. Хорошая периодизируемость, но также далека от 100 процентной.
4. Двумерная числовая таблица 16 × 8
16-разрядную таблицу рассматриваем в связи с тем, что она кратна 8-ми разрядной таблице, а на 8-ми разрядной таблице достигли максимальной периодичности в 74,6 %. В этом случае в таблице 128 числовых элементов. Таблица химических элементов для этого случая:

Рис. 9. Таблица 16 × 8 химических элементов
Элементы 121–128 относятся к следующему за f-бло-ком g-блоку ожидаемых химических элементов. Но их пока нет. Поэтому химических элементов и в этом случае только 118. В такой таблице имеются 4 периодизи-рующихся рядов, и в них 64 химических элемента. Они составляют примерно 54,23 %. Это намного меньше максимального 74,6 %. Уменьшать или повышать далее разрядность таблиц смысла не имеет. Мы получили весь диапазон «хорошей» периодизируемости химических элементов. К искомому результату – 100 %-му охвату всех химических элементов не подошли и близко.
Вывод: разрядность чисел не может служить основой систематизации химических элементов. Следует искать другие закономерности.
5. Специальное распределение натуральных чисел
1. Квадрат натуральных чётных чисел (2n)2 при n = 1; 2; 3; 4:
(2n)2 = 4; 16; 36; 64 (1)
2. Квадрат любого числа n равен сумме последовательных нечётных чисел:
n2 = Σ(2n –1) (2)
Это подтверждается последовательной подстановкой каждого из n = 1; 2; 3; 4:
Σ(2n –1) = 1; 1 + 3; 1 + 3 + 5; 1 + 3 + 5; 1 + 3 + 5 + 7
Тогда: (2n)2 = 2[2(1); 2(1 + 3); 2(1 + 3 + 5); 2(1 + 3 + 5 + 7)], (3)
и
(2n)2 = 2(2n2) = 2(2; 8; 18; 32) (4)
Получились числовые сдвоенности – Диады из числовых Монад: 2; 8; 18; 32.
Просуммируем все Диады (4) с учётом (2), (3) и правила: «от перестановки мест слагаемых сумма не изменяется».
Σ2(2n2) = 2Σ2Σ(2n –1) = 2{2[(1) + (1 + 3) + (1 + 3 + 5) + (1 + 3 + 5 + 7)]} = 2(2) + 2(2 + 6) + 2(2 + 6 + 10) + 2(2 + 6 + 10 + 14) = 2(2) + 2(6 + 2) + 2(10 + 6 + 2) + 2(14 + 10 + 6 + 2)
Полученный результат представляет полное количество KD чисел в четырёх Диадах из пар (2 перед скобками) Монад, которые состоят последовательно из 1, 2, 3, 4 слагаемых (в скобках). В сумме они составляют:
KD = 2(2) + 2(6 + 2) + 2(10 + 6 + 2) + 2(14 + 10 + 6 + 2) = 120 (5)
С учётом (3) формулу (4) можно записать как последовательность количества KN номеров N в Монадах последовательности n = 1; 2; 3; 4 Диад:
KN = 2(2n2) = 2Σ2(2n –1) = 2[2(1), 2(3 + 1), 2(5 + 3 + 1), 2(7 + 5 + 3 + 1)] (6)
Произведя суммирование и раскрытие скобок в правой части формулы (6), получим распределение количества KN номеров N в n = 1; 2; 3; 4 Диадах:

Это именно количества номеров, которые не обязательно должны следовать по определённому нарастающему порядку в монадах. Номера же должны последовательно нарастать. Номера N, в отличие от KN по формуле (6), должны выстраиваться в последовательных монадах 1–4 Диад по этой же простой формуле:
N = 2Σ2(2n –1), (7)
но в последовательно нарастающем порядке от 1 до 120.
Все значения KN чётные. Поэтому можно построить геометрическое воплощение формул (5) и (6) в виде вертикально-симметричной последовательности 20-ти рядов ячеек-квадратиков 8-ми Монад для 1-120 номеров N в n = 1; 2; 3; 4 Диадах-Уровнях сверху вниз:

Рис. 10. Вертикально-симметричное 4-Уровневое распределение ячеек-квадратиков для 1-120 номеров в 20-ти рядах 8-ми Монад по формуле (6)
Ряды 1, 2,4, 6, 9,12,16, 20 состоят из 2 ячеек, ряды 3, 5, 8, 11, 15, 19 – из 6 ячеек, ряды 7,10, 14, 18 – из 10 ячеек, ряды 13, 17 – из 14 ячеек. В целом форма с ячейками напоминает ветвистую Ёлку. Ряды с двумя ячейками выглядят стволом Ёлки. Очевидно, ствол отличается от ветвей. И первые ветви Уровней n = 2; 3; 4 отличаются друг от друга. Таким образом, Ёлка составлена из ствола и трёх разных ветвей. Эти очевидные различия отразим тонами серой шкалы (gray scale).

Рис. 11. Ячейки Ёлки в различных тонах серой шкалы
Первый ряд первой диады из двух ячеек задаёт однообразие стволовых ячеек первого типа в остальных нижележащих подобных семи рядах. Третий ряд (первый ряд во второй Диаде) задаёт шестиячеечный первый тип ветви Ёлки в нижележащих подобных пяти рядах. Седьмой ряд (первый ряд в третьей Диаде) задаёт десятиячеечный второй тип ветви Ёлки в нижележащих трёх подобных рядах. Тринадцатый ряд (первый ряд в четвёртой Диаде) задаёт четырнадцатиячеечный третий тип ветви Ёлки в нижележащем одном ряду. Таким образом, первые ряды с 2, 6,10,14 ячейками являются типозадающими для нижележащих подобных рядов, и все 120 ячеек закономерно подразделяются на 4 типа.
Пронумеруем ячейки последовательно в строго нарастающем порядке слева направо в рядах с последовательным переходом на нижележащие ряды сверху вниз. При этом номера n = 1, 2, 3, 4 Диад-Уровней и рядов 1-20, зафиксированные на рис. 10 и номера Диад-Уровней на рис. 11, опустим.

Рис. 12. Последовательная нумерация ячеек на рис. 11
В соответствии с разделением ячеек на четыре типа и последовательные номера 1-120 распределяется по этим четырём типам.
6. Преобразование формы Ёлки
Форма Ёлки на рис. 12 монотонна, 4 уровня выражены не чётко. Имеет смысл перейти к другой форме – Ёлке 1. Преобразование Ёлки к Ёлке 1 проводится последовательными перестановками наверх рядов нижних монад Диад на уровнях 2, 3 и 4, не нарушающими правило: от перестановки мест слагаемых (рядов) сумма не изменяется. Очевидно, преобразование должно быть обратимым:

Рис. 13. Преобразование Ёлки в Ёлку 1
Повернём Ёлку 1 на 90° против часовой стрелки в горизонтальное положение:

Рис. 14. Горизонтальное положение Ёлки 1.
Диады-Уровни 1, 2, 3,4 имеют конфигурации с последовательным наращиванием квадратиков от Квадрата из 4-х квадратиков до Прямоугольника 8 × 14 с симметричными ступенчатыми выемками.
Разнесём верхние и нижние части Диад-Уровней Ёлки 1 по горизонтальной оси симметрии так, чтобы из них образовалась непрерывная последовательность верхних и нижних половин Диад-Уровней:

Рис. 15. Последовательность верхних и нижних половин Диад-Уровней Ёлки 1 на рис. 14
Полученная картина напоминает «волну из симметричных половин Диад-Уровней. Они изменяются и по ширине, и по высоте на два квадратика. Такую «импульсную последовательность» распределения чисел-номеров нельзя называть периодической, потому что промежутки между импульсами (периоды) не постоянны. Но с учётом того, что ширина и размах импульсов последовательно увеличиваются на постоянное число 2, т. е. по арифметической прогрессии, полученную закономерность можно называть прогрессионно-периодической или кратко – про-периодической.
7. Свёртка ветвистой Ёлки 1 в компактную форму
Первая Диада в Ёлке 1 на рис. 13 уже в компактной форме Квадрата 2 × 2 из 4-х квадратиков с номерами: 1,2,3,4. Квадраты 2 × 2 можно рассматривать как квадратные слои первого типа, окаймляющие внутренний Квадрат со стороной, равной 0. Квадраты с квадратиками будем писать с прописной буквы К.
Во второй Диаде Ёлки 1 ячейки с номерами 5, 10 и 13, 16 переместим так, чтобы образовался второй тип Квадратного слоя из 12 ячеек, окаймляющий первый тип Квадратного слоя из ячеек с номерами: 11,12 и 19,20.
В третьей Диаде ячейки с номерами 31,36 и 49,54 переместим так, чтобы образовался второй тип Квадратного слоя из 12 ячеек, окаймляющий первый тип Квадратный слоя из ячеек с номерами: 37, 38 и 55, 56. Ячейки с номерами 21, 22, 23, 28, 29, 30 и ячейки с номерами 39, 40, 41, 46,47,48 переместим так, чтобы образовался третий тип Квадратного слоя из 20 квадратиков, окаймляющий второй тип Квадратного слоя.
В четвёртой Диаде ячейки с номерами 81, 86 и 113, 118 переместим так, чтобы образовался второй тип Квадратного слоя, окаймляющий первый тип Квадратного слоя из ячеек с номерами 87, 88, 119, 120.
Ячейки с номерами 71, 72,73 и 103, 104, 105 переместим так, чтобы образовался третий тип Квадратного слоя из 20 ячеек, окаймляющий второй тип Квадратного слоя. Ячейки с номерами 57–60, 67–70 и 89–92, 99-102 переместим так, чтобы образовался четвёртый тип Квадратного слоя с верхними номерами 57–70, и нижними номерами 89-102 из 28 ячеек, окаймляющий третий тип Квадратного слоя.
В результате этих перемещений получим свёртку разветвлённой Ёлки в компактную фигуру из Квадратов 2 × 2, 4 × 4, 6 × 6 и 8 × 8, напоминающую Монумент.

Рис. 16. Монумент из 1-120 ячеек в Квадратах 2 × 2, 4 × 4, 6 × 6, 8 × 8
Типизация пронумерованных ячеек тонами серой шкалы на рис. 11 сохранилась, но не в линейных рядах, а в концентрически замкнутых Квадратных слоях.
8. «Волновое» распределение чисел-номеров в половинах Квадратов
Вертикальную последовательность Квадратов 2 × 2, 4 × 4, 6 × 6, 8 × 8 сверху вниз на рис. 16 в уменьшенном масштабе переведём на горизонтальную их последовательность слева направо:

Рис. 17. Горизонтальная последовательность Квадратов 2 × 2, 4 × 4, 6 × 6, 8 × 8
Разнесём верхние и нижние половины Квадратов 2 × 2, 4 × 4, 6 × 6, 8 × 8 на рис. 17 в непрерывную последовательность вдоль срединной горизонтальной линии:

Рис. 18. Непрерывная последовательность половин Квадратов 2 × 2, 4 × 4, 6 × 6, 8 × 8 Уровней 1, 2, 3, 4
Получилась последовательность «волн прямоугольных импульсов» с нарастанием аргумента на 4 единицы, а амплитуды на 1 единицу с каждой последующей «волной». Нет определяющего признака периодичности – постоянства периода. Поэтому такая последовательность не является периодической в строгом определении понятия периодичности. Но, поскольку аргумент и амплитуда изменяются на постоянные числа в арифметической прогрессии от «импульса» к «импульсу», то полученную закономерность можно называть прогрессионно-периодической (про-периодической).
Таким образом, и для случая Диадной (Ёлочной), и для случая Квадратной (Монументальной) форм распределения натуральных чисел-номеров получается прогрессионно-периодическая (про-периодическая) закономерность в последовательности их распределения.
Ёлочное Диадное (рис. 12, 13.) и Монументальное Квадратное (рис. 16) распределения пронумерованных ячеек исключительно математического (теоретического) происхождения. Они могут быть эффективны для разных множеств объектов реального Мира, как искусственных, так и естественных. Например, в искусственных построениях таким может быть эффективный ступенчато-клинообразный строй бойцов, подразделений, боевых машин, танков, судов, самолётов, воинских соединений для прорыва оборонительных линий или наступательного фронта противника. Для естественных объектов можно сопоставить их с распределением множества химических элементов.
9. Распределения множества химических элементов
На рис. 12 и на рис. 16 ячейки с номерами дополним символами соответствующих химических элементов. Все существующие на сегодня химические элементы отнесены к 4-м блокам: s, р, d, f. Ячейки с химическими элементами этих блоков обычно отцвечивают соответственно красным, жёлто-оранжевым, синим и зелёным цветами. На нижеследующих рис. 19 и рис. 20 представлены числовая Ёлка на рис. 12 и Числовой Монумент на рис. 16 с символами химических элементов и в цветах ячеек s, р, d, f блоков. По логике формул (5) и (6) элементы 119 и 120 должны быть s-элементами. Но они ещё не обнаружены и не синтезированы. Ячейки с этими элементами отцвечены не красным, а тёмно-красным цветом.
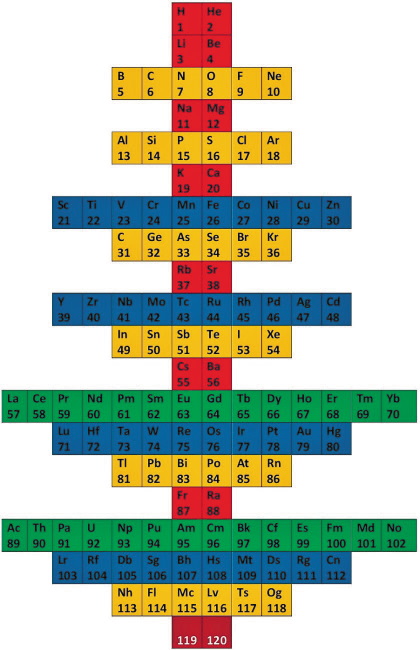
Рис. 19. Ёлка химических элементов

Рис. 20.Монумент химических элементов
Разделы 5 и 7 завершились выявлением четырёх типов ячеек, которые были зафиксированы различными тонами серой шкалы. Рассмотрим совместно Числовую Ёлку (рис. 12), числовой Монумент (рис. 16), Ёлку химических элементов (рис. 19) и Монумент химических элементов (рис. 20).

Рис. 21. Совместное представление рис. 12, рис. 19 и рис. 16, рис. 20
В Ёлочном распределении химических элементов первая пара s-элементов первого уровня проявляет свою типозадающую роль тем, что все пары «стволовых» элементов являются «красными» s-элементами. В Монументе химических элементов этот тип проявляется «красными» квадратиками в четырёх концентрических слоях из четырёх ячеек в Квадратах 2 × 2, 4 × 4, 6 × 6, 8 × 8.
Первая оранжевая «ветвь» второго уровня Ёлки химических элементов задаёт тип остальных р-элементов. В Монументе все p-элементы располагаются во вторых концентрических слоях, окаймляющих Квадраты из двух пар s-элементов.
Первая «синяя ветвь» третьего уровня Ёлки химических элементов задаёт тип остальных ветвей d-элементов. В Монументе все d-элементы располагаются в третьих концентрических слоях, окаймляющих вторые концентрические слои р-элементов.
Первая зелёная «ветвь» четвёртого уровня Ёлки химических элементов задаёт тип остальных 14-ти f-элементов. В Монументе все f-элементы располагаются в четвёртом концентрическом слое, окаймляющем третий концентрический слой из d-элементов.
Сравнение фигур 1 с 2 и 3 с 4 на рис. 21 показывает совпадение типизации ячеек тонами серой шкалы и ячеек с цветами s, р, d, f блоков. Поскольку Систематизация и типизация ячеек с номерами 1-120 на фигурах 1 и 3 тонами серой шкалы были проведены исключительно математически, то и фигуры 2 и 4 представляют математическую Систематизацию и Типизацию химических элементов. Математическая типизация совпадает с квантово-механической типизацией s, р, d, f – блоками.
Совпадение квантово-механической типизации химических элементов и их типизации на основе закономерностей распределения натуральных чисел в квадратах чётных чисел удивительно, даже поразительно. Ведь, что получается? Натуральные числа, чётные числа, нечётные числа известны человечеству тысячелетия. Это только человечеству. В природе, во Вселенной они всегда были. Химические же элементы начали открывать лишь в XVIII веке. А числа уже «знали» о четырёх типах химических элементов (!).
10.4-Уровневая Диадная Таблица химических элементов
Ячейки на рис. 19 последовательны, но с большим количеством «пустот» между Монадами и Диадами. Уплотнением фигуры, т. е. сокращением количества «пустот» между Монадами и Диадами, далее, расширением квадратиков до прямоугольников для возможности размещения в них дополнительной информации (атомные массы, электронную структуру, числа нуклонов….), наконец, размещением в рамки с номерами Уровней и Групп, можно получить 4-Уровневую Диадную Таблицу химических элементов:

Рис. 22. 4-Уровневая Диадная Таблица химических элементов
Наверху Таблицы помещены три симметричные полосы с номерами групп в ячейках s-, р-, d-, f-расцветок, в точности соответствующие цветам ячеек в рядах этих элементов. Групп XXXII, но столбцов всего 14. У Периодической Таблицы IUPAC XVIII групп и 18 столбцов. Номера групп в цветных ячейках трёх полос в точности указывают на элементы-аналоги по всем столбцам Таблицы. Слева сбоку указаны номера Уровней (Диад). Их только 4. Каждый Уровень состоит из двух количественно равных половин. Они в Периодической Таблице IUPAC представляются Периодами. Все элементы располагаются